SDS细胞裂解液(含PMSF)
保存:-20℃保存,一年有效。
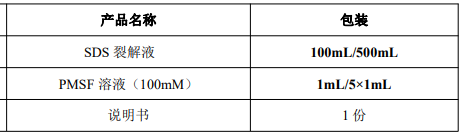
包装内容:
产品简介:
SDS 裂解液(SDS Lysis Buffer)是一种比较强烈的细胞组织裂解液。SDS 裂解液裂解得到的蛋白样品可以用于常 规的 Western、ChIP(染色质免疫共沉淀,chromatin immunoprecipitation)等。
用 SDS 裂解液裂解得到的蛋白样品,可选用本公司生产的 BCA 蛋白浓度测定试剂盒测定蛋白浓度。
由于 SDS 裂解液含有较高浓度的去垢剂,不能用 Bradford 法测定由本产品裂解得到样品的蛋白浓度。
SDS 裂解液含多种蛋白酶抑制剂。可以有效抑制蛋白降解,但需避免反复冻融。
使用方法
对于培养细胞样品:
1. 融解 SDS 裂解液,混匀。取适当量的裂解液,在使用前数分钟内加入 PMSF,使 PMSF 的最终浓度为 1mM。
2. 对于贴壁细胞:去除培养液,用 PBS、生理盐水或无血清培养液洗一遍(如果血清中的蛋白没有干扰,可以不洗)。按照 6 孔板每孔加入 150-250 微升裂解液的比例加入裂解液。用枪吹打数下,使裂解液和细胞充分接触。通常裂解液接触细胞 1-2 秒后,细胞就会被裂解。如果用于 ChIP,初步裂解后需在冰浴上继续裂解 10 分钟。
对于悬浮细胞:离心收集细胞,用手指把细胞用力弹散。按照 6 孔板每孔细胞加入 150-250 微升裂解液的比例加入裂解液。再用手指轻弹以充分裂解细胞。充分裂解后应没有明显的细胞沉淀。如果细胞量较多,必需分装成 50-100 万细胞/管,然后再裂解。如果用于 ChIP,初步裂解后需在冰浴上继续裂解 10 分钟。
3. 充分裂解后,10000-14000g 离心 3-5 分钟,取上清,即可进行后续的 PAGE、Western 和免疫沉淀等操作。
裂解液用量说明:通常 6 孔板每孔细胞加入 150 微升裂解液已经足够,但如果细胞密度非常高可以适当加大裂解液的用量到 200 微升或 250 微升。如果用于 ChIP,建议 6 孔板每孔细胞至少加入 200 微升裂解液。每 100 万细胞用 100 微升本产品裂解后获 得的上清,其蛋白浓度约为 2-4mg/ml,不同细胞有所不同。
对于组织样品:
1. 把组织剪切成细小的碎片。
2. 融解 SDS 裂解液,混匀。取适当量的裂解液,在使用前数分钟内加入 PMSF,使 PMSF 的最终浓度为 1mM。
3. 按照每 20 毫克组织加入 150-250 微升裂解液的比例加入裂解液。(如果裂解不充分可以适当添加更多的裂解液,如果需要高浓度的蛋白样品,可以适当减少裂解液的用量。)
4. 用玻璃匀浆器匀浆,直至充分裂解。如果用于 ChIP,初步裂解后需在冰浴上继续裂解 10 分钟。
5. 充分裂解后,10000-14000g 离心 3-5 分钟,取上清,即可进行后续的 PAGE、Western 和免疫沉淀等操作。
6. 如果组织样品本身非常细小,可以适当剪切后直接加入裂解液裂解,通过强烈 vortex 使样品裂解充分。然后同样离心取上清,用于后续实验。直接裂解的优点是比较方便,不必使用匀浆器,缺点是不如使用匀浆器那样裂解得比较充分。
注意事项:
* 为取得最佳的使用效果,尽量避免过多的反复冻融。购买后可以适当分装后使用。
* 裂解样品的所有步骤都需在冰上或 4℃进行。
* 关于裂解液的选择,一方面可以参考我们提供的裂解液成分、特点进行选择,另一方面也需要通过一些预实验来摸索最佳的适合您实验条件的裂解液。
* 为了您的安全和健康,请穿实验服并戴一次性手套操作。
特别提示:本公司的所有产品仅可用于科研实验,严禁用于临床医疗及其他非科研用途!
