2×CTAB裂解液(除菌)
储存条件:常温保存,保质期 2 年。
产品内容:
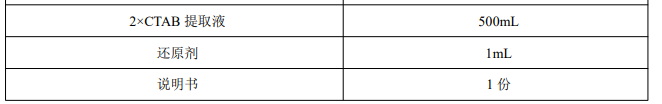
产品说明:
CTAB(hexadecyltrimethylammonium bromide,十六烷基三甲基溴化铵),是一种阳离子去污剂,具有从低离子强度溶液中沉淀核酸与酸性多聚糖的特性。在高离子强度的溶液中(0.7mol/L NaCl),CTAB 与蛋白质和多聚糖形成复合物,只是不能沉淀核酸.通过有机溶剂抽提,去除蛋白、多糖、酚类等杂质后加入乙醇沉淀即可使核酸分离出来。
使用方法:
一、试剂准备
1、氯仿-混合液(24:1)。96mL 氯仿加 4mL 混匀。
2、65℃预热 CTAB 溶液后将 1mL 还原剂加入 CTAB 溶液中。
二、操作步骤
1、液氮研磨 0.1g左右植物组织,转移到 1.5mL 离心管中,加入 700uL 2×CTAB 提取液(已加入还原剂)。
或者液氮研磨之后,在研钵中加入 700uL 2×CTAB 提取液,然后吸取到 1.5mL 的离心管中(建议总体积不要超过 1mL)。
2、将离心管置于 65℃水浴 30min-1h,期间每隔 10min 左右轻轻晃动离心管。
3、水浴完成后冷却 2min,加入 0.5mL 的氯仿-混合液,剧烈震荡混匀。10000-12000rmp 离心 5-10min。
4、取上步离心管中上清液到新的离心管中。
注意:上步离心后应该会分三层:上层为水相,中间为蛋白和植物碎片,下层为有机相。吸取时避免触及蛋白和有机相。如不小心吸取到中下层,或者中间层较厚,建议少吸取水相,或吸取之后再加入 500uL 氯仿-混合液,重新混匀离心取上清。
5、在上清中加入等体积的异丙醇,颠倒混匀。(或加入 2 倍体积的无水乙醇和 1/10 体积的 3M pH5.2 的乙酸钠) 。置于-20℃沉淀 30min 以上,12000rmp 离心 10min,弃上清。
6、 沉淀用 75%乙醇洗涤 1 次,12000 r/min 离心 3-5 min,弃上清,沉淀自然干燥后溶于 50uL 去离子水或者 TE 中,加入 1 uL RNase(20 ug/mL),37 摄氏度温育 30 min。
7、置于-20℃保存。
备选方案:
1、可以加入适量 PVP 去除多糖多酚污染。PVP(聚乙烯酮)是酚的络合物,能与多酚形成一种不溶的络合物质,有效去除多酚,减少 DNA 中酚的污染;同时它也能和多糖结合,有效去除多糖。
2、可以在加入 CTAB 提取液之后震荡混匀,5000rmp 离心 2min 取上清,沉淀为未研磨充分的碎片或者不溶物。然后在上清中加入氯仿-混合液纯化,可以有效去除未裂解的植物碎片。
3、可以在加氯仿-混合液之前,加入 tris 酚(pH>7.8)-氯仿混合液震荡离心取上清后,再用氯仿-混合液纯化。可以有效去除蛋白污染。
常见问题:
问题一:DNA 样品不纯,抑制后续酶解和 PCR 反应。
原因:1.DNA 中含有蛋白、多糖、多酚类杂质
2.DNA 在溶解前,有酒精残留,酒精抑制后续酶解反应
3.DNA 中残留有金属离子
对策:1.重新纯化 DNA,去除蛋白、多糖、多酚等杂质(具体方法见前)
2.重新沉淀 DNA,让酒精充分挥发
3.增加 70%乙醇洗涤的次数(2-3 次)
问题二:DNA 降解,DNA 提取量少。
原因:1.实验材料不佳或量少
2.破壁或裂解不充分
3.沉淀不完全
4.洗涤时 DNA 丢失对策:1.尽量选用新鲜(幼嫩)的材料
2.动植物要匀浆研磨充分;G+菌、酵母裂解前先用生物酶或机械方式破壁
3.高温裂解时,时间适当延长(对于动物细胞、细菌可增加裂解液的用量)
4.低温沉淀,延长沉淀时间
5.加辅助物,促进沉淀
6.洗涤时,最好用枪头将洗涤液吸出,勿倾倒
特别提示:本公司的所有产品仅可用于科研实验,严禁用于临床医疗及其他非科研用途!
