相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 询价记录
- 文献和实验
- 技术资料
- 提供商:
江苏集萃药康生物科技股份有限公司
- 服务名称:
BALB/cJGpt-Tg(hCD3E BAC)102/Gpt
BALB/c-hCD3E
品系名称:BALB/cJGpt-Tg(hCD3EBAC)102/Gpt
品系类型:转基因
品系编号:T001550
背景:BALB/cJGpt
品系描述
CD3E全名为CD3Emolecule,存在于T细胞表面,与CD3其他亚基分子及T细胞受体α/β和γ/δ异二聚体一起构成T细胞受体-CD3复合物(TCR-CD3),参与T细胞的信号转导[1,2]。研究表明,CD3E在T细胞发育中扮演者重要角色,此基因缺陷可导致严重的免疫缺陷疾病[3,4]。部分TCR-CD3复合物存在于T淋巴细胞表面,接受抗原呈递细胞信号,激活胞内下游信号通路,在适应性免疫应答中起重要作用[5]。
基于CD3靶点的双特异性抗体(CD3-TCB)在淋巴瘤的治疗方面大放异彩。CD3-TCB特异性识别T细胞上的靶分子CD3,同时又能够识别肿瘤特异性靶点,从而激发T细胞的靶向性免疫反应并带来特异性杀伤[6]。
集萃药康利用转基因技术开发了BALB/c-hCD3E小鼠模型。BALB/c-hCD3E转基因小鼠可在CD3E自身启动子调控序列的控制下在T细胞表面表达人源CD3E蛋白,且hCD3E表达量与小鼠自身mCD3E表达量相当。经验证,该人源化小鼠体内的hCD3E分子表现出良好的功能活性,参与机体免疫反应。当我们将BALB/c-hCD3E小鼠中的mCd3e敲除后,获得BALB/c-hCD3E/mCd3e-KO模型,该模型小鼠的脾脏和外周血的T细胞相对量明显下降(极显著,p=0.0021),且CD8+T细胞和CD4+T细胞比例和数量发生了显著变化。当用anti-mCTLA4抗体处理接种CT26细胞的小鼠时,BALB/c-CD3E小鼠有明显的肿瘤生长抑制作用,而BALB/c-hCD3E/mCd3e-KO小鼠无明显反应。结果表明,mCd3e对BALB/c-hCD3E转基因小鼠T细胞的发育和功能起着不可或缺的作用。
为了BALB/c-hCD3E品系能更好的评价双特异性抗体,我们建立相应的人源化肿瘤细胞系库,涵盖了CD3E双特异性抗体的热门靶点。将CD3E人源化小鼠与对应靶点人源化的细胞系相结合的评价体系,使双特异性抗体药物的评价更有效。
应用领域
-
T细胞的发育和活化研究
-
筛选以CD3E为基础的双特异性抗体
验证数据
BALB/c-hCD3E小鼠hCD3E表达及免疫系统分析
-
hCD3E蛋白表达分析
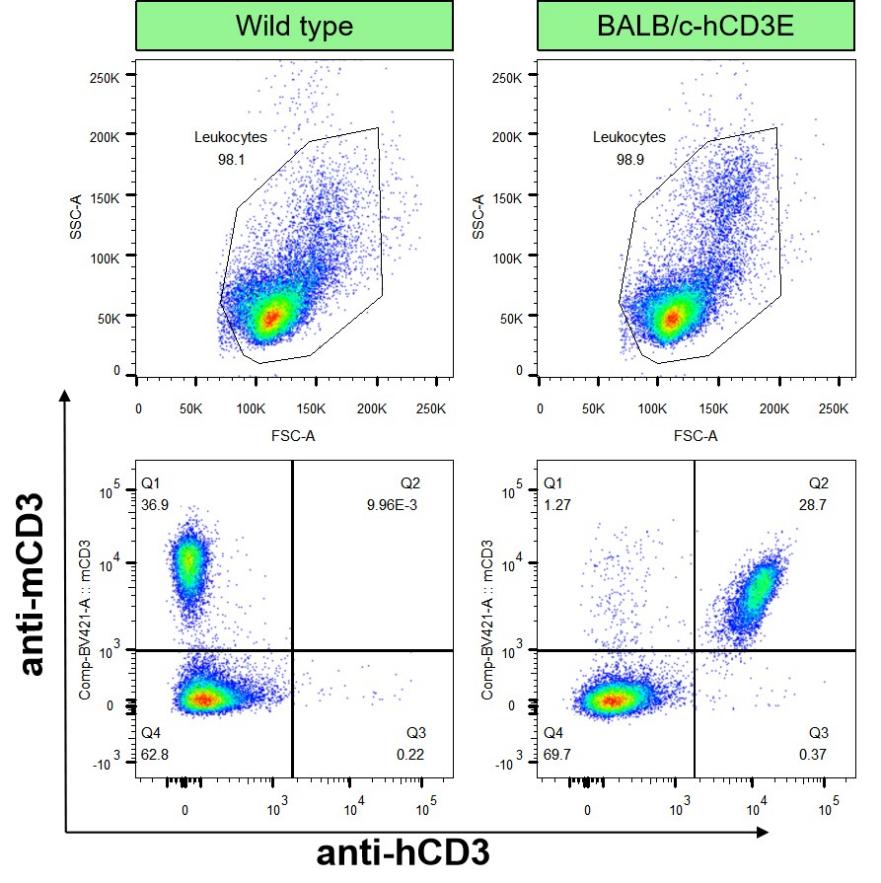
图1BALB/c-hCD3E小鼠hCD3E表达检测
BALB/c-hCD3E小鼠T细胞表面能成功表达hCD3E,且96%的CD3+T细胞表面共表达mCD3E及hCD3E。
-
T/B/NK细胞比例检测
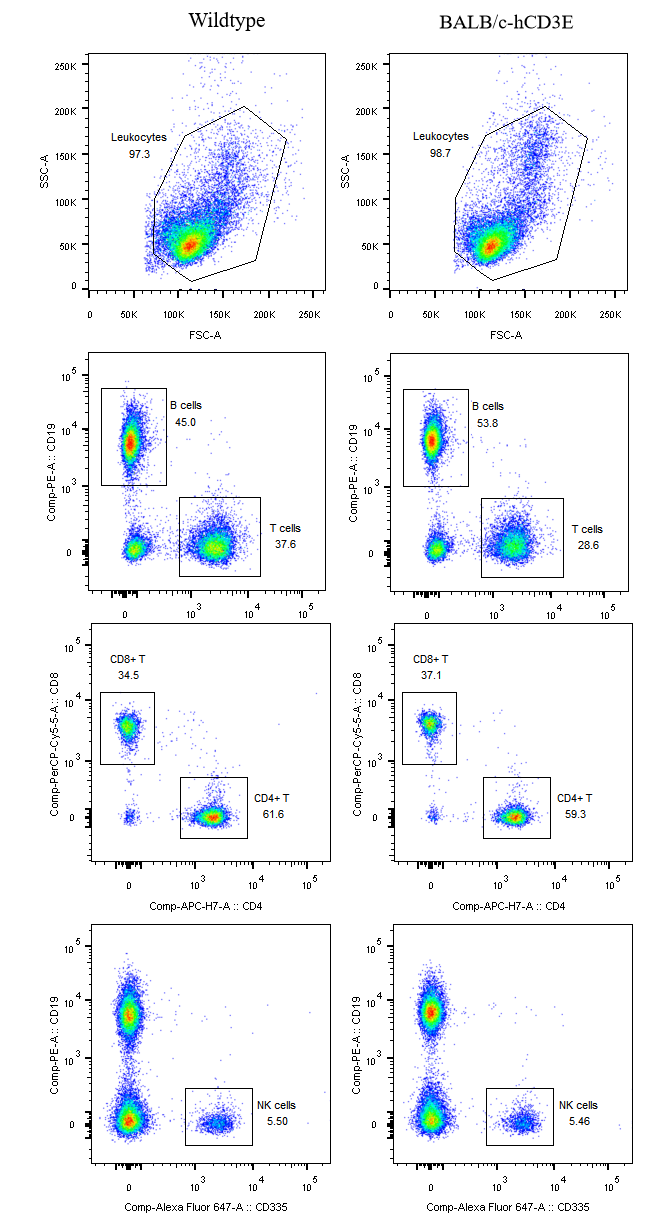
图2BALB/c-hCD3E小鼠体内T/B/NK细胞比例检测
BALB/c-hCD3E小鼠体内T/B/NK细胞比例与野生型小鼠类似。
-
细胞因子释放


图3BALB/c-hCD3E小鼠对抗体刺激的响应
BALB/c-hCD3E小鼠对anti-hCD3E及anti-mCd3e抗体刺激均有响应,野生型BALB/c仅对anti-mCD3E抗体刺激有响应。BALB/c-hCD3E脾脏细胞经anti-hCD3E及anti-mCD3E抗体刺激后,细胞因子TNF、IL2及IFNγ水平均升高且趋势类似,且与野生型BALB/c脾脏细胞经anti-mCD3E抗体刺激后,细胞因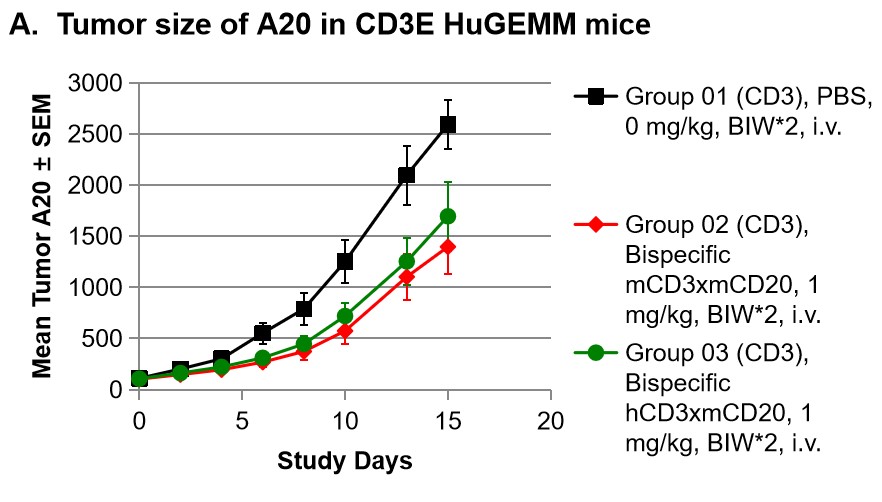
子水平升高程度类似。
-
体
内药效
图4基于BALB/c-h的体内药效试验(与Crownbio合作验证)
A20在hCD3E小鼠中的肿瘤大小(平均体积±SEM),(B)使用CD3/CD20双特异性抗体后,小鼠血液中的B细胞耗竭。将对数生长期A20肿瘤接种至6-8周龄的BALB/c-hCD3E小鼠皮下,待肿瘤生长至平均体积约100mm3时随机分为PBS(对照)组,BispecificmCD3xmCD20药物组及BispecifichCD3xmCD20药物组(n=8),并使用相应的药物进行治疗。每周给药两次,共给药4次。
实验结果:BispecifichCD3xmCD20和BispecificmCD3xmCD20对肿瘤生长有相似的抑制作用(BispecifichCD3xmCD20治疗组TGI=42%,BispecificmCD3xmCD20治疗组TGI=50%)。BispecifichCD3xmCD20治疗后,BALB/c-hCD3E小鼠血液中的B细胞被消耗,而wt-BALB/c小鼠血液中的B细胞无明显变化。
结果证明:BALB/c-hCD3E小鼠是评估CD3E双特异性抗体体内药效的理想模型。
BALB/c-hCD3E/mCd3e-KO小鼠免疫系统分析
-
T/B/NK细胞比例检测
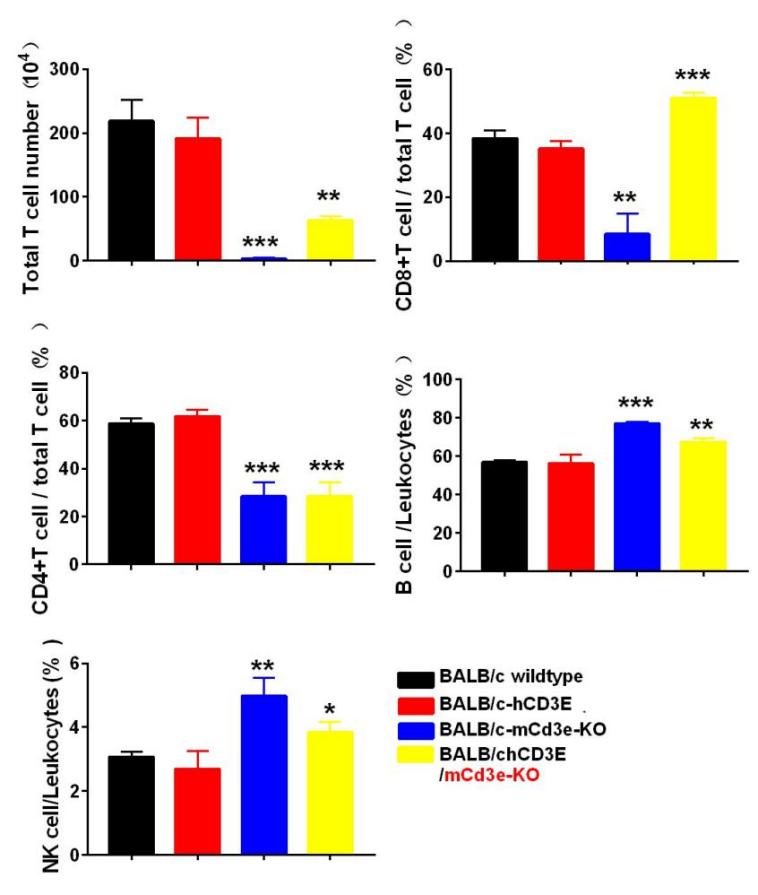
图5BALB/c-hCD3E/mCd3e-KO小鼠体内T/B/NK细胞比例检测
与野生型和BALB/c-hCD3E小鼠相比,BALB/c-hCD3E/mCd3e-KO小鼠脾脏T细胞数量明显减少,CD4+T和CD8+T细胞百分比和数量也减少。
-
体内药效

图6基于BALB/c-hCD3E和BALB/c-hCD3E/mCd3e-KO小鼠的体内药效。
BALB/c-hCD3E和BALB/c-hCD3E/mCd3e-KO小鼠皮下接种小鼠结肠癌CT26细胞。当肿瘤平均体积达到100mm3时,小鼠给予vehicle或anti-mCTLA4治疗,初始给药每2天一次,共4次,后续每3天给药1次,共3次。结果表明,经anti-mCTLA4抗体治疗,BALB/c-hCD3E小鼠对肿瘤细胞生长有较强的抑制作用(TGI=61.68),但BALB/c-hCD3E/mCd3e-KO小鼠无明显抑制作用。
结果表明:在BALB/c-hCD3E小鼠中,mCD3E是不可缺少的,BALB/c-hCD3E小鼠是评估CD3E双特异性抗体体内药效的理想模型。
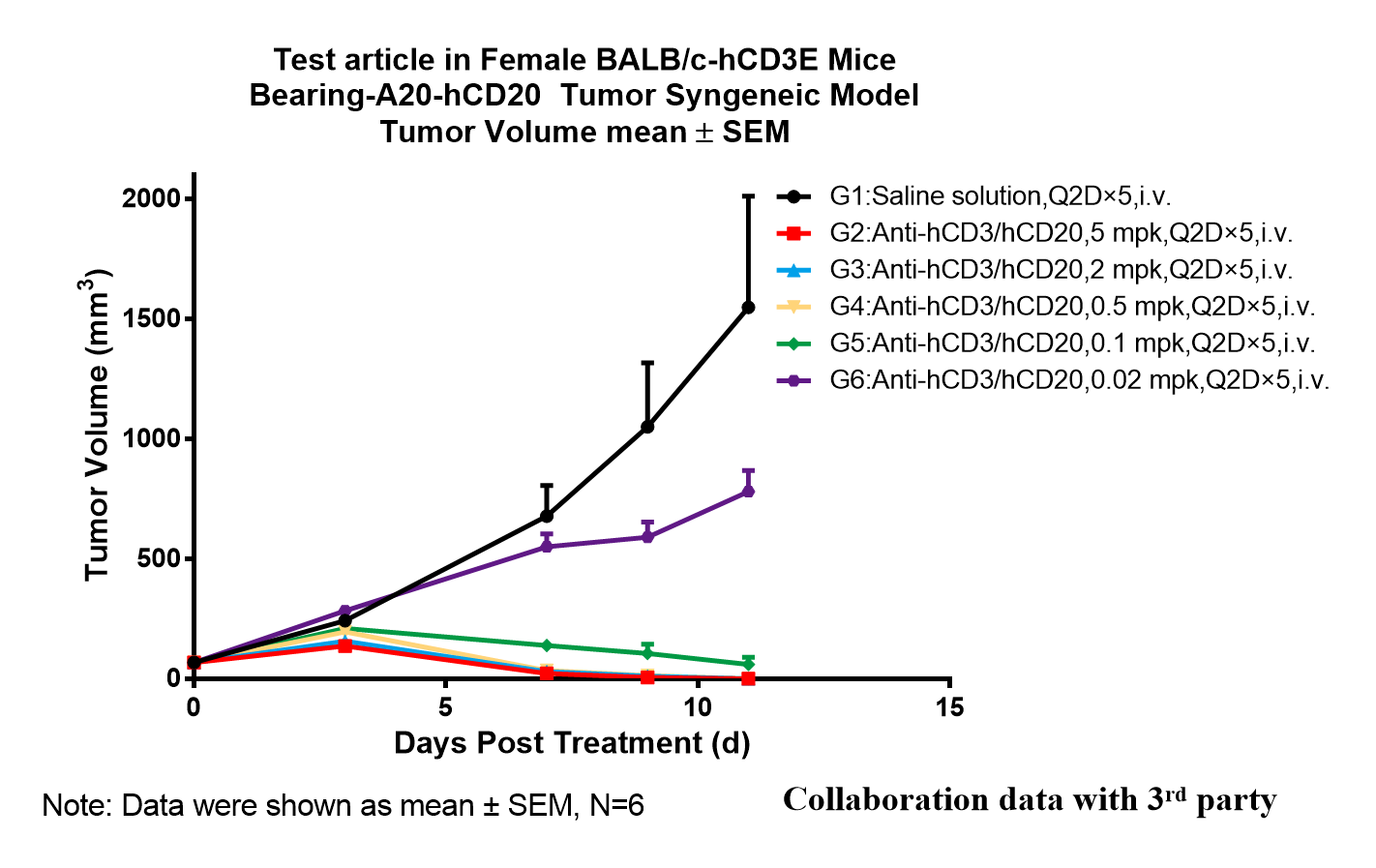
图7基于BALB/c-hCD3E小鼠接种CT26模型评价Anti-hCD3/hCD20的体内药效试验
将对数生长期的CD20人源化的小鼠B淋巴癌细胞A20-hCD20接种至6到9周龄的BALB/c-hCD3E小鼠皮下,待肿瘤生长至平均体积约105mm3左右时时随机分为PBS组,Anti-hCD3/hCD20(0.02mpk、0.1mpk、0.5mpk、2mpk和5mpk)给药组(n=8),并使用相应的药物进行治疗。每周给药两次,共给药6次。结果显示:Anti-hCD3/hCD20(0.02mpk、0.1mpk、0.5mpk、2mpk和5mpk)对肿瘤体积有明显的抑制率,且在G5组低浓度条件对肿瘤的生长就有了一定抑制作用。
结果表明:BALB/c-hCD3E小鼠可以用来评价双特异性抗体体内药效的理想模型。
-
人源化的肿瘤细胞

参考文献
-
Yamazaki, Tetsuo, et al. "CAST, a novel CD3ε-binding protein transducing activation signal for interleukin-2 production in T cells." Journal of Biological Chemistry 274.26 (1999): 18173-18180.
-
Kuhn, Chantal, et al. "Human CD3 transgenic mice: preclinical testing of antibodies promoting immune tolerance." Science Translational Medicine 3.68 (2011): 68ra10-68ra10.
-
Soudais, Claire, et al. "Independent mutations of the human CD3–ε gene resulting in a T cell receptor/CD3 complex immunodeficiency." Nature genetics 3.1 (1993): 77.
-
de Saint Basile, Geneviève, et al. "Severe combined immunodeficiency caused by deficiency in either the δ or the ε subunit of CD3." The Journal of clinical investigation 114.10 (2004): 1512-1517.
-
Dreier, Torsten, et al. "T cell costimulus-independent and very efficacious inhibition of tumor growth in mice bearing subcutaneous or leukemic human B cell lymphoma xenografts by a CD19-/CD3-bispecific single-chain antibody construct." The Journal of Immunology 170.8 (2003): 4397-4402.
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
- 作者
- 内容
- 询问日期
 文献和实验
文献和实验10b基因连接到脂肪组织特异表达的FABP4启动子上,通过常规转基因技术获得转基因小鼠。在FABP4启动子调控下,转基因小鼠脂肪组织中Wnt10b表达比正常情况高50倍。Wnt10b基因在正常小鼠的白色和棕色两种脂肪组织内的作用不同,转基因小鼠只有正常白色脂肪的一半,而没有棕色脂肪,这使得它无法维持自身体温从而容易受到寒冷的攻击。研究人员无法解释这种转基因小鼠的皮肤比正常小鼠厚2倍,体重较重,耗氧量也较少,然而更奇怪的是它们活得都很健康。 脂肪组织负责产生机体响应胰岛素的leptin
脑梗是研究缺血性脑中风的经典动物模型。沿颈部正中开口,钝性分离皮下组织,游离出颈总动脉1.5cm,穿线备用,向远心端找到颈外侧动脉,游离涌现结扎,提起颈总备用线,在近心端,远心端用动脉夹夹住,在近心端动脉夹处,用5mL注射器针头刺破血管,稍微提起动脉夹,用镊子夹住线栓,从小口插入动脉后,去掉远心端动脉夹,然后用镊子夹住线栓,线栓插入到颈内距分叉处1.8-2.0cm,用备用线将颈总和线栓一起结扎住,最好是结扎双道,记录线栓插入时间,在将动脉夹另一边近心端颈总结扎住,去掉动脉夹,注意缝合时不要
输卵管转移前一天晚上与切除输精管小鼠交配的假孕母鼠,注射当天早上母鼠可见精栓。尽管像Swiss Webster系的哺育母鼠很容易超重,随着体重的增加,它们将表现出不同程度的感觉消失,但它们是优良的哺育母鼠。另外,它们的价格也便宜。另一个成功的鼠系是B6D2F1,它们生命力强并有一定杂合优势。(3)麻醉剂:阿佛丁被证明是输卵管转移手术的有效麻醉剂。(三)实验操作程序和方法1.鼠系克隆(1) 动情期的探测:在转基因动物模型的建立中母鼠动情期的监测有很高的技巧性。小鼠的动情期主要划分为四个时期:① 动情
 技术资料
技术资料暂无技术资料 索取技术资料







![B6[GF] 无菌鼠](https://img1.dxycdn.com/2023/0215/858/4978763752213010063-14.jpg!wh200)


