粒曼生物科技(武汉)有限公司
3 年
手机商铺
- NaN
- 0
- 0
- 0
- 0
推荐产品
技术资料/正文
问题解读 | 细胞基因敲除后的验证问题来源于实验技术操作还是科研试剂行业?【收藏】
109 人阅读发布时间:2025-04-07 11:09

一、问题背景介绍
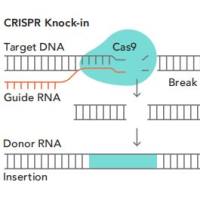
在生命科学研究等众多领域,基因敲除技术(如:CRISPR/Cas9)已成为解析基因功能、探索疾病机制及研究药物靶点等常用的、关键工具。然而,在“基因敲除后的验证”这一看似“不起眼”的环节,科研论文中鲜有进行系统性地分析和着重对待。不过,可喜的是,针对抗体质量问题越来越引起学术界和产业界的重视,国际抗体验证工作组(IWGAV)从2016年Nature发表文章认为:“验证抗体特异性是目前确保抗体可重复性最重要的步骤。”

2024年11月4日,Diana Kwon在Nature期刊发表评论文章,探讨了有关这一问题的现状和学术界、产业界做出的改变举措。

为什么细胞基因敲除验证的问题,会如此重视抗体的质量问题呢?
究其原因是因为:科研人员总“习惯性”地采用“Western Blot”的结果来证明基因敲除细胞的“成功性”。这种习惯性来自众多的方面:大量参考文献是这样的,以及同门师兄师姐也是这样的。我们尚且不去详细讨论这两个不同的概念和关系(下一期问题解读:何为成功的基因敲除?何为成功的WB实验,成功的WB实验就能代表成功的基因敲除吗?),就在上述的思路下,我们继续往下进行。采用WB实验,就必然用到‘抗体“,抗体的特异性和亲和力就成为WB实验成功的关键。这就是为什么“细胞基因敲除验证”的问题,为什么绕不开“抗体”的质量问题。
粒曼团队专注于提供细胞基因敲除解决方案,在提供高质量的服务过程中,自然产生了这个“细胞基因敲除验证”的行业拷问问题:究竟是单纯的实验技术问题(基因敲除的设计问题、细胞实验操作问题、WB实验操作问题等),还是与科研试剂行业问题(抗体试剂等)紧密相连。实则却是一个涉及多方面复杂因素的议题。接下来,我们通过“典型案例分析”,试图去阐释细胞基因敲除定制服务行业,不得不面临的“售后”问题。
基于此问题的阐释,粒曼团队正式推出:
LM NGMSTM验证平台: 粒曼“NGS二代测序+MS蛋白质谱”双重验证体系,从“根”上解决细胞基因敲除验证问题,完美绕开抗体行业问题(让“抗体”再跑一会儿~)——细胞基因敲除验证“金标准”验证服务
二、验证问题典型案例分享
案例一:不同厂家的抗体,获得不同的“敲除验证”结论
我们发现针对相同的靶蛋白,不同厂家抗体检测有明显的差异结果;下图分别为厂家A和厂家B,针对同批次的WT细胞和KO细胞裂解液进行WB检测的结果,厂家A抗体在目的蛋白大小位置WT细胞与KO细胞中均由条带,未发生敲除效果,厂家B抗体在目的蛋白大小位置KO细胞条带完全消失,有明显的敲除效果。出现上述的结果,我们该如何确定敲除验证的结论呢?
(备注:厂家A和B都是知名的抗体厂家,基于粒曼目前的数据显示,该情况出现的比例较多,我们将开始新的公众号文章系列“案例分享”,系统全面的推进该种案例的展示:将公开靶点蛋白信息,逐步推进常见靶点-优质单抗的KO验证进程。)
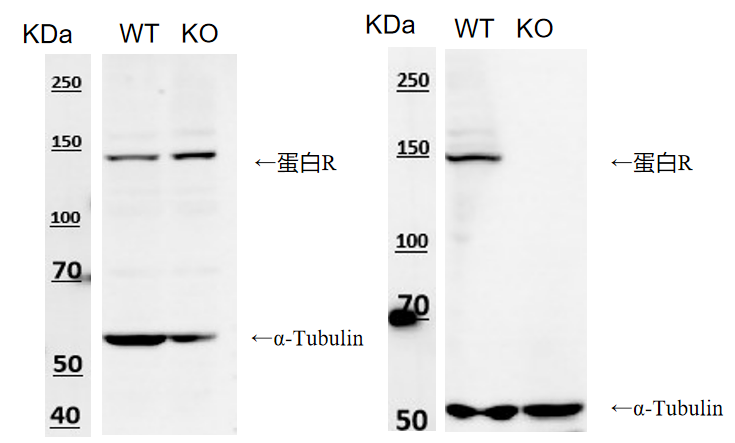 图1 不同厂家抗体针对相同的基因敲除细胞WB结果
图1 不同厂家抗体针对相同的基因敲除细胞WB结果
案例二:基因水平100%敲除,抗体显示无敲除(市面只有一款Abxxx单抗)
我们构建的一株基因敲除细胞系,在基因水平验证显示100%敲除,WB验证显示KO细胞与WT细胞条带都很亮。在售前分析中,我们在粒曼内部数据库显示:该靶点蛋白在该目的细胞中,mRNA水平以及蛋白水平都显示不表达。基于对基因水平的确凿证据以及蛋白表达水平(对WT细胞进行质谱检测)的“未检测到”的结果。出现上述的结果,我们实事求是去确定问题的关键:该WB的条带,能不能证明“该靶点”的存在?
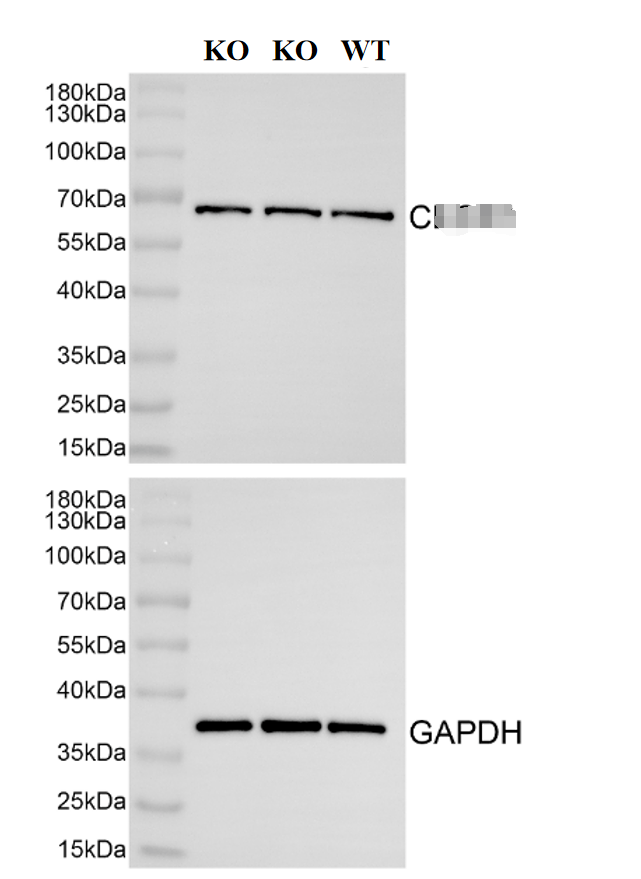
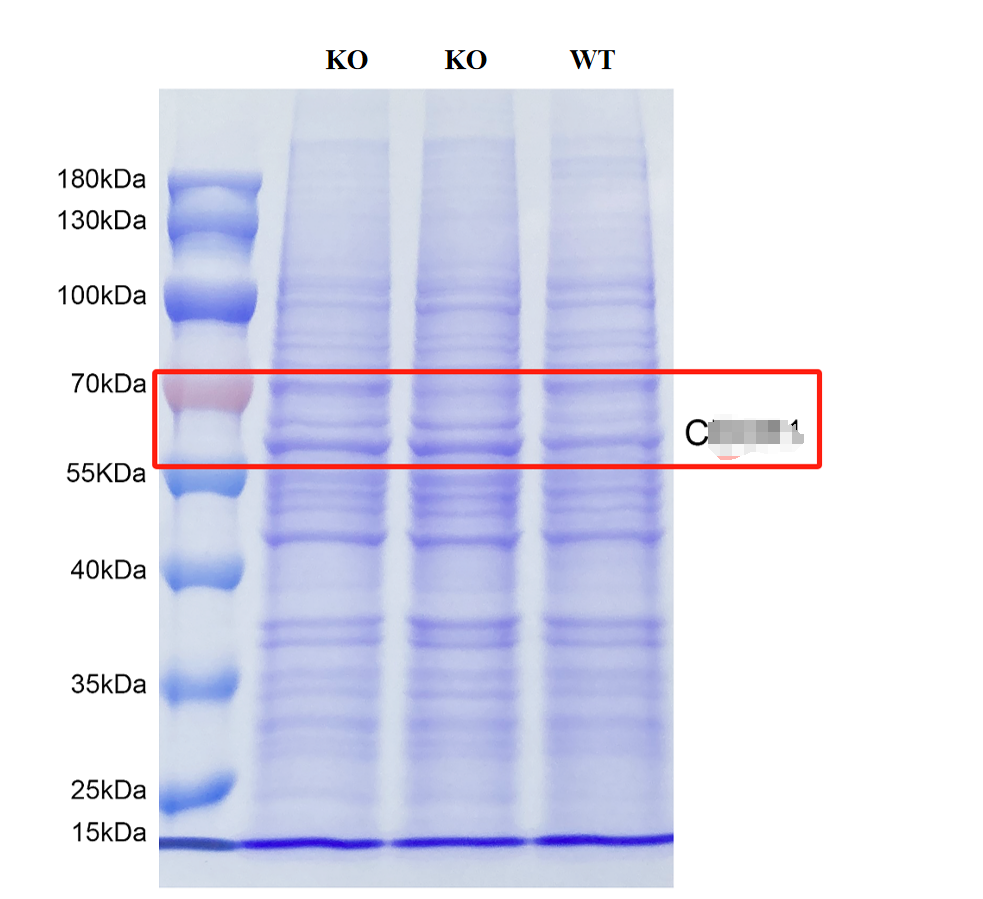 图2 知名抗体厂家X靶点WB检测结果以及切胶回收X蛋白大小区域展示(切胶区域质谱检测)
图2 知名抗体厂家X靶点WB检测结果以及切胶回收X蛋白大小区域展示(切胶区域质谱检测)
考虑抗体特异性问题,我们对蛋白条带进行了切胶,采用质谱方法对目的蛋白大小区域的切胶条带进行质谱鉴定。
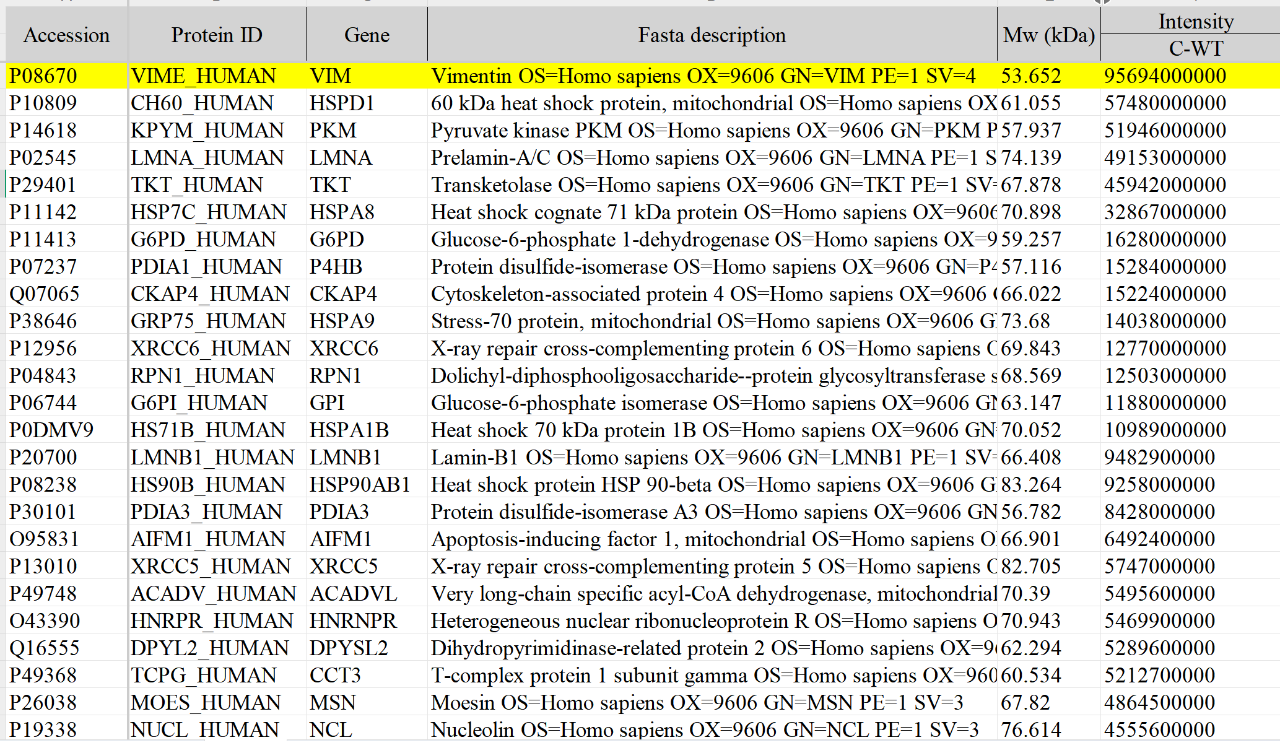
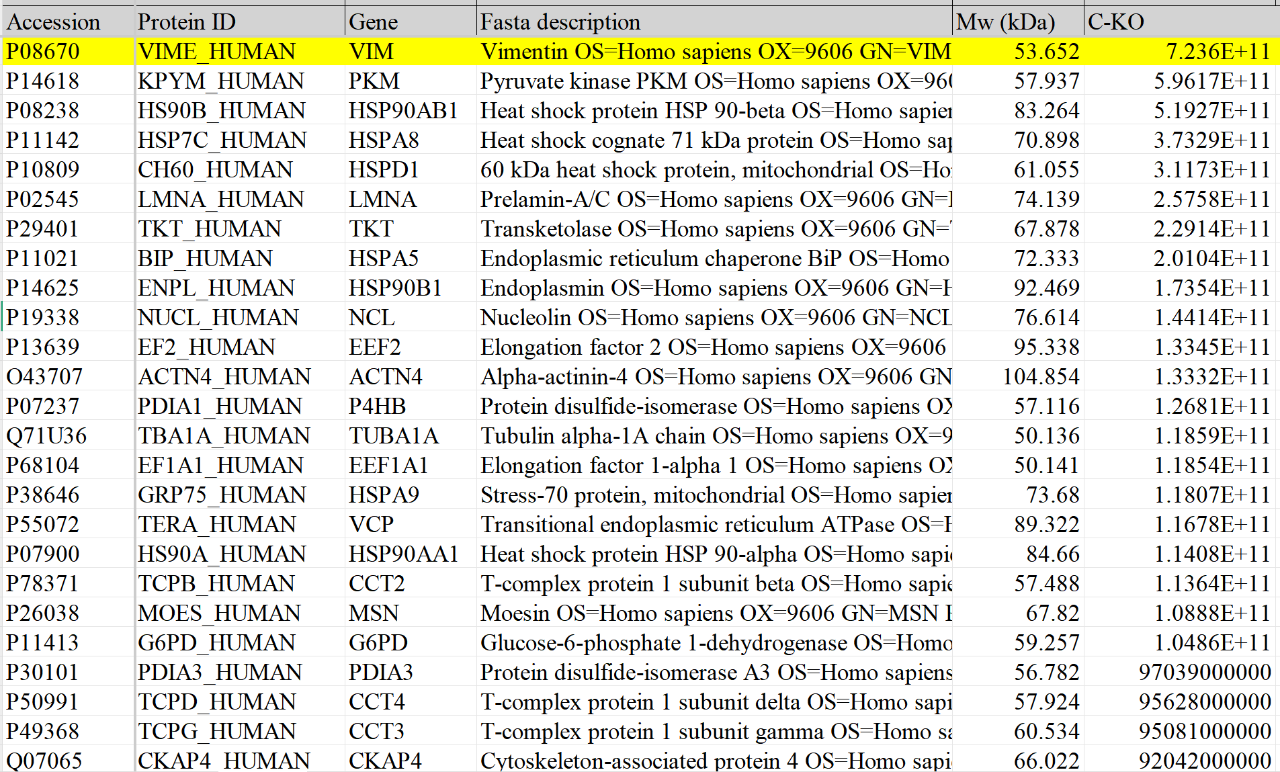
图3 WT细胞X蛋白胶条鉴定结果(上)和KO细胞X蛋白胶条鉴定结果(下)
从蛋白胶条鉴定结果显示,在对应目标条带大小的位置未鉴定到目标蛋白C。由此推测,WB检测抗体杂到的条带可能并非目标条带,只是与目标蛋白的预期大小比较一致而已。
(该结果已与该国际知名抗体品牌厂家进行沟通,反馈客户协商解决。粒曼团队基于“LM NGMS验证平台”正在持续针对国际及国内知名科研抗体品牌厂家进行系统的抗体验证实验,并为国内药企及高端科研客户提供质量保障的抗体筛选服务及产品。粒曼KO细胞裂解液,全面完成基因水平+质谱蛋白水平全验证,目前已逐步成为国内科研抗体行业抗体特异性质控的“标准品”。)
三、基因敲除后的验证方法概述
(一)基因组水平验证
- 一代测序(Sanger 测序法)验证敲除效率:在 CRISPR/Cas9 基因编辑技术中,通过设计引物 PCR 扩增sgRNA 涵盖的敲除区域,将野生型(WT)及基因敲除(KO)样本的 PCR 产物进行 Sanger 测序比对。若 KO 细胞对应基因碱基序列出现缺失或者非三倍数的移码,会致使后续阅读框移码,往往产生提前终止密码子(PTC),导致蛋白功能丧失,达成敲除效果。此方法优点在于实验及数据分析操作简便,能从基因组水平验证敲除效果。但前期 sgRNA 及引物设计策略需极为精确且全面考量。粒曼生物专有的敲除效率分析软件可对 Sanger 测序结果进行分析,得出敲除细胞的基因型及准确的 KO 效率数据。
- 二代测序(NGS测序法)验证敲除效率:通过对基因组 DNA 进行片段化处理,然后在片段两端连接特定的接头,构建测序文库。接着,利用测序仪器对文库中的 DNA 片段进行高通量测序,获得大量的短序列 reads。这些 reads 经过生物信息学分析,与参考基因组进行比对,从而可以确定基因编辑的位点以及检测基因敲除的效率,还能针对目标敲除区域深度分析,还能全面扫描全基因组,检测潜在脱靶位点及其他相关基因变化,了解基因敲除对整体基因组的影响,提供更全面的基因敲除情况评估。粒曼NGS二代测序将全面升级基因水平验证能力,作为“标准交付”在实验报告中。(请咨询我们了解详情)
(二)蛋白质水平验证
蛋白质水平的检测是鉴定基因敲除效果的重要手段。通过 Western blot(蛋白质免疫印迹)或蛋白质谱等实验方法检测蛋白质表达量,判断基因敲除是否成功。
- 在 Western blot 检测中,将细胞裂解液提取的蛋白质电泳分离,再经抗体免疫反应,最后通过显色或荧光检测,定量或定性分析蛋白质表达情况。若蛋白质表达量较WT细胞显著降低或条带消失,表明发生了基因敲除。不过,因抗体特异性问题或敲除后蛋白残留问题,Western blot 并非完全适用于所有 KO 细胞敲除效率的评估。
- 通过对 KO 细胞与 WT 细胞同时进行蛋白质组学(质谱检测)前处理、数据采集和数据分析,分析目标基因的特征多肽缺失情况以及相关蛋白的变化(火山图),可了解靶基因的敲除情况以及因靶基因缺失引发的相关代谢通路变化。
(三)转录水平验证
利用实时荧光定量 PCR 法(RT-PCR)等技术检测 mRNA 的表达丰度。具体通过特异性引物和荧光标记的探针,经 RT-PCR 扩增技术对 mRNA 定量分析。需注意,mRNA 的下调是有效敲除的充分条件,而非必要条件,因此不能仅用 qPCR 检测目的基因的 mRNA 来单独验证是否敲除(特殊设计引物情况除外)。
详见:问题解读 I 为什么qPCR不完全适用于KO细胞的敲除效率评价?
(四)功能验证
根据靶点功能不同,基因敲除细胞还可进行特定功能验证(表型验证),通过观察细胞表型变化间接鉴定基因敲除效果。例如,观察敲除基因后生物体的生长状况、生理指标,细胞的增殖、迁移、侵袭、衰老等能力是否受影响,若基因敲除导致表型变化,则说明基因敲除成功影响了细胞生理功能。
四、实验技术与试剂在敲除验证中的关键作用
(一)实验设计与操作的精确性
从细胞裂解液的制备、蛋白质提取与电泳、抗体孵育等一系列实验操作,每个环节都对实验人员的专业技能和操作熟练度有极高要求。任何细微偏差都可能导致实验结果不准确。
(二)数据分析能力
面对测序结果、蛋白质免疫印迹、蛋白质谱数据、PCR 定量等验证数据,实验人员需具备强大的数据分析能力。能够运用各种专业软件和专业知识储备,判断基因敲除是否成功、是否存在脱靶效应、基因表达变化与预期是否相符等。例如,对 Sanger 测序结果的分析,需准确识别碱基的插入、缺失及移码突变;对蛋白质免疫印迹中抗原表位区域位置、抗体特异性、靶点特殊结构等等对结果的判读影响;对蛋白质组学数据的分析,要能从众多蛋白表达变化中筛选出与靶基因敲除相关的信息。
(三)稳定且高质量的试剂
高质量的试剂是生物实验成功的基础,稳定性高的试剂是验证实验得以重复的保证。在蛋白质检测中,抗体的特异性和亲和力对 Western blot 结果至关重要,优质抗体能准确识别目标蛋白,清晰呈现蛋白表达变化,而低质量抗体可能产生假阳性或假阴性结果,影响对敲除效率的分析判断。
总结
综上所述,细胞基因敲除验证既是一个对实验技术要求极高的领域,又与科研试剂行业的发展息息相关。实验技术人员需不断提升专业技能,精准把控实验各环节;试剂行业则应持续创新,提供更优质、高效的产品。双方协同发展,才能推动细胞基因敲除验证技术不断进步,为生命科学研究开辟更广阔的道路。粒曼团队为此推出的LM NGMSTM验证平台”: 粒曼“NGS二代测序+MS蛋白质谱”双重验证体系,从“根”上解决细胞基因敲除验证问题,完美绕开抗体行业问题,期待为该细胞基因敲除验证问题提供一种合理、有效的解决方案