推荐产品
技术资料/正文
小麦胚芽凝集素(WGA)修饰脂质体/脂质体纳米颗粒/胶束/聚合物纳米粒等:WGA赋能纳米载体,引领精准给药新浪潮
490 人阅读发布时间:2025-10-13 09:46
在精准医疗的时代,我们如何将高效的药物精确地送达体内的“隐秘角落”,如大脑、肠道黏膜或肿瘤深处?这曾是困扰科学界的一大难题。传统的纳米载体虽能保护药物,但往往在复杂的生物屏障前功亏一篑。
如今,一项源于自然的灵感——小麦胚芽凝集素(WGA),正为纳米药物递送领域带来革命性的突破。当WGA与脂质体、LNP、胶束、聚合物纳米粒等先进载体结合时,我们便获得了一把能够智能识别并穿越多重生物屏障的“生物钥匙”。
一、 自然界的灵感:什么是小麦胚芽凝集素(WGA)?
WGA是一种来源于小麦胚芽的蛋白质,它本身并非药物,而是一位卓越的“导航员”。其独特之处在于它能特异性识别并结合细胞表面的N-乙酰氨基葡萄糖和唾液酸——这些糖基化修饰分子广泛存在于肠道上皮细胞、血脑屏障内皮细胞以及多种肿瘤细胞的表面。
这种特异性的结合能力,使得WGA成为了修饰纳米载体的完美“向导”,赋予了载体四大核心优势:
增强的黏膜粘附性:延长载体在吸收部位(如肠道)的滞留时间,促进吸收。
促进细胞摄取:通过内吞作用,高效地将载体“送入”细胞内部。
开启细胞间通路:可暂时、可逆地打开细胞间的紧密连接,允许载体穿过屏障。
靶向性:天然倾向于富集在特定糖基化模式的病变细胞(如某些肿瘤细胞)周围。
二、 强强联合:WGA修饰的各类纳米载体平台
我们将这把“生物钥匙”与最前沿的纳米技术平台相结合,打造出新一代智能递送系统:
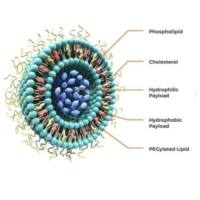
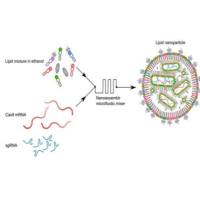
WGA修饰脂质体/LNP:作为最成熟的载体之一,脂质体和LNP(脂质纳米颗粒)以其优异的生物相容性和载药能力著称。WGA的修饰使其如虎添翼,不仅能高效包裹疏水/亲水药物、mRNA等,更能突破血脑屏障,为中枢神经系统疾病(如阿尔茨海默病、脑瘤)的治疗带来希望,或极大地提升口服药物的肠道吸收效率。
WGA修饰聚合物纳米粒:以PLGA、壳聚糖等生物可降解聚合物为材料,该载体可控释药、稳定性强。WGA的引导使其能够靶向肠道相关淋巴组织(GALT),为口服疫苗、免疫疗法提供了极具潜力的平台。
WGA修饰胶束:由两亲性共聚物自组装而成,擅长包裹疏水性药物。经WGA修饰后,这些微小的“运输船”能够穿透黏液层并锚定在肠壁细胞上,极大提高口服生物利用度,为难溶性药物的开发提供了新思路。
三、 应用前景:颠覆传统治疗的无限可能
1. 口服给药领域的革命
口服是最便捷的给药方式,但胃肠道屏障使许多大分子药物(如胰岛素、肽类、疫苗)无法有效吸收。WGA修饰的纳米载体能够粘附于肠壁,促进吸收,使“口服胰岛素”、“口服疫苗”从梦想照进现实。
2. 攻克“大脑堡垒”——中枢神经系统(CNS)给药
血脑屏障(BBB)保护了大脑,却也阻碍了98%以上的治疗药物入脑。WGA修饰的载体能识别BBB内皮细胞表面的特定糖配体,通过“特洛伊木马”机制将药物递送入脑,为脑肿瘤、神经退行性疾病的治疗开辟全新通道。
3. 精准靶向肿瘤治疗
许多肿瘤细胞表面会过度表达特定的糖基化蛋白。WGA修饰的纳米药物可以更高效地富集在肿瘤组织,实现主动靶向,增强疗效的同时降低全身毒副作用。
4. 黏膜疫苗与免疫调节
通过靶向肠道黏膜免疫系统,WGA修饰的载体可高效递送抗原,激发强大的黏膜免疫和全身免疫反应,为预防感染性疾病和癌症免疫治疗提供新策略。
四、 携手共进,引领未来
WGA修饰纳米载体技术,是生物学智慧与材料学技术的完美融合。它不仅仅是一项技术升级,更是为无数此前无法有效治疗的疾病提供了全新的解决方案。