推荐产品
技术资料/正文
甘露糖修饰脂质体(Liposome)和脂质纳米颗粒(LNP):靶向巨噬细胞、树突状细胞甘露糖受体
636 人阅读发布时间:2025-10-10 14:00
基于脂质体(Liposome)和脂质纳米颗粒(LNP)的递送技术已在制药领域引发革命。然而,实现递送系统的细胞特异性靶向仍是挑战。甘露糖(Mannose)受体(MR)高表达于巨噬细胞、树突状细胞等抗原呈递细胞(APCs)表面,为其靶向提供了绝佳途径。甘露糖修饰的脂质体/LNP技术,正成为增强免疫治疗、疫苗开发和抗炎疗法效力的关键策略。
一、核心技术机制:以“糖钥”启“免疫之锁”
甘露糖受体属于C型凝集素超家族,是内吞模式识别受体,在固有免疫和适应性免疫的桥梁细胞——巨噬细胞和树突状细胞上呈特异性高表达。这一生物学特性为精准药物递送提供了天然靶点。
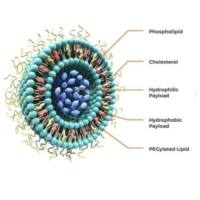
我们的技术通过在脂质体/LNP表面共价结合或锚定甘露糖衍生物,为其装上“智能导航系统”。
当载药颗粒进入体内后:
主动靶向:颗粒通过表面的甘露糖配体,特异性识别并结合APC表面的甘露糖受体。
高效内化:结合后触发受体介导的内存作用,将颗粒及其荷载药物高效内吞入细胞。
胞内释放:在胞内溶酶体等酸性环境中,脂质成分降解,实现药物在靶细胞胞质内的精准释放。
二、应用领域与巨大潜力
肿瘤免疫治疗:靶向递送免疫佐剂(如TLR激动剂)或抗原至树突状细胞,极大增强DC的抗原呈递能力,激活细胞毒性T细胞(CTL),对抗原低免疫原性肿瘤(如肝癌、胰腺癌)效果显著。
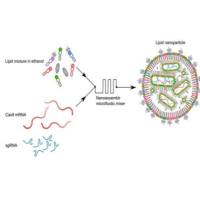
新型疫苗开发:作为mRNA疫苗或DNA疫苗的载体(甘露糖-LNP),可高效将抗原编码基因递送至APC,同时通过靶向作用本身激活免疫反应,实现“载体+佐剂”双重功能,大幅提升疫苗效力。
抗炎与抗感染治疗:靶向M2型巨噬细胞或炎症部位的巨噬细胞,递送抗炎药物(如糖皮质激素)或抗菌药物,用于治疗类风湿性关节炎、炎症性肠病(IBD)或胞内菌感染(如结核病),提高局部药物浓度,降低全身副作用。
罕见病治疗:用于靶向递送酶替代疗法中的功能性酶至巨噬细胞,治疗戈谢病等溶酶体贮积症。
三、我们的技术优势
高靶向效率:优化的甘露糖密度与空间构象,最大化受体结合率。
卓越的包封率:兼容亲水性、疏水性药物及核酸大分子(siRNA, mRNA, pDNA)。
良好的生物相容性:可降解脂质材料,安全性高。
可定制化平台:可根据客户需求,定制不同粒径、Zeta电位和载药类型的靶向颗粒。
甘露糖修饰的脂质体/LNP平台技术,是连接创新药物与关键免疫细胞的精准桥梁。它为解决药物递送的“最后一公里”问题提供了强大工具,尤其在免疫调控相关疾病领域拥有无可限量的应用前景。