推荐产品
技术资料/正文
精准导航:利用EGFR适配体修饰脂质体实现肿瘤高效靶向治疗
446 人阅读发布时间:2025-10-10 13:59
在肿瘤治疗的漫长征程中,如何实现药物在病灶部位的高效富集,同时降低对正常组织的毒副作用,一直是临床面临的核心挑战。表皮生长因子受体(EGFR)作为在多种上皮源性肿瘤(如非小细胞肺癌、结直肠癌、头颈部鳞癌等)中过度表达的关键靶点,是精准医疗的理想突破口。如今,一种革命性的药物递送平台——EGFR适配体修饰的脂质体(Aptamer-Liposome),它将为您的临床研究与治疗策略带来全新可能。
传统疗法的局限:
• 脱靶效应: 化疗药物广泛分布,系统性毒性大。
• 耐药性: 肿瘤细胞易产生耐药,导致治疗失败。
• 生物屏障: 药物难以有效穿透至肿瘤组织内部。
我们的解决方案:EGFR适配体修饰脂质体
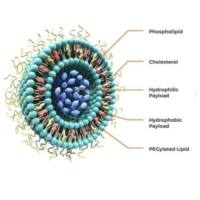
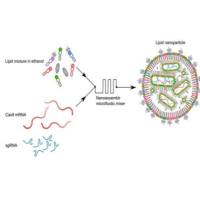
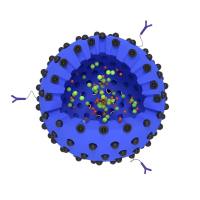
脂质体作为经典的纳米药物载体,具有良好的生物相容性和载药能力。我们通过前沿的分子工程技术,将特异性识别EGFR的核酸适配体(Aptamer)精准修饰于脂质体表面,打造出“生物导弹”般的智能递送系统。
其核心优势在于:
精准靶向,高效富集: 适配体像“智能导航头”,主动识别并牢固结合肿瘤细胞表面的EGFR,引导脂质体在病灶部位大量聚集,显著提升局部药物浓度。
增强内化,克服耐药: 结合后通过受体介导的内吞作用,将所载药物(如化疗药、基因药物等)高效送入细胞内部,绕过外排泵机制,有效逆转耐药。
减毒增效,提升窗口: 药物被“封印”在脂质体中直至抵达靶点,大幅减少在血液循环中的暴露,显著降低全身性毒副作用,提高治疗指数。
灵活载药,应用广阔: 脂质体亲水内核和疏水双分子层可同时负载不同性质的药物(如阿霉素、紫杉醇、siRNA等),实现联合治疗与个性化用药。
应用前景与临床价值:
• 化疗增效: 装载化疗药物,用于EGFR高表达肿瘤的一线及耐药后治疗。
• 基因沉默: 递送靶向致癌基因的siRNA或miRNA,实现精准基因治疗。
• 联合免疫: 装载免疫佐剂或调控因子,重塑肿瘤微环境,与免疫疗法协同。
EGFR适配体修饰脂质体平台,不仅是技术的革新,更是治疗理念的进化。它为我们提供了攻克实体瘤的又一利器,有望真正实现“指哪打哪”的精准医疗愿景。我们诚挚邀请各位临床专家与研究同仁共同探索这一平台的无限潜力,为患者带来更长、更优质的生存获益。