普瑞麦迪(北京)实验室技术有限公司代理商
7 年
手机商铺
- NaN
- 0.20000000000000018
- 0.20000000000000018
- 1.2000000000000002
- 0.20000000000000018
技术资料/正文
从二维到三维:3D 生物打印技术在科研中的原理、应用与未来
63 人阅读发布时间:2026-02-12 13:49
随着生命科学研究迈向更高维度的模型,传统二维细胞培养体系的局限性越来越明显。细胞在二维平面中无法真实模拟体内复杂的三维微环境,这在药物筛选、疾病机理研究等领域中造成了显著的偏差。为此,3D 生物打印(3D Bioprinting)应运而生,成为构建体外三维细胞/组织模型的重要技术。
什么是 3D 生物打印?
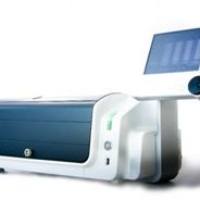
3D 生物打印是一种基于增材制造的技术,它按照预设的数字模型,在空间上逐层构建由生物墨水组成的三维组织结构。这些生物墨水通常由活细胞与生物相容性材料(如水凝胶)组成,打印后的结构可进行培养并保持细胞活性。3D 生物打印的核心在于精确控制细胞与支架的空间分布,从而模拟体内组织特征。

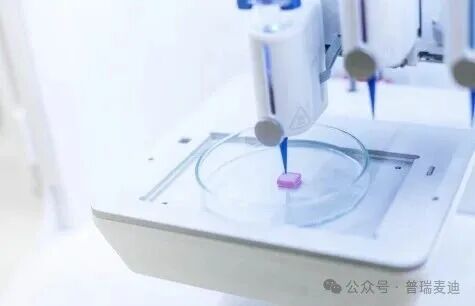
技术层面上,3D 生物打印既不同于传统工业 3D 打印,也不同于简单的三维细胞培养。它要求材料、打印过程和后续培养严格兼顾生物活性与组织功能。其研究价值在于,打印出的三维结构可更真实地反映体内环境,有助于机制探索与药物评价。
核心技术路径
目前生物打印技术主要包括以下几类:
-
挤出式生物打印(Extrusion-based)
-
光固化生物打印(DLP/SLA)
使用光照投影数字图案固化光敏生物墨水层,从而构建精细的三维结构,在微结构构建与分辨率上具有优势。
-
微滴/喷墨式生物打印(Inkjet/Microdroplet)
通过控制液滴沉积,将低粘度 bioink 定点输送,适合高通量低耗体模型构建。
这些技术路径各自具有研究适用性:例如,挤出式更适合大体积的组织模型构建,而光固化式更适合高分辨率、细微结构设计(如微通道、毛细管网状结构)。
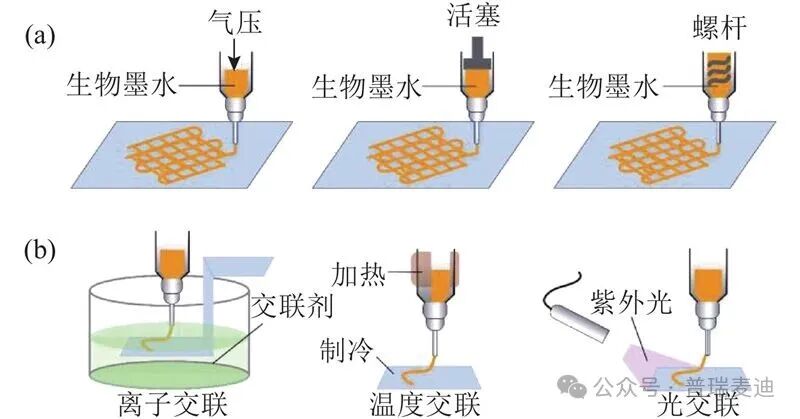
图示:挤出式3D生物打印原理
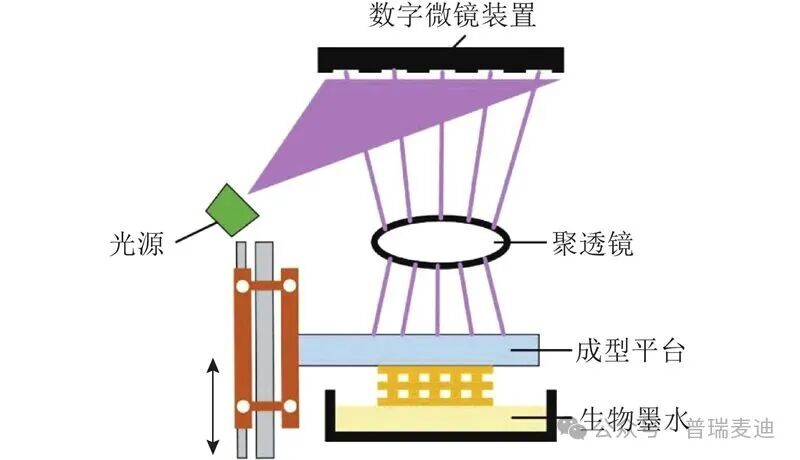
图示:光固化式3D生物打印原理
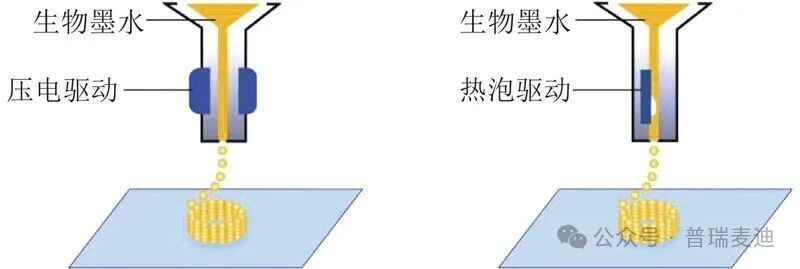
图注:喷墨式3D生物打印原理
科研典型应用方向
3D 生物打印正在推动多个生命科学领域的研究进展:
-
三维细胞培养与组织模型构建
这些模型相比二维体系能更好地表达体内细胞行为。
-
药物筛选与毒性评估
在药代动力学和药效评估中,三维组织模型显示出更高的预测一致性与生理相关性。
-
疾病模型与机制研究
例如肿瘤模型、纤维化模型等,为机制和治疗策略提供了高效平台。
-
再生医学与组织工程基础研究
支持逐步探索可植入组织结构、干细胞支撑环境等。

图注:3D生物打印人类角膜基质及基座支架装置
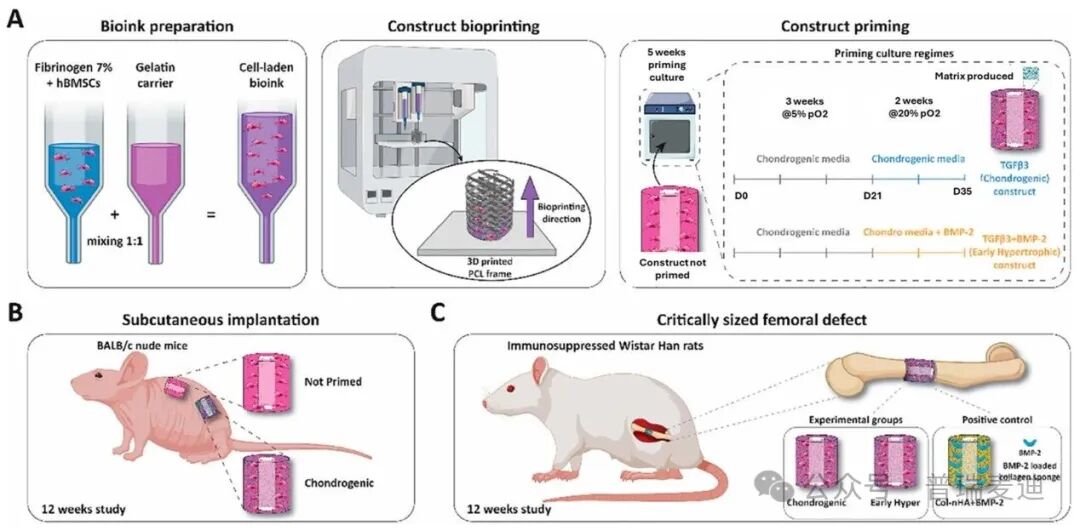
图注:用于骨科的软骨模板生物打印示意图
设备与平台示例(以 CELLINK 设备为例)
在科研实践中,基于不同技术路径的生物打印平台正逐渐形成体系化解决方案:
1 挤出式 3D 生物打印平台:BIO X 系列
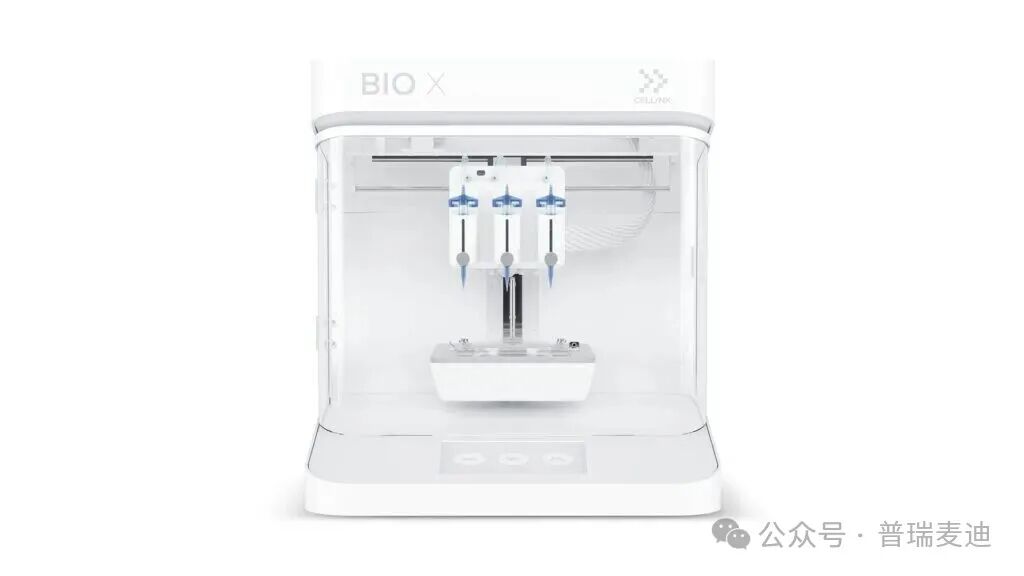

图注:BIO X 与 BIO X6 生物打印系统——CELLINK 挤出式打印平台,支持多打印头和不同材料体系。
挤出式系统具有以下特点:
-
多打印头设计,提高多材料/多细胞类型打印能力。
-
温控打印床和封闭清洁室设计,提升生物打印的稳定性与实验可重复性。
-
清洁室 HEPA 过滤与无菌环境,有助于长时间培养与后续实验操作。
其中 BIO X6 采用多达 6 个智能打印头,可在同一过程构建更复杂的多材料/多细胞结构,有助于更接近体内结构的构建。
2 光固化技术平台:LUMEN X / Bionova X


图注:LUMEN X / Bionova X 光固化生物打印平台——用于高精细光固化打印,适合微结构模型的构建。
光固化系统通过数字光图案同时固化整个层面的生物墨水,可实现更高打印分辨率和更精细的微结构设计。
科研方法与实验工艺
在结构构建之外,3D 生物打印的大量科研工作依赖于:
-
生物墨水设计与表征:流变学特性、印迹力学性质需要优化以保持打印精度与细胞生存环境。
-
打印后培养策略:打印构建完成后的培养环境设计,如生物反应器、动态培养体系等,对组织成熟与功能表达至关重要。
-
成像与分析方法:包括显微成像、免疫荧光分析、功能测试等,以评估模型的生理相关性。
当前挑战与研究前沿
尽管应用范围正在扩大,3D 生物打印在科研中仍面临挑战:
-
如何在打印过程中降低细胞剪切应力并提高生存率。
-
生物墨水与功能材料的可控性与生物响应需要深入理解与优化。
-
打印后培养体系与体外环境的集成仍需创新实验设计。
结论:面向研究的三维生物构建平台
3D 生物打印作为一种集成了细胞生物学、材料科学和工程制造的交叉技术,为构建真实生理相关模型提供了工程手段。其核心价值在于通过精确空间控制与功能化材料配伍,使研究者能够更接近体内微环境,并为药物筛选、疾病机制研究与组织工程提供有效实验工具。
参考文献
1.He Y , Gao Q , Liu A ,et al.3D bioprinting: from structure to function[J].Journal of Zhejiang University(Engineering Science), 2019.DOI:10.3785/J.ISSN.1008-973X.2019.03.001.
2.Kutlehria, S.; Dinh, T.C.; Bagde, A.; Patel, N.; Gebeyehu, A.; Singh, M. High-throughput 3D bioprinting of corneal stromal equivalents. J. Biomed. Mater. Res. B Appl. Biomater. 2020, 108, 2981–2994.DOI: 10.1002/jbm.b.34628
3.Pitacco, P.; Sadowska, J.M.; O’Brien, F.J.; Kelly, D.J. 3D bioprinting of cartilaginous templates for large bone defect healing. Acta Biomater. 2023, 156, 61–74.DOI: 10.1016/j.actbio.2022.07.037