普瑞麦迪(北京)实验室技术有限公司代理商
7 年
手机商铺
- NaN
- 0.20000000000000018
- 0.20000000000000018
- 1.2000000000000002
- 0.20000000000000018
技术资料/正文
【网络层面看AD】大规模电生理如何解释海马环路失调——3Brain MEA 相关文献分享
68 人阅读发布时间:2026-02-12 13:47
在阿尔兹海默病(Alzheimer’s disease AD)研究中,我们已经非常熟悉Aβ、tau和神经元死亡等分子与细胞病理。但一个越来越清晰的事实是:在明显结构性损伤出现之前,神经网络本身已经“不同步了”。
如果记忆不是单个神经元的属性,而是网络协同活动的结果,那么,AD是否首先是一种“网络疾病”?
本文基于2025年IEEE EMBC会议发表的一项研究,系统解读研究者是如何利用高密度微电极阵列(HD-MEA),在完整海马环路尺度上刻画AD模型中的网络失调,并探索天然化合物对网络功能的调控潜力。
一 为什么必须从“网络层面”重新理解AD?
长期以来,AD的研究范式主要聚焦于:
-
Aβ斑块沉积
-
tau蛋白异常磷酸化
-
神经元和突出丢失
但在临床上,一个长期存在的矛盾是:分子病理负荷≠认知损伤程度。
越来越多证据表明,在神经元大规模死亡之前,海马-皮层(HC)环路的功能协同已经被破坏,直接影响记忆编码、巩固和提取。
-
θ / γ振荡
-
Sharp-wave ripple(SWR)
被视为连接分子病理与认知功能的重要“功能中间层”。
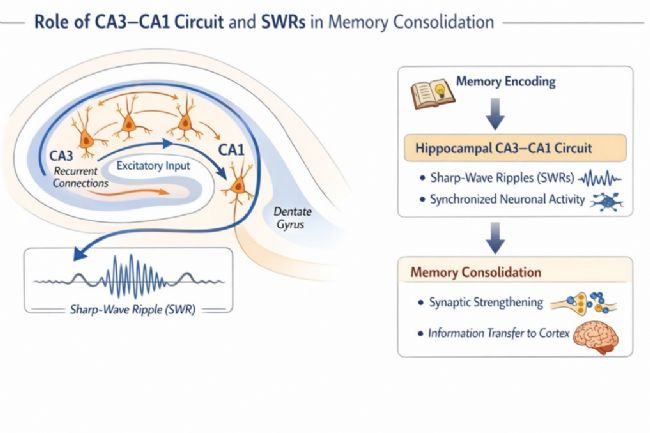
图 1 海马 CA3–CA1 回路 + SWR 在记忆巩固中的作用示意图
二 技术关键:HD-MEA为什么适合研究“网络失调”?
要真正回答“网络是否失调”,技术平台至关重要。
传统单电极或低通道MEA面临三大限制:
-
空间覆盖不足,无法记录完整海马回路;
-
难以同时解析LFP、SWR、MUA等多尺度信号;
-
对网络同步性和传播模式不敏感。
本研究采用CMOS工艺高密度微电极阵列(HD-MEA),其核心优势包括:
01 空间尺度
-
单芯片4096个电极
-
42μm电极间距
-
覆盖7mm2,可完整覆盖DG-CA3-CA1-EC
02 信号尺度
-
1Hz-5kHz带宽
-
同时捕捉LFP、SWR与MUA
03 网络分析友好
-
支持事件检测、空间分布、频谱和时间动力学分析
三 模型设计:APPNL vs. APPNL-G-F,有何不同?
研究选用了两种knock-in AD小鼠模型
-
APPNL:病理相对温和
-
APPNL-G-F:Aβ与tau相关病理更重,更接近进展期AD
在36周龄小鼠的急性海马切片中,通过4-AP诱导自发网络活动,对两种模型进行系统比较。
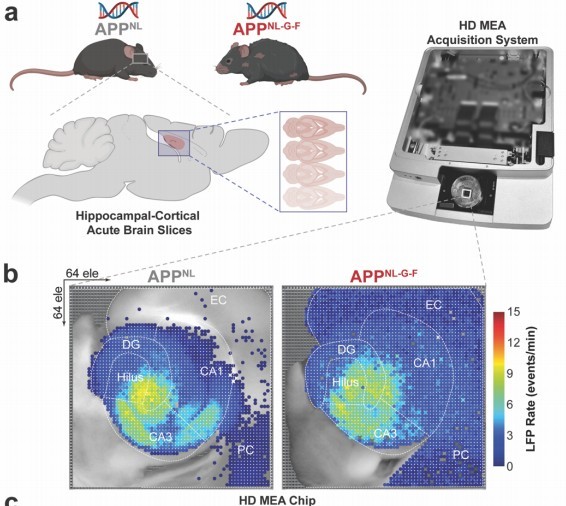
图 2 HD-MEA + 海马切片示意(a) 描述了整个实验系统:从小鼠脑组织取样 → 制备急性脑切片 → 放置在 HD-MEA 芯片上进行记录。(b) 展示了两个基因型(APPNL 和 APPNL-GF)切片中 LFP 活动的空间分布热图,颜色代表 LFP 频率(events/min),可见不同区域(如 CA1、DG、EC)的活动差异。
四 核心结果一:高频网络活动最先“失语”
01 LFP:低频活动基本保留
两种模型在LFP事件频率上差异不显著,说明:基础群体活动尚未完全崩溃。
02 SWR与MUA:显著受损
相比APPNL,APPNL-G-F表现出:
-
SWR事件频率显著下降
-
MUA放电水平降低
-
SWR持续时间缩短、空间分布收缩(尤以CA3-CA1为甚)
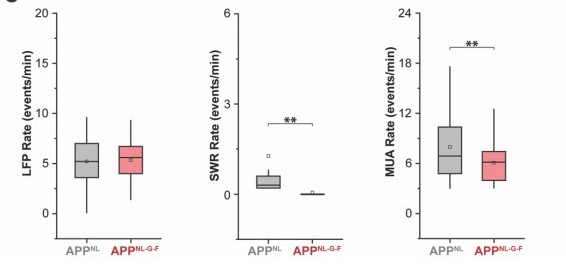
图 3 LFP / SWR / MUA 事件率比较。左图:LFP 率(整体神经活动),中图:SWR 率(尖波涟漪事件频率),右图:MUA 率(多单位放电活动)。显示 APPNL-GF 在 SWR 方面显著降低( 表示 p < 0.01),而其他指标无明显差异。
这表明:AD首先破坏的不是“有没有放电”,而是“能不能精确协同”。
五 为什么SWR是极具价值的网络级指标?
SWR的产生依赖于:
-
CA3递归兴奋网络
-
精确的兴奋/抑制(E/I)平衡
-
亚毫秒级时间同步
因此,SWR的频率、持续时间和空间传播,都是网络完整性的直接读出。
本研究中SWR的多维度受损,提示AD的核心问题在于:网络协调能力的系统性下降,而非简单的神经元沉默。
六 干预探索:藏红花能“修复”网络吗?
研究进一步测试了天然化合物藏红花(saffron)对网络活动的影响。
01 剂量依赖的功能恢复
在APPNL-G-F切片中,25μg/ml藏红花即可:
-
显著提高SWR与MUA频率
-
扩大参与SWR的活跃电极数量(约2.75倍)
-
恢复CA3-CA1网络协同
而在APPNL中几乎无效,说明其作用偏向病理状态下的网络恢复
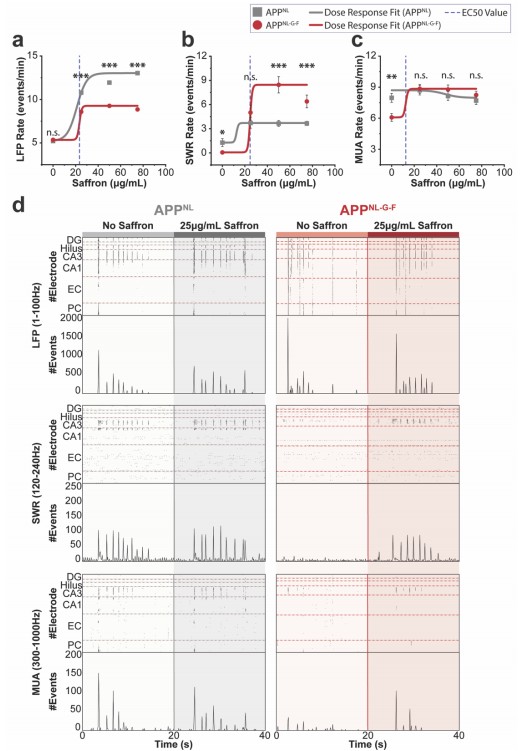
图 4 剂量-反应关系。(a), (b), (c):剂量-反应曲线(Dose-response curves),显示不同频率带的神经活动随藏红花浓度变化的趋势。(d):原始数据的“raster plots”(事件时间序列图),展示0 μg/mL 和 25 μg/mL 藏红花处理下各脑区的神经活动动态。
02 平台效应:网络恢复存在上限
更高剂量(50-75μg/ml)并未带来额外增强,提示:
-
网络可塑性存在结构性限制
-
干预存在“最佳窗口”
七 方法学延申:HD-MEA作为“网络药效学”平台
从方法论角度看,本研究的意义不仅在于AD结论本身,更在于展示了一种可推广的研究范式:
-
不只问“分子是否改变”,而是问网络是否恢复协同;
-
用SWR、MUA等网络指标评估药物或干预效果;
-
适用于AD、癫痫、精神分裂症、脑损伤等多种疾病模型。
以3Brain的HD-MEA为代表的高密度电生理平台,正在成为连接分子机制、环路功能与行为表型的重要工具,尤其适合:
-
神经退行性疾病网络表型研究
-
神经保护/调控策略的功能筛选
八 结论与展望
这项研究清晰表明:
-
AD是一种网络层面的疾病;
-
高频振荡(尤其是SWR)是高度敏感的功能指标;
-
网络功能的恢复并非线性、无限,而受制于结构完整性;
-
HD-MEA为“网络精准干预”提供了轻量化工具。
当我们把视角从“单个分子”拉升到“整个网络”,阿尔兹海默病呈现出一种全新的面貌。
未来,真正有效的干预,或许并不只是减少病理负担,而是让神经网络重新学会协同工作。
参考文献
B. A. Emery, S. Khanzada, X. Hu, M. A. Maggi, S. Bisti and H. Amin, "Network-Level Characterization of Hippocampal Disruptions in Alzheimer’s Disease Using Large-Scale Electrophysiology," 2025 47th Annual International Conference of the IEEE Engineering in Medicine and Biology Society (EMBC), Copenhagen, Denmark, 2025, pp. 1-4, doi: 10.1109/EMBC58623.2025.11253272.