| 高血压(hypertension)病是一种常见的慢性病,以体循环动脉血压增高为主要特征,伴有心、脑、肾等器官的功能或器质性损害的临床综合征。它是心脑血管病发病和死亡最重要的因素,约半数心脑血管病相关死亡,由高血压所致。
临床上常用的抗高血压药,在降压及改善症状方面尚存在许多不足。高血压的确切病因及发病机制尚存在许多未知,亟须加强对高血压病因及发病机制的研究,从而开发出更有效的治疗药物。
其中实验研究离不开高血压动物模型,好的动物模型能够较好地模拟疾病状态。为了更好地研究高血压发病机制及治疗方法,高血压疾病相关研究者建立了多种高血压实验动物模型,具体分为两大类,分别为基因相关的高血压病动物模型(分为遗传性高血压模型和基因工程型高血压动物模型)和非基因相关的高血压病动物模型。
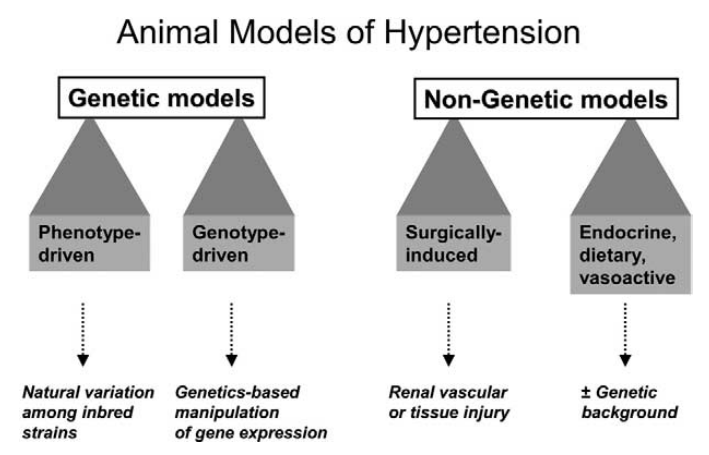
(DOI: 10.1016/j.lab.2005.05.005)
每种模型各有各的特点。模型选择是实验成功的第一步,要求研究者明白每种动物模型及自身实验的特点,再结合实验条件综合考虑选取。本文就一些经典、常用的高血压动物模型的制备方法及特点进行总结,以供参考。
应用于高血压研究的实验动物可以选择猪、猴、羊、犬和大鼠等,其中以犬和大鼠造模居多。兔因血压不够稳定,一般不用。
一、遗传性模型 (1)自发性高血压大鼠(SHR)模型
通过 Wistar 大鼠同系近系多代繁殖培育成功。饲养过程中无需给予特殊饲料即可发生高血压病。该大鼠随着月龄的增加,会出现明显的高血压病变和由此引发的各种临床症状。6-8 周为高血压发病期,末梢动脉变得狭窄、弯曲,心脏渐渐肥大。
该模型具有病程较短,血压高且稳定,病态表现与人原发性高血压的病态表现极为相似等优点。因此,SHR 大鼠是目前国际公认的最接近于人类原发性高血压的动物模型,也是目前应用最广泛的模型,广泛应用于高血压的发病机制、预防、治疗和诊断等诸多方面的研究。
然而,该模型对饲养条件有一定要求,且培育周期较长,价格较普通 SD 大鼠稍高,遗传育种麻烦,易变种、断种,大量使用尚存在困难。
(2)盐敏感性高血压遗传大鼠(Dahl SS 大鼠)
Dahl 盐敏感 (Dahl salt sensitive,Dahl-SS) 大鼠作为研究盐敏感高血压的经典动物模型,具备血压的盐敏感性、高脂血症、胰岛素抵抗、肾功能衰竭、尿蛋白分泌增加以及低血浆肾素活性等和人类盐敏感高血压患者相类似的病理生理学特征,并能够稳定遗传。
作为独特的盐敏感性高血压遗传大鼠,它是揭示盐敏感性高血压发病机制及治疗的经典模型,在一些影响较大的实验研究中发挥重要作用。但动物饲养条件高,价格贵,遗传育种麻烦。
二、诱导性模型
除遗传性高血压动物模型较能模拟人类高血压病的自然过程外,还有其它各类实验性高血压动物模型,大多要经过一定的手术、药物或其他附加因素处理。
(1)手术诱导
1. 肾动脉狭窄性高血压模型
肾血管性高血压是由于缺血导致肾素-血管紧张素-醛固酮系统的激活而产生的,而肾素-血管紧张素-醛固酮系统的激活引发高血压的发病机制中已被公认。因此,动物肾动脉狭窄,能非常相似地复制出高血压模型。
狭窄肾动脉可造成肾脏缺血,引起肾小球旁器分泌肾素增多。肾素能使血管紧张素原变为血管紧张素 I,后者又经转换酶的作用变为能使血管收缩的血管紧张素 II,最终加重了全身小动脉的痉挛,形成持久、恒定的高血压。
1934 年 Goldblatt 证实狭窄犬肾动脉可产生持续性高血压,为高血压的实验研究开辟了一条途径。
肾动脉狭窄性高血压模型,为一侧或两侧肾动脉主干或分支狭窄、阻塞使肾血管流量减少,导致肾脏内肾素形成,进而增高血中血管紧张素 II 含量,使血压升高,为最常见的继发性高血压。
两 (双) 肾一夹型(2K1C)
两肾一夹模型即保留双侧肾脏,狭窄单侧肾动脉。健康雄性 SD 大鼠,CHN₂NaO₃ 麻醉,在无菌操作下经腹部正中切口入腹腔,分离并暴露一侧肾动脉,利用无菌银夹或银环套在肾动脉上造成肾动脉狭窄。
该模型具有造模简单、成功率高、同一性高等优点,且可长期稳定维持高血压,与人类高血压病理过程具有可比性,是国际上最常用的经典的高血压动物模型(接近于 SHR),是目前筛选降压药物中选用较多的一种模型。
双肾双夹型(2K2C)
选用健康雄性 SD 大鼠,CHN₂NaO₃ 麻醉,在无菌操作下经腹正中切口入腹腔,依次钝性分离双侧肾动脉,用无菌银夹分别钳夹双侧肾动脉起始部。
该模型自发性脑卒中发生率高,高血压病发生过程与人类高血压病的发生发展过程相似,广泛应用于高血压心、脑、肾等并发症防治方面的研究。
单肾单夹型(1K1C)
单肾单夹型即切除右肾,缩窄左肾动脉。该模型由于成功率较低,血压不能持续上升,限制了其使用范围,目前已较少使用。
肾动脉狭窄型模型由于复制简便、动物来源充足,广泛应用于人类高血压及其并发症的研究,亦是目前在降压药物研究中选用较多的一种模型。
2. 腹主动脉缩窄型高血压模型
适用于大型动物犬、兔。多采用无菌丝线于两肾动脉之间环扎腹主动脉,一般使管径减小约 50%,致外周阻力增大,血压升高。该模型适用于高血压的心血管损害相关研究,然而动物死亡率较高、手术难度大,一定程度上限制了其广泛应用。
3. 肾外包扎性高血压模型
肾外异物包扎,可致肾周围炎,在肾外形成一层纤维素鞘膜,压迫肾实质造成肾组织缺血,使肾素形成增加,血压上升。
造模方法:利用双层乳胶薄膜对一侧肾脏进行包扎处理,对另一侧肾脏进行切除处理。
大鼠麻醉后,无菌打开腹腔暴露左侧肾脏,小心将肾脏与周围剥离,将双层乳胶薄膜剪成 X 形,绕肾门将肾脏交叉包扎,然后在相对侧切开,暴露右肾,分离后摘除,关闭腹腔并缝合伤口。术后 20 天,有 70% 以上的大鼠出现高血压。
模型验证
(1)血压检测:对高血压动物模型需建立一种可靠的测量血压的方法,并且该方法本身不会导致血压的升高。
在没有合适测量方法的情况下,化合物降低血压的能力可能会被测量方法本身引起的血压升高掩盖,这就需要 1-2 周的训练期来训练动物适应血压表的应用。
(2)生化检测:尿酸,尿素氮及肌酐
(3)肾脏形态检测:手术成功后,结扎侧肾脏会萎缩,对侧肾脏扩大。
(2)药物诱导该模型易造成一定程度的肾损伤及其他副作用,适用于高血压中血管和肾脏功能研究。
1. 血管紧张素Ⅱ(AngⅡ)诱导
该模型的制备多采用渗透泵皮下注射法,该模型复制方法无创、简单,血压升高持续稳定,为非常有应用前景和值得推广的模型之一,主要在肾素、血管紧张素和氧化应激等研究中应用广泛。
2.N-硝基-L-精氨酸甲酯(L-NAME)诱导
研究发现,血管内皮功能异常是高血压的诱发因素之一,而一氧化氮(NO)是促进内皮功能的一种活性物质,NO 升高时血压下降。NO 合成酶抑制剂 L-NAME 可削弱一氧化氮的舒血管作用,介导升压反应。
该模型血管内皮损害较心肌损害突出,血压能稳定持续升高,复制方法无创、简单,特别适用于一氧化氮系统对高血压病的影响及心血管系统损害等相关研究。
3. 醋酸去氧皮质酮(DOCA)诱导
醋酸去氧皮质酮可抑制肾素-血管紧张素的发生从而介导血压升高。通过在皮下注射 DOCA 的基础上用盐灌胃可诱导高血压。
该模型制备简便、高血压稳定,除了适用于水钠代谢相关研究外,也适用于肾素血管紧张素系统(renin-angiotensin-aldosterone system,RAS)以外的其他可能参与高血压发病的病理机制研究,如高容量型高血压的免疫炎症损伤机制相关研究。
(3)饮食诱导
在饮食方面,高钠(高盐)饮食是其中一个重要的因素,因此也是研究高血压模型的重要方向。
此外,多种营养素缺乏,如缺钙、缺镁、缺精氨酸、低蛋白质,以及营养相关性疾病(肥胖)等均是高血压的诱因。
此种动物模型的建立对于现临床常见饮食不健康的年轻人有很大意义,对于青年高血压病患者的发病机制、治疗及预后有着不可或缺的作用。但造模时间较长,血压升高不甚理想,停止特殊饮食后,血压不能维持。
(4)环境诱导
该模型多应用于急性高血压实验,采用各种刺激(闪光灯、噪音、疼痛、冷 / 热等)造成动物高度紧张,交感神经、RAS 激活致全身细小动脉收缩,血压升高。
造模实验处理周期较长,与人的高血压表型相似,适用于降压药的筛选。然而其血压稳定性、可控性不及经典模型,除应用于高血压神经精神相关性研究外,较少用于其他方面的研究。

(DOI: 10.1016/j.lab.2005.05.005)
三、基因工程型
基因工程高血压病动物模型分为转基因动物模型和基因敲除动物模型。
前者是将外源基因整合到基因组中过分表达造成高血压病(如 AGT-REN 双转基因高血压病小鼠、多巴胺 D5F173L 突变基因及 D5 正常基因转基因小鼠、A142V 转基因小鼠)。
后者将相关基因定向敲除造成高血压病(如小鼠肾特异性敲除 Nedd4-2 或 ACE,大鼠肾特异性敲除 Hsd11b2)。
该类模型能够从基因层面阐释高血压的发病机制,阐述目的基因的作用及其与高血压的关系,发现靶向治疗基因,有助于建立人群药物遗传学基因档案,在基因层面明确个体对降压药物的敏感性,提高降压药物疗效奠定基础等。
然而该模型制备技术要求高,且无论现有的基因工程高血压病模型造模多么完美,仍旧无法完全复刻多基因遗传的人类高血压病。

(DOI: 10.1016/j.lab.2005.05.005)
四、特殊模型 (1)妊娠高血压综合征模型
多选取成年 Wistar 孕 2-3 周雌鼠,造模方法有多种,如超低剂量内毒素(1.0μg/kg)鼠尾静脉注射法、L-NAME 皮下注射法、子宫动脉缩窄法等,适用于妊娠高血压发病机制的研究。
(2)绝经期高血压模型
绝经期高血压主要因年老造成血管硬化及植物神经功能紊乱、精神焦虑紧张等引起。目前有关绝经期高血压的研究主要集中在临床观察,动物实验较少。
参考文献:
【1】Animal models of hypertension: an overview,DOI: 10.1016/j.lab.2005.05.005
【2】高血压与颈性高血压动物模型研究进展,谢思维等,2022
【3】温欣 , 张琪 . 高血压病实验动物模型的应用概况与评价 [J]. 中国医药导报 , 2021, 18(17):4.
【4】杨昌振 , 张雯斐 , 陈丹阳 , 等 . 非手术性高血压大鼠模型建立的研究进展与比较 [J]. 中国循证心血管医学杂志 , 2019, 11(1):4.
【5】黄冬梅 (综述), 郑文武 , 李秀英 (审校). 实验性高血压大鼠模型制备方法及应用概述 [J]. 现代医药卫生 , 2017, 33(3):3.
【6】李建橡 , 马晓聪 , 邓学秋 , 等 . 高血压不同种属动物模型的研究近况 [J]. 广西中医药大学学报 , 2016, 19(3):4.
【7】Animal Models of Hypertension: A Scientific Statement From the American Heart Association,DOI: 10.1161/HYP.000000000000009
【8】Animal Models in Cardiovascular Research: Hypertension and Atherosclerosis,DOI: 10.1155/2015/528757
|