| 细胞增殖是肿瘤研究的必备实验之一。最简单直接的检测细胞增殖的方法就是在不同时间点进行细胞计数,但是在96孔板甚至384孔板的实验设置下,这无疑是难以操作的。于是,研究者们更倾向于用间接方法研究细胞增殖,比如基于线粒体内脱氢酶还原能力的MTT, MTS, CCK-8法,还有基于胞内ATP水平的CellTiter-Glo, ATPlite等。原理上,这些方法都是以细胞的代谢水平来代表细胞数量。但是大家有没有怀疑过这些间接方法真能准确反映细胞的生长状态吗? 美国Genentech公司的科学家对这一问题进行了深入的研究。在2013年发表的一篇文献中,作者选择了两种最常见的检测细胞增殖的方法 – MTS和 CellTiter-Glo和直接细胞计数法进行比较,得到了意想不到的结果。
Chan G K Y, Kleinheinz T L, Peterson D, et al. A simple high-content cell cycle assay reveals frequent discrepancies between cell number and ATP and MTS proliferation assays[J]. PloS one, 2013, 8(5): e63583.
如上图所示,HT29细胞被6种不同药物处理48小时后用不同方法对细胞增殖进行了分析。从生长曲线来看,这三种方法得到的结果之间有不小的差异。比如Etoposide( 细胞周期特异性的抗肿瘤药),虽然最高与最低剂量得到的杀伤效率分别相同,但细胞计数与另两种方法的曲线趋势完全不同,所得IC50也小得多。又比如Gemcitabine(DNA合成抑制剂), 细胞计数所测得的最高剂量杀伤效率比另两种方法测得的要高得多。总体来说,与细胞计数相比较时,MTS和CellTiter-Glo会不同程度地低估药物杀伤效率。 
在这篇文献发表之后,很多期刊的编辑都要求,对于MTS类似原理做出的细胞增殖数据,需要用其他原理的方法进行佐证。小伙伴们的烦恼随之而来:今后如何再愉快地做细胞增殖实验呢?手动数细胞实在太痛苦了。 美国Nexcelom公司的一款名为Celigo的神器了解一下: 
● 全孔成像,图片清晰,适用于6-1536孔板 ● 软件可沿轮廓勾勒识别贴壁和悬浮细胞 ● 原位检测,不需染色,不需任何试剂,无毒无侵扰 ● 高速成像和分析,完成一块96孔板仅需不到5分钟 
● 一块板即可完成所有时间点的追踪和检测 ● 分析全孔细胞,也可选择分析局部视野 ● 可记录查看每个时间点任一视野的细胞形态 ● 针对不同的细胞类型可选择不同的分析方法: ▸直接细胞计数法,适合于轮廓清晰的细胞类型 ▸融合率检测法,适合于成片生长,轮廓不清晰的细胞类型 ● 软件可生成每孔细胞生长曲线 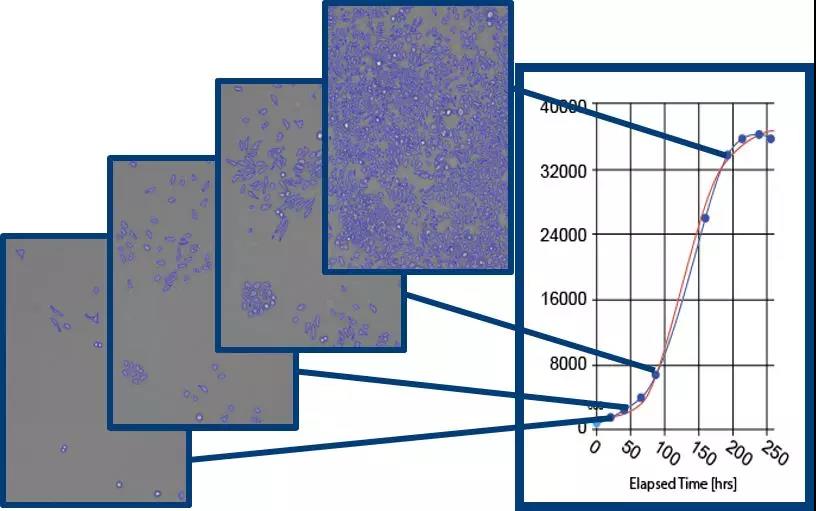
分析方法1:直接细胞计数 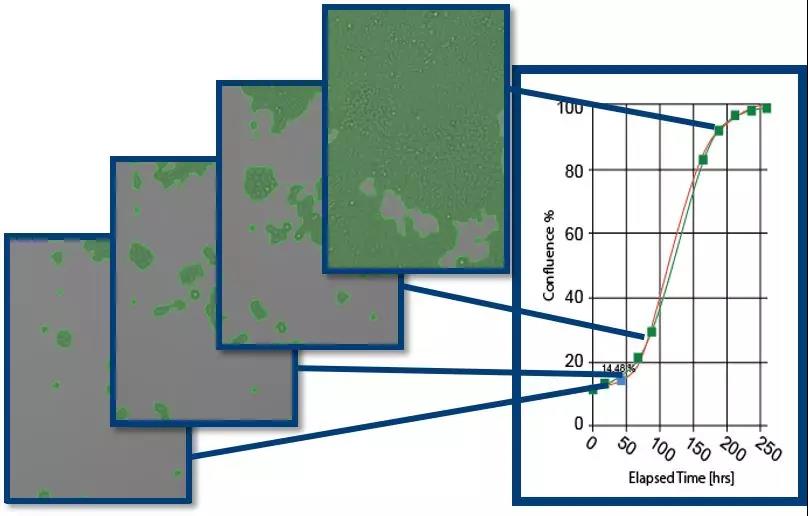
分析方法2:细胞融合率检测 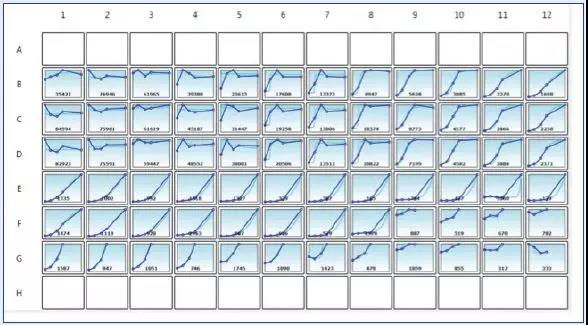
96孔板细胞生长曲线 
384孔板融合率填充图 无标记细胞增殖只用到了 Celigo 的明场通道,也仅仅是该神器众多应用中最基本的一个。除了明场,Celigo 还配置有 4 个荧光通道(蓝、绿、红和远红),为实验的设计提供了无限可能。 目前 Nexcelom 已开发出在细胞健康、肿瘤免疫、病毒学、细胞株构建、干细胞、3D 肿瘤球检测等九大领域的数十种 Celigo 应用。感兴趣的小伙伴可与我们的应用科学家联系,了解更多信息~
|