【关键词】外泌体、角质形成细胞靶向脂质纳米颗粒、巨噬细胞、组织纳米转染、伤口愈合

【摘要】细胞间通过外泌体携带miRNA进行相互作用已经成为伤口愈合的关键机制,而外泌体主要通过hnRNPA2B1蛋白的SUMO化选择性包装miRNA。本研究团队阐明了角质形成细胞-巨噬细胞互作对组织修复的重要性,从伤口边缘组织分离出角质形成细胞来源的外泌体并进行标记(Exok-GFP),结果表明巨噬细胞选择性吞噬这些外泌体。进一步构建siRNA-hnRNPA2B1功能化脂质纳米粒子(TLNPk)来抑制外泌体中miRNA的封装,结果表明干扰组中的肉芽组织促炎巨噬细胞增多,屏障功能受损,连接蛋白也相应减少,因此证实了角质形成细胞来源的外泌体中miRNA对于上皮屏障的修复有重要作用。
【前言】皮肤损伤后细胞间的通讯促进伤口的愈合,而这种细胞间通讯通常是由细胞外囊泡的旁分泌介导,这些囊泡直径在50-1000nm之间,起源于质膜,可分为微囊泡、外泌体、微粒和外囊泡。其中外泌体所携带的miRNA等介导了多种细胞间通讯,SUMO化的hnRNPA2B1是外泌体包裹miRNA的主要机制。在细胞中miRNA具有特定的基序,通过识别这些基序,hnRNPA2B1结合miRNA将其包裹进外泌体中,而SUMO化可调节hnRNPA2B1与miRNA的结合能力,因此细胞间通过外泌体交互是一种动态过程。由于缺乏从其他相似大小的膜囊泡中分离外泌体的有效技术,因此目前只能认为外泌体具有一定的异质性。
角质形成细胞在伤口愈合和炎症过程中发挥重要作用,而且作者先前研究表明角质形成细胞来源的细胞外囊泡对于将髓样细胞转化为肉芽组织中的成纤维细胞至关重要,但是角质形成细胞对炎症消退的作用尚不清楚,本研究揭示了角质形成细胞来源的外泌体携带miRNA调节肉芽组织中巨噬细胞数量和功能,并且对于形成功能性伤口闭合非常关键。
【结果】
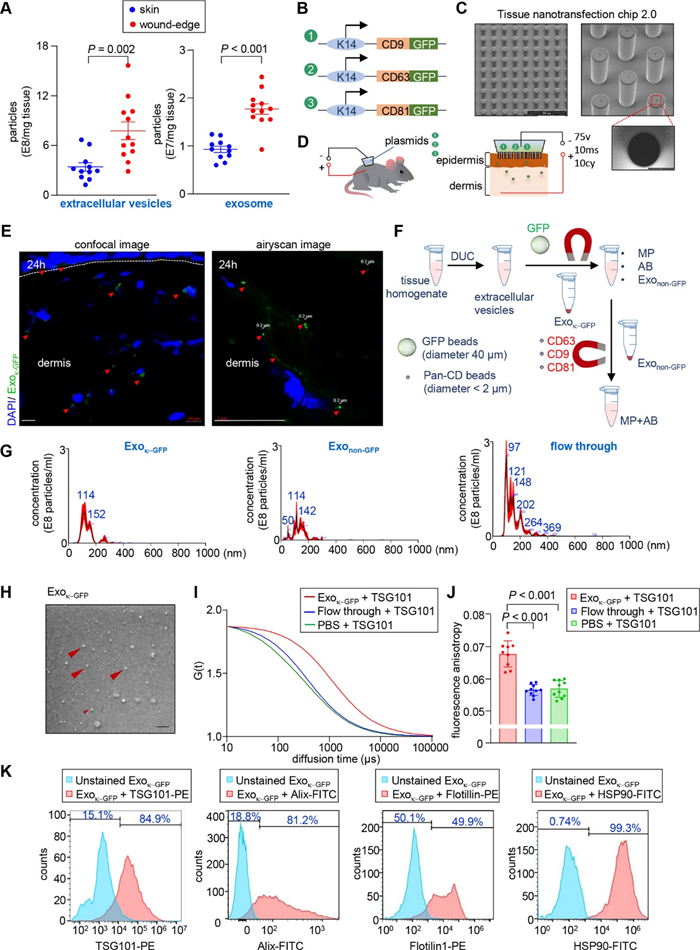
体外培养角质形成细胞用两步法分离EVs进行鉴定表征,检测不同时间伤口边缘EVs的浓度和细胞类型,伤后第5天EVs和外泌体量最高,有角质形成细胞、成纤维细胞以及血源性细胞(巨噬细胞)等,因此要区分伤口边缘的外泌体是由何种细胞分泌,构建三种仅在角质形成细胞中表达的编码CD9、CD63、CD81的GFP报告基因并在体内验证。
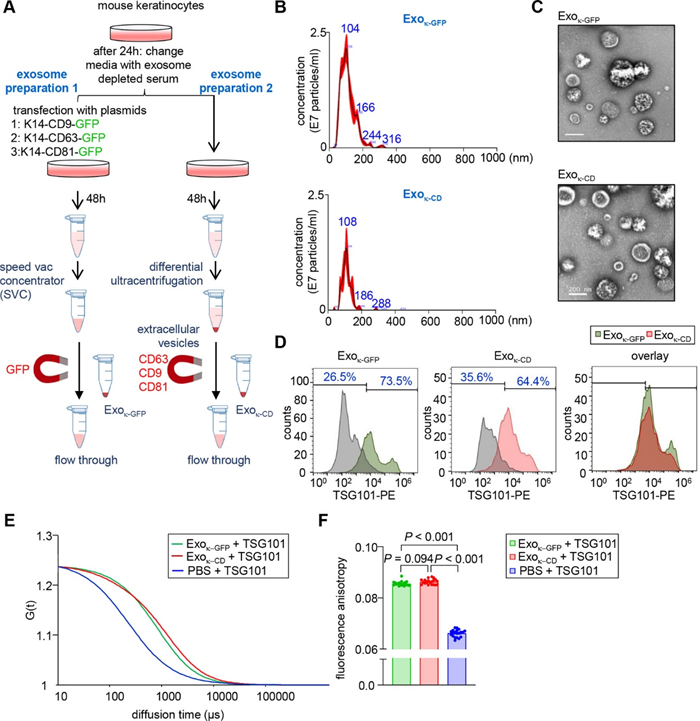
比较两步法分离的外泌体和传统超速离心方法分离的Exok-GFP外泌体量和大小,证实GFP转染后角质形成细胞的外泌体释放不受分离方法的影响。
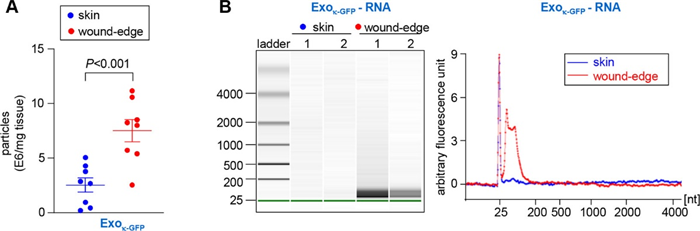
与皮肤相比,从野生型小鼠中分离的Exok-GFP在伤后第5天伤口边缘显著增加,并且该处有大量短RNA(<100bp),表明伤后第5天角质形成细胞释放大量包裹miRNA的外泌体参与损伤修复。
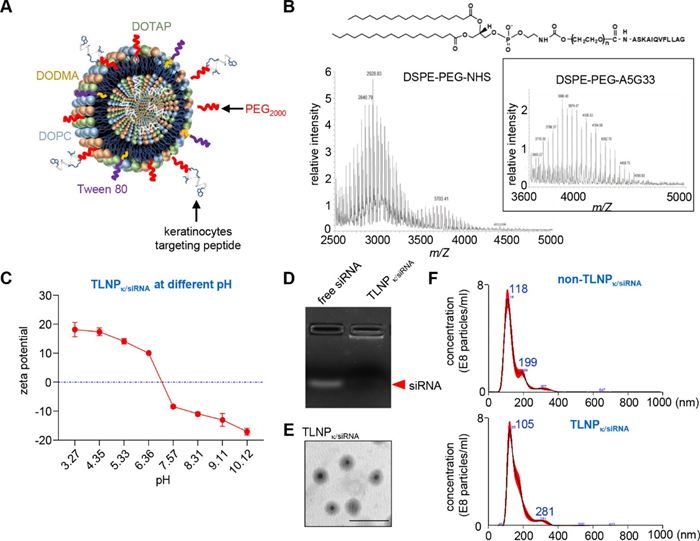
亲代细胞中miRNA丰度和外泌体中存在一定差异,表明外泌体在包裹miRNA时有特定的机制,据报道hnRNPAA2B1蛋白SUMO化后获得功能,调节外泌体包裹miRNA的能力,因此构建靶向角质形成细胞hnRNPA2B1蛋白的siRNA实现靶向敲低。
由角质形成细胞、内皮细胞、成纤维细胞组成的混合培养物检测脂质纳米颗粒(TLNPk)的靶向性,并检测其细胞毒性。
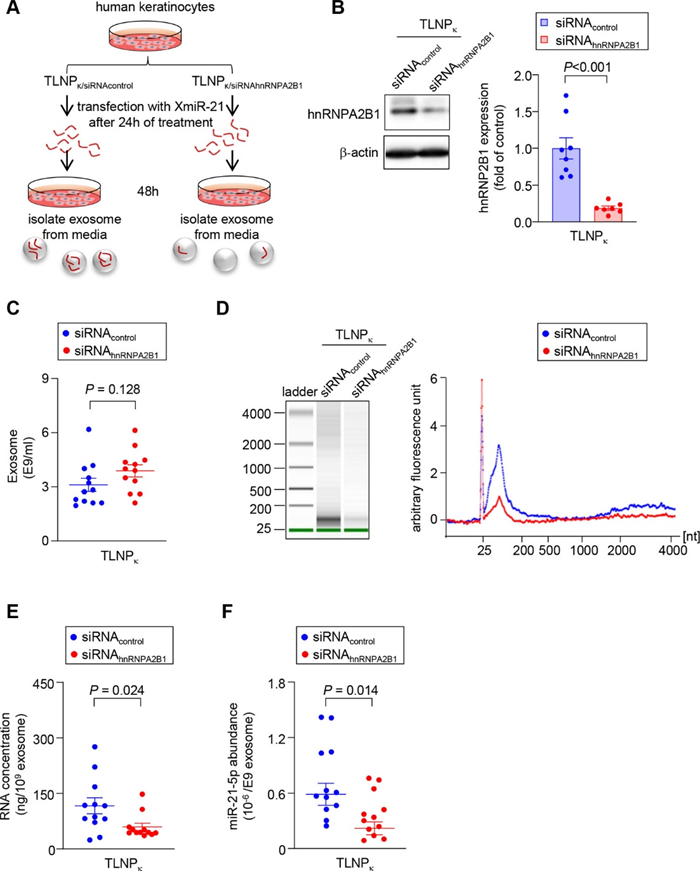
利用XMIR技术检测外泌体包裹miRNA的能力,检测sihnRNPA2B1及其对照组人角质形成细胞来源的外泌体数量及包裹的miRNA的量,结果表明特异性抑制角质形成细胞的hnRNPA2B1蛋白后,其来源的外泌体中miRNA的丰度显著降低。
体内实验验证靶向角质形成细胞的TLNPk/sihnRNPA2B1可抑制角质形成细胞包裹miRNA进入外泌体中,并检测损伤周边的巨噬细胞表型转变(促炎型/促修复型)。
为了研究TLNPk/si-hnRNPA2B1处理的小鼠第10天肉芽组织中丰富的促炎型巨噬细胞的重要性,检测组织愈合后上皮化皮肤的屏障功能。
|