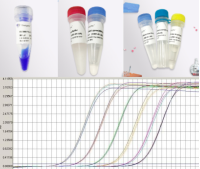
相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 库存:
大量
- 英文名:
Enterobacter sakazaki
- 保质期:
一年
- 供应商:
上海钰博生物科技有限公司
- 保存条件:
-20℃保存
- 规格:
50次
Enterobacter sakazaki
本试剂盒采用聚合酶链式反应(PCR)技术检测,可用于检测各种待检标本(如血液、粪便、食物、生物材料等)中所感染的特定细菌或病毒的某一特定基因,进而确定该细菌或病毒的感染/污染状态。试剂盒中所含引物能特异性扩增该细菌或者病毒的保守区域,不会交叉扩增细胞基因组。与传统的选择性培养基培养检测方法和免疫血清学检测方法相比较,本方法更为快速,特异性更高。
它具有下列特点:
1. 即开即用,用户只需要提供 DNA 模板。
2. 引物经过精心优化,专一性强,只扩增阪崎肠杆菌序列,与其他没有交叉反应。
3. 提供阳性对照,便于区分假阴性样品。
4. PCR mix 中含上样染料,PCR 后可以直接上样电泳。
5. 本试剂盒足够做 40μL 体系的 PCR 50 次,但只能用于科研。
规格及成分:
| 成 份 | 编号 | 十孔盒包装 |
| PCR MagicMix 3.0 | 试剂一 | 1 mL(红盖) |
| 超纯水 | 试剂二 | 1 mL(亮黄色) |
| 阪崎肠杆菌PCR 引物混合液 | 试剂三 | 100 μL(白盖) |
| 阪崎肠杆菌PCR 阳性对照(1×10E8 拷贝/μL) | 试剂四 | 50 μL(黄盖) |
| 使用手册 | ZY-99047 | 1份 |
运输及保存:
低温运输,-20℃保存,保存期限为一年。阳性对照需要单独放置,不要污染其他试剂。
自备试剂:
样本DNA。
使用方法:
一、样品 DNA 的制备
1. 用自选方法纯化 N+2 个样品的 DNA,本试剂盒跟市场上大多数核酸提取试剂盒兼容。
2. 如果有 N 个样品,则需要做 N+2 个提取,包括一个样品制备阳性对照和一个样品制备阴性对照。样品制备阳性对照是阪崎肠杆菌PCR 阳性对照的1000 倍稀释液,样品制备阴性对照是直接用水。提取结束后最后得到模板 DNA 放冰上待用。
二、设置 PCR 反应(40μL 体系)
3. 对 N+2 个样品,在 PCR 时需要增加一个 PCR 阳性对照和一个 PCR 阴性对照,故需要设置 N+4 个反应。在 N+4 个 PCR 管中分别加入下列成分:
成分 |
样品管 N+2 个 |
PCR 阴性对照 |
PCR 阳性对照 |
| PCR MagicMix 3.0 | 各 20 μL | 20 μL | 20 μL |
| 阪崎肠杆菌PCR 引物混合液 | 各 2 μL | 2 μL | 2 μL |
| N+2 个样品 DNA 模板 | 各 18 μL | - | - |
| PCR 阴性对照(水) | - | 18 μL | - |
| PCR 阳性对照(阪崎肠杆菌PCR 阳性对照的 1000 倍稀释液) | - |
- |
18 μL |
4. 按下表设置 PCR 反应:
| 过程 | 温度 | 时间 |
| 预变性 | 95℃ | 5 min |
PCR 反应 (35 个循环) |
95℃ | 15 sec |
| 57℃ | 15 sec | |
| 72℃ | 40 sec | |
| 最后延伸 | 72℃ | 10 min |
三、电泳检测
5. 取 10-20 μL PCR 产物。电泳检测 PCR 产物。本产品提供的 PCR Mix在扩增结束后可以直接上样,不需要另外再加 loading buffer。PCR 产物阳性对照必须有预期条带出现,阴性对照必须无任何扩增,否则实验无效。 对没有扩增产物的样品,可以稀释 10 倍后重复 PCR 扩增以排除 PCR 抑制剂的感染。
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验杆菌、寄生虫病等在内的数十种荧光定量PCR试剂盒,购买方便,价格便宜,并获得了国家相关认证。 值得一提的是鉴于当前流行病的频发以及实时荧光定量PCR技术的实际应用,国内外已将实时荧光定量PCR检测技术强制应用于相关行业并相继制定了国际、国家、及行业标准作为法律依据。例如: SN/T 1632.3-2005 奶粉中阪崎肠杆菌检验方法 荧光PCR方法 GB/T 19438.1-2004 禽流感病毒通用荧光RT
过敏源、转基因、乳品企业阪崎肠杆菌等检测。相比以往的药敏试验,接种感染实验以及免疫学等检测方法,不仅样本量需求少,而且操作简便,省时,灵敏度高,特异性好,结果更可靠。同样的还可应用于物种鉴定,基因分型等定性分析研究。 real time PCR技术不仅可用于定性分析,更多的是用于定量分析。其中绝对定量可用于(1)病毒及病原菌定量分析;(2)导入基因拷贝数解析;(3)GMO(转基因生物)定量检测。相对定量则多用于(1)差异显示结果验证,例如某一基因在生物体内不同发育阶段,不同组织器官的表达
。 (一)病原体测定 由于PCR技术的问世,使得病原体检测能够快速而方便的进行。但由于其高灵敏性,实验操作很容易受到污染而出现假阳性。只要有微量病原体存在,PCR扩增即可为阳性结果,但并不能作为诊断依据,只有当一定数量的病原体存在时才有临床意义,因此结模板定量显得特别重要。常规PCR由于不能定量而限制了其应用,然而,PE公司研制的FQ-PCR技术给解决这一问题提供了可能。目前该技术已经应用于丙肝病毒、人类乳头瘤病毒、结核杆菌和食品中大肠杆菌等许多病原体的检测研究。 Morris等[3]用FQ-PCR
 技术资料
技术资料暂无技术资料 索取技术资料