万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 保存条件:
低温冷藏
- 保质期:
详见说明书
- 英文名:
RT-LAMP kit for mouse hepatitis virus
- 库存:
100
- 供应商:
上海邦景
- 规格:
50次
1.仪器:分析天平、离心机、荧光 PCR 扩增仪、组织研磨器、-20 ℃冰箱、可调移液器(2 µL、20 µL、200 µL、1000 µL)。
2.耗材:荧光 PCR 专用反应管、眼科剪、眼科镊、生理盐水、1.5 mL 经焦碳酸二乙酯(DEPC)水 处理的灭菌离心管、吸头(10 µL、200 µL、1000 µL)、灭菌双蒸水。
【质控标准】
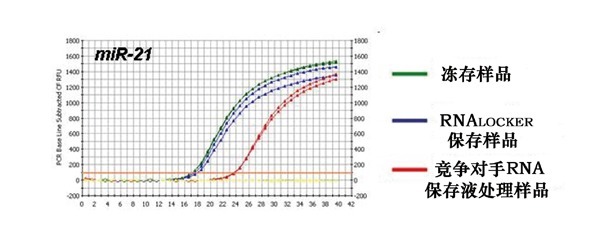
1. 阴性质控品的检测结果应为阴性,无指数扩增期,Ct=40或无Ct;
2. 阳性质控品的检测结果应为阳性,有明显的指数扩增期,Ct值应小于等于35;
3. 以上要求需在一次实验中同时满足,否则该次实验视为无效。
【结果判断】
1. 阳性:有明显的指数扩增期,且Ct<38; 2.可疑:有明显的指数扩增期,且38≤Ct<40,此时样本为可疑样本;对于可疑样本建议复核一次,若复核结果Ct<40且有指数扩增期,则判定为阳性,否则判定为阴性;
3. 阴性:无指数扩增期,Ct=40或无Ct值均判定为阴性样本。
【对检验结果的解释】
1. 实验室环境污染、试剂污染、样品交叉污染会出现假阳性结果;
2. 试剂运输、保存不当或试剂配制不准确引起的试剂检测效能下降,可能会导致出现假阴性结果。
实验注意事项:
1)RT-PCR可以检测组织、细胞、血液、细菌等很多材料,不同的样本有不同要求,实验前请充分沟通确认实验方案和样本情况;
2)客户尽可能提供实验的背景信息、物种、基因准确的名称和ID号;
3)客户尽量不要提供DNA或RNA样品。
4)样本保存于液氮或干冰,也可以保存于Trizol液中。
实时荧光定量PCR(quantitative real-time PCR,qPCR)是指在PCR反应体系中加入荧光基团,利用荧光信号积累实时监测整个PCR进程,最后通过标准曲线对未知模板进行定量分析的方法。实时荧光定量PCR的化学原理包括探针类和非探针类两类,探针类是利用与靶细胞序列特异性杂交的探针来指示扩增产物的增加,非探针类是利用荧光染料或者特异性设计的引物来指示扩增的增加。运用该技术可以对DNA、RNA样品进行定量(包括绝对定量和相对定量)和定性分析。
主要服务:DNA或RNA的绝对定量分析、基因表达差异分析、基因分型。
主要技术:引物设计、RNA提取、cDNA合成、qPCR。
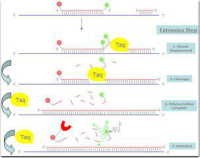
PCR反应的特异性决定因素为:
①引物与模板DNA特异正确的结合;
②碱基配对原则;
③Taq DNA聚合酶合成反应的忠实性;
④靶基因的特异性与保守性。
其中引物与模板的正确结合是关键。引物与模板的结合及引物链的延伸是遵循碱基配对原则的。聚合酶合成反应的忠实性及Taq DNA聚合酶耐高温性,
使反应中模板与引物的结合(复性)可以在较高的温度下进行,结合的特异性大大增加,被扩增的靶基因片段也就能保持很高的正确度。再通过选择特异性和保守性高的靶基因区,其特异性程度就更高。
(2) 灵敏度高
PCR产物的生成量是以指数方式增加的,能将皮克(pg=10-12g)量级的起始待测模板扩增到微克(ug=10-6g)水平。能从100万个细胞中检出一个靶细胞;在病毒的检测中,PCR的灵敏度可达3个RFU(空斑形成单位);在细菌学中zui小检出率为3个细菌。
(3) 简便、快速
PCR反应用耐高温的Taq DNA聚合酶,一次性地将反应液加好后,即在DNA扩增液和水浴锅上进行变性-退火-延伸反应,一般在2~4 小时完成扩增反应。扩增产物一般用电泳分析,不一定要用同位素,无放射性污染、易推广。
(4) 对标本的纯度要求低
不需要分离病毒或细菌及培养细胞,DNA 粗制品及总RNA均可作为扩增模板。可直接用临床标本如血液、体腔液、洗嗽液、毛发、细胞、活PCR技术概论。
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验小鼠肝炎病毒抗原(MHV Ag) 酶联免疫 分析( ELISA ) 试剂 盒使用说明书 本试剂仅供研究使用 目的:本试剂盒用于检测小鼠血清,血浆中肝炎病毒抗原(MHV Ag)水平。 实验原理 : 本试剂盒 采 用双抗 体 夹心 酶联免疫 法 (ELISA ) 测定 标本 中 小鼠肝炎病毒抗原(MHV Ag) 。用纯化的 小鼠肝炎病毒(MHV) 抗体 包被微孔板,制成固相抗 体 , 可与样品中肝炎病毒抗原(MHV
的5'和3’末端的有效方法,以其简单、快速、廉价等优势而受到越来越多的重视。经典的RACE技术是由Frohman等(1988)发明的一项技术,主要通过RT-PCR技术由已知部分cDNA序列来得到完整的cDNA5’和3’端,包括单边PCR和锚定PCR。该技术提出以来经过不断发展和完善,克服了早期技术步骤多、时间长、特异性差的缺点(Frohman等,1995:Schaefer,l995: Chen,1998: Bespalova等,1998: Matz等11999)。对传统RACE技术的改进主要是引物设计及RT
组织WHO、各国学者和相关政府部门的关注,短短几年,该技术已成功地应用于SARS、禽流感、HIV等疾病的检测中,在这次甲型H1N1流感事件中,日本荣研化学公司接受WHO的邀请进行H1N1 LAMP试剂盒的研制。通过荣研公司近十年的推广,LAMP技术已广泛应用于日本国内各种病毒、细菌、寄生虫等引起的疾病检测、食品化妆品安全检查及进出口快速诊断中,并得到了欧美国家的认同。LAMP方法的优势除了高特异性、高灵敏度外,操作十分简单,对仪器设备要求低,一台水浴锅或恒温箱就能实现反应,结果的检测也很简单,不需要像PCR
 技术资料
技术资料暂无技术资料 索取技术资料