相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 规格:
96次
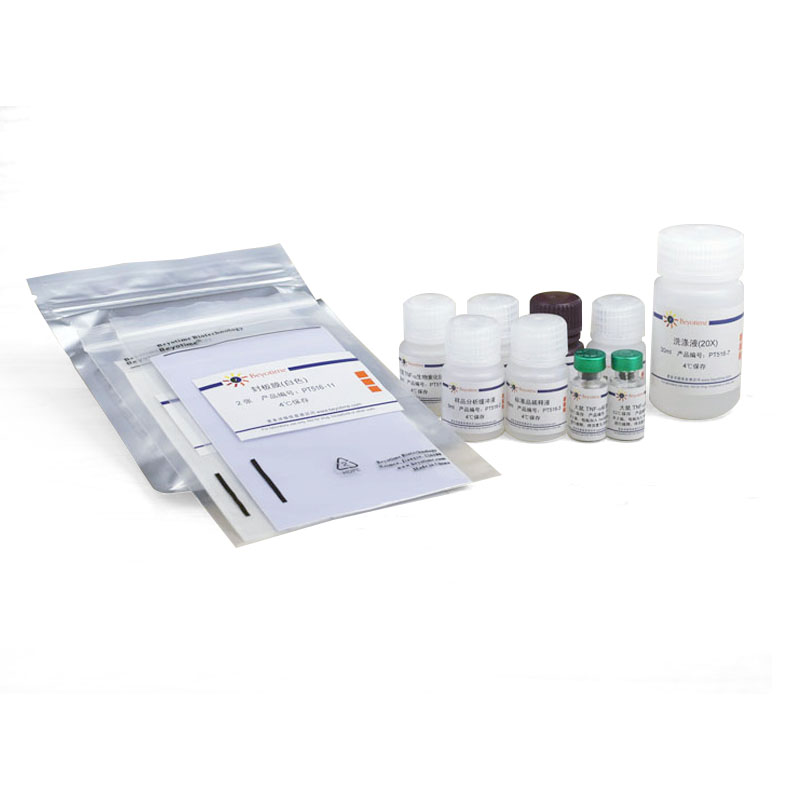
碧云天的Rat TNF-α ELISA Kit (Rat Tumor Necrosis Factor-α Enzyme-Linked ImmunoSorbent Assay Kit),即大鼠肿瘤坏死因子-α酶联免疫吸附检测试剂盒,是一种用于特异性地高灵敏地定量检测大鼠血清、血浆、细胞或组织裂解液、或细胞培养上清液中的TNF-α的试剂盒。
本产品检测灵敏度高,特异性强,重复性好。多次重复检测结果表明,最小检出量为26pg/ml,与GDNF、IL-1α、IL-1β、IL-2、IL-4、PDGF-BB、IL-10、人TNF-α、小鼠TNF-α等均没有交叉反应,板内、板间变异系数均小于10%。
TNF-α,即TNF、TNFα或TNFalpha,也称cachectin、cachexin或TNFSF1A。TNF-α由巨噬细胞、上皮细胞等多种细胞在细菌感染、内毒素刺激、病毒或寄生虫感染时产生。肿瘤坏死因子超家族(Tumor necrosis factor superfamily)共约19个成员,包含由巨噬细胞等产生的TNF-α和T淋巴细胞产生的TNF-β(也称Lymphotoxin-alpha),以及FASL、TRAIL、CD40L、CD27L、CD30L等。TNF-α与TNF-β在结构上有一定的相似性,并且在氨基酸水平有28%的同源性,它们拥有共同的受体TNFR1和TNFR2。由于TNF-α的生物学活性占TNF总活性的70%~95%,因此目前常说的TNF多指TNF-α。TNF (Tumor Necrosis Factor)因为能诱导细胞死亡而得名,实际上其很多时候诱导的细胞死亡为细胞凋亡。人TNF-α有两种形式,一种是由233个氨基酸组成的跨膜蛋白同源三聚体(homotrimers),另外一种是该跨膜蛋白在TNF-α转化酶TACE(TNF-α converting enzyme)的作用下切除信号肽,形成成熟的157个氨基酸的可溶性TNF-α单体(分子量为17KDa)的同源三聚体。无论TNF-α的跨膜同源三聚体还是可溶性同源三聚体(51kD),都具有生物学活性,但活性的差异目前仍有争议。小鼠和人的TNF-α有约79%的氨基酸同源性,也同样形成同源三聚体发挥作用。TNF-α可以诱导产生炎症反应、发烧(fever)、细胞凋亡、抑制肿瘤形成和病毒复制等。TNF-α也参与了包括哮喘、克罗恩氏病、类风湿性关节炎、神经性疼痛、阿兹海默症、肥胖症、II型糖尿病、自身免疫病和肿瘤等疾病的发生发展。
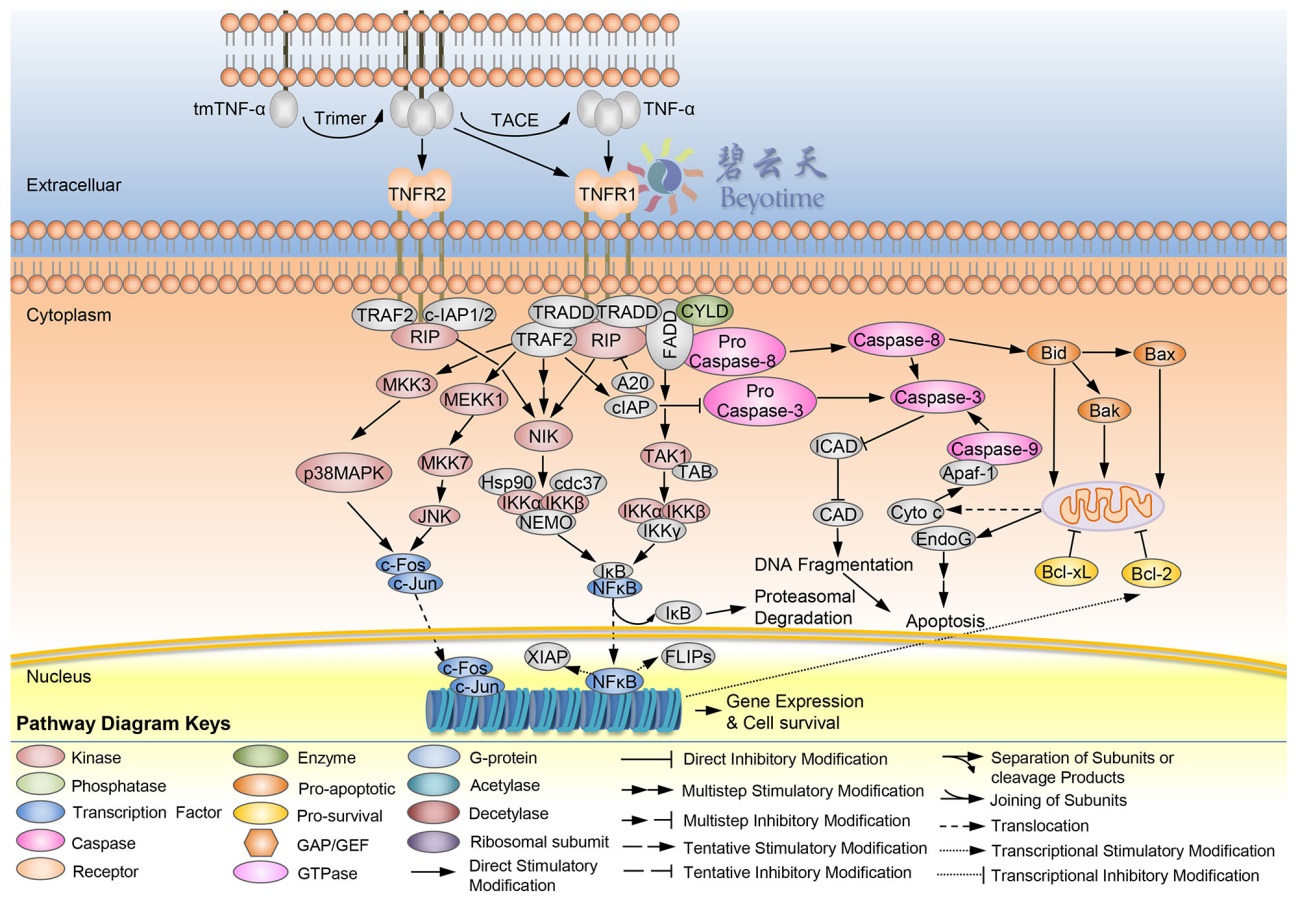
图1. TNF-α的信号通路示意图
TNF-α被诱导分泌后,其同源三聚体与受体TNFR1(TNF receptor, type I)或TNFR2(TNF receptor, type II)结合而引发其下游信号通路的一系列反应。TNF-α的信号通路参见图1。TNFR1在大多数组织中有表达,而TNFR2主要在免疫细胞中表达。TNF-α的跨膜同源三聚体和可溶性同源三聚体都可以完全激活TNFR1,而TNFR2仅对TNF-α的跨膜同源三聚体产生响应。
本试剂盒采用双抗体夹心ELISA法(Sandwich ELISA)检测样品中靶蛋白的的浓度,其原理见图2。靶蛋白特异的单克隆捕获抗体已预包被于酶标板上,当加入标准品或样品时,其中的靶蛋白会与捕获抗体结合。当加入生物素化的抗靶蛋白抗体后,生物素化抗靶蛋白抗体与靶蛋白结合,形成夹心的免疫复合物。随后加入辣根过氧化物酶标记Streptavidin(HRP-Streptavidin),由于生物素与链霉亲和素(Streptavidin)可以特异性地结合,因此链霉亲和素连接的HRP就会与夹心的免疫复合物连接起来而被固相捕获。最后加入显色剂TMB溶液,固相捕获的辣根过氧化物酶就会催化无色的显色剂氧化成蓝色物质,在加入终止液后呈黄色。通过酶标仪检测450nm处的吸光度值就能实现定量检测。靶蛋白浓度与A450值呈正比,通过绘制标准曲线,对照样品吸光度值,即可计算出样品中靶蛋白浓度。
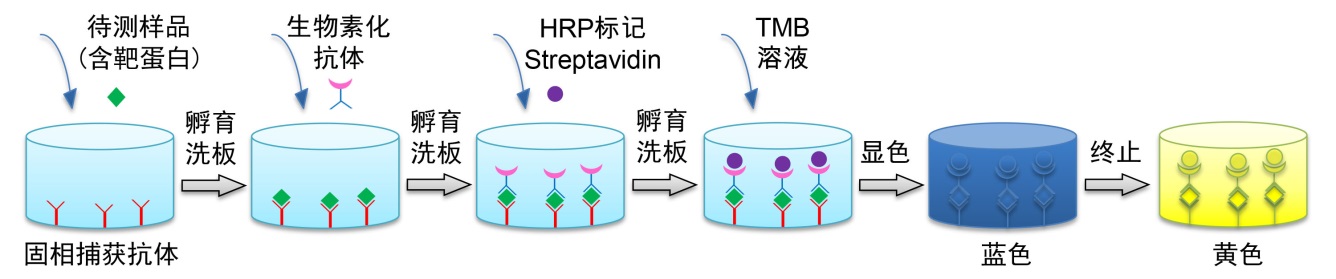
图2. 双抗体夹心ELISA原理图。
一个包装的本试剂盒,包括标准品检测,可以进行96次检测。
包装清单:
| 产品编号 | 产品名称 | 包装 |
| PT516-1 | 大鼠TNF-α抗体预包被板 | 8孔×12条 |
| PT516-2 | 样品分析缓冲液 | 5ml |
| PT516-3 | 标准品稀释液 | 10ml |
| PT516-4 | 大鼠TNF-α标准品 | 2-4瓶 |
| PT516-5 | 大鼠TNF-α生物素化抗体 | 10ml |
| PT516-6 | 辣根过氧化物酶标记Streptavidin | 10ml |
| PT516-7 | 洗涤液(20X) | 30ml |
| PT516-8 | TMB溶液 | 10ml |
| PT516-9 | 终止液 | 5ml |
| PT516-10 | 封板膜(透明) | 2张 |
| PT516-11 | 封板膜(白色) | 2张 |
| — | 说明书 | 1份 |
保存条件:
除标准品外,4℃保存6个月内有效。标准品4℃保存,1-2周内有效,-20℃保存6个月内有效。注意TMB溶液避光保存。
注意事项:
由于标准品一般是冻干粉,在制备后需要严格校准,所以标准品的瓶数及每瓶标准品所需加入的稀释液体积请以实际收到的试剂盒及标准品标签上的标注为准。
洗涤液(20X)在低温下可能有结晶,如果发现有结晶,请室温水浴加热使结晶完全溶解后再配制工作液。
为保证标准品的精确性,标准品配制使用后,如果有剩余请勿再次使用。
TMB对人体有刺激性,操作时请小心,并注意适当防护以避免直接接触人体或吸入体内。
如果发现TMB辣根过氧化物酶显色液出现混浊或颜色变成蓝色,应该停止使用。
加样时,请注意每个样品或标准品必须更换枪头,一方面避免交叉污染,另一方面也避免吸取体积的误差。
不宜混用不同批号的试剂盒组份,每批次试剂盒均经过独立测试。
充分混匀对保证反应结果的精准性很重要,在加液后请轻轻晃动整个96孔板,以保证混匀。
本试剂盒很多操作在室温进行,要求严格控制室温在25-28℃。温度低于25℃会导致最终检测到的吸光度显著下降。
洗涤过程非常重要,洗涤不充分会使精确度下降并导致结果误差较大。
检测标准品和样品时建议设置重复孔,以确保检测结果的可信度。
加样过程中须避免气泡的产生。
本产品仅限于专业人员的科学研究用,不得用于临床诊断或治疗,不得用于食品或药品,不得存放于普通住宅内。
为了您的安全和健康,请穿实验服并戴一次性手套操作。
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验RAT/MOUSE GROWTH HORMONE ELISA KIT
实验原理 This assay is a Sandwich ELISA based, sequentially, on: 1) capture of rat or mouse Growth Hormone molecules from samples to the wells of a microtiter plate coated by a pre-titered amount of anti-Growth Hormone
saline (PBS) (Cat. no. 10010-049) or equivalent Optional: ArC™ Amine Reactive Compensation Bead Kit (Cat. no. A10346) 实验步骤 1. Using the AbC™ anti- Rat/Hamster Bead Kit 1) Completely resuspend the AbC™ RH
RNA was purified using the AllPrep DNA/RNA 96 Kit and analyzed on the Agilent 2100 bioanalyzer. Intact RNA is indicated by a RIN value of close to 10. RNA with no genomic DNA contamination. Total RNA was purified from rat kidney
 技术资料
技术资料暂无技术资料 索取技术资料