相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 库存:
52
- 英文名:
Edwardsiella ictaluri
- 保质期:
详见说明书
- 供应商:
上海一研
- 保存条件:
低温冷藏
- 规格:
50T
| 产品名称 | 鮰爱德华氏菌探针法荧光定量PCR试剂盒 |
| 英文名称 | Edwardsiella ictaluri |
| 编号 | EY00P3944 |
鮰爱德华氏菌探针法荧光定量PCR试剂盒从土壤农杆菌 CP4 菌株中分离得到的抗除草剂草甘膦基因,是转基因植物研究中最为常用的一种筛选标记基因,因此本公司根据探针法 qPCR 原理开发了专门用于检测鮰爱德华氏菌探针法荧光定量PCR试剂盒的试剂盒,它具有下列特点:
1. 即开即用,用户只需要提供样品 DNA 模板。
2. 根据鮰爱德华氏菌探针法荧光定量PCR试剂盒保守区域设计引物和探针,能专一性地检测出样品中的鮰爱德华氏菌探针法荧光定量PCR试剂盒成分,但不能检测其他非鮰爱德华氏菌探针法荧光定量PCR试剂盒成分。
3. 提供阳性对照,便于区分假阴性样品。
4. 一管式闭管操作,降低了交叉污染。
5. 快速,整个检测过程(按一个样品计)所需时间仅为 2.0 小时。
6. 本只能用于科研,足够 50 次 20uL 体系的探针法荧光定量 PCR。
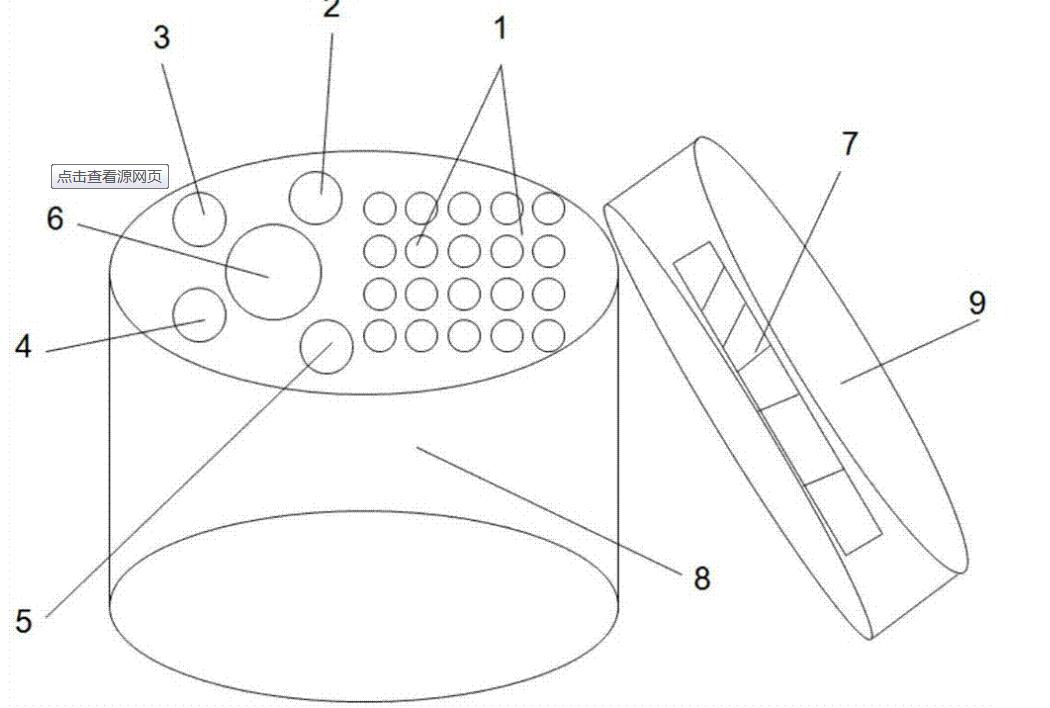
【技术保护点】
1.一种实时荧光定量PCR检测EB病毒C/D基因基因分型试剂盒,其特征在于,由定量PCR反应液(1)、C型标准品(2)、D型标准品(3)、阳性对照品(4)、阴性对照品(5)、病毒DNA抽提裂解液(6)、操作说明书(7)、盒体(8)、盒盖(9)组成,其中定量PCR反应液(1)含有PCR缓冲液、Mgcl2、dNTPs、EB病毒C/D基因基因通用上游引物、EB病毒C/D基因基因通用下游引物、C型荧光探针、D型荧光探针、Taq DNA聚合酶,上游引物序列为:5’ATACTCCCGCCATGCGACT3’,下游引物序列为:5’CTGTCACAACCTCACTGTCAT3’C型荧光探针为:5’FAMCCTGCGGACCCCGATMGB 3’,D型荧光探针为:5’VICCCTGCGGATCCCGATMGB 3’。
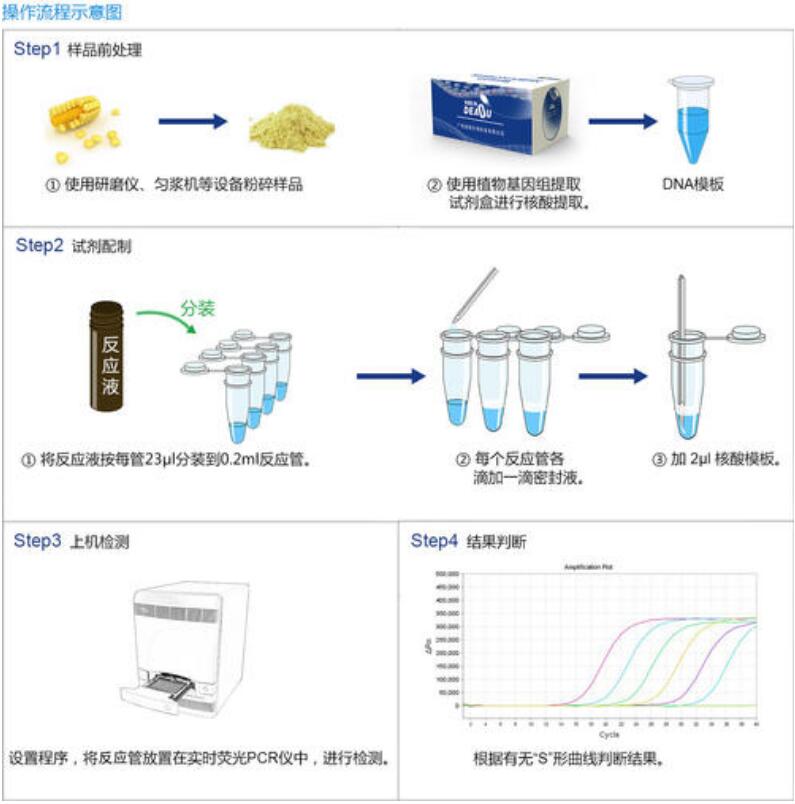
荧光定量PCR检测方法包括以下步骤:
(1)将参照基因与待测目的基因片段等比例连接,克隆到同一个质粒载体上,构建一种可同时用于参照基因以及待测目的基因扩增检测的标准品,并将所得标准品按照浓度梯度稀释后同时用于绘制参照基因以及待测目的基因的标准曲线;
(2)待测样本与步骤(1)所述标准品经同步进行实时荧光定量PCR扩增后,目的基因与参照基因按照各自的标准曲线计算各自的拷贝数,计算待测样本的目的基因与参照基因拷贝数比值,即得目的基因的拷贝数相对定量检测结果。
其中步骤(1)为:将参照基因与待测目的基因片段等比例连接,克隆到同一个质粒载体上,构建一种可同时用于参照基因以及待测目的基因扩增检测的标准品,并将所得标准品按照浓度梯度稀释后同时用于绘制参照基因以及待测目的基因的标准曲线。
其中所述参照基因为本领域常规参照基因,较佳地管家基因,优选地为RPPH1的扩增区域,其中所述质粒载体为本领域常规质粒载体,较佳地为PCR克隆载体,优选地为TA cloning载体,所述TA cloning载体较佳地为pMD18-T载体。其中所述标准品的核酸序列如序列表中SEQ ID NO:6所示。所述的等比例较佳地为1:1。由于标准品中待测目的基因与参照基因的比例为1:1,解决了目前相对标准曲线法应用中目的基因与参照基因的浓度比例关系难以控制的问题,提高HER2基因扩增检测的可靠性。
步骤(2)为:待测样本与步骤(1)所述标准品经同步进行实时荧光定量PCR扩增后,目的基因与参照基因按照各自的标准曲线计算各自的拷贝数,计算待测样本的目的基因与参照基因拷贝数比值,即得目的基因的拷贝数相对定量检测结果。
其中所述待测目的基因为本领域常规待测目的基因,较佳地为肿瘤或者疾病的特异性基因,更佳地为HER2基因的扩增区域,所述荧光定量PCR扩增为本领域常规荧光定量PCR扩增方法,所述荧光定量PCR扩增方法较佳地为多通道荧光定量PCR扩增,更佳地为双通道荧光定量PCR扩增。
以下是公司正在促销打折产品:
Fraser Medium 250g Fraser培养基
Fortum 3mg/支*5 复达欣
Folic Acid Assay Medium 250g 烟酸测定培养基
Folic Acid Assay Medium 250g 叶酸测定培养基
Fluid Tetrathionate Medium 250g 液体连四酸盐培养基
Fluid Lactose Medium 250g 液体乳糖培养基
Filter Membrane Enterococcus Agar 250g 滤膜肠球菌琼脂
COX5A 细胞色素c氧酶5A抗体 特价促销
COX5B 抗體, 兔單抗
COX5B 抗體, 兔多抗
COX5B 抗體, 兔多抗, 抗原親和純
COX5B 抗體, 兔多抗, 抗原親和純
COX6B 细胞色素C氧酶亚基6B抗体 特价促销
COX7A2 细胞色素c氧酶7A2抗体 特价促销
COX7A2 细胞色素c氧酶COX7A2抗体 特价促销
COX7A2 细胞色素c氧酶VIIA亚型2抗体 特价促销
Coxsackie Adenovirus Receptor 柯萨奇病毒蛋白受体B抗体 特价促销
Anti-KChIP1 KChIP1抗体(0.2 ml)
Anti-KCC1 KCC1抗体(50 ul)
Anti-KCC1 KCC1抗体(25 ul)
Anti-KCC1 KCC1抗体(0.2 ml)
Anti-KCa4.2 (Slick) KCa4.2 (Slick)抗体(50 ul)
Anti-KCa4.2 (Slick) KCa4.2 (Slick)抗体(0.2 ml)
Anti-KCa4.1 (Slack) KCa4.1 (Slack)抗体(50 ul)
Anti-KCa4.1 (Slack) KCa4.1 (Slack)抗体(25 ul)
Anti-KCa4.1 (Slack) KCa4.1 (Slack)抗体(0.2 ml)
Anti-KCa3.1 (SK4, IKCa1) KCa3.1 (SK4, IKCa1)抗体(50 ul)
鮰爱德华氏菌探针法荧光定量PCR试剂盒聚山梨酯80培养基(真菌)250克Tween80 Medium(Fungi)油剂的真菌无菌试验
真菌琼脂培养基250克Fungi Agar生物制品真菌无菌检验
虎红钠盐琼脂培养基250克Rose Bengal Agar生物制品真菌、酵母菌计数
沙氏琼脂培养基250克Sabouraud′s Agar用于真菌检测
改良沙氏琼脂培养基250克Sabouraud′s Agar,Modified真菌检测
沙氏液体培养基250克Liquid Sabourand Medium真菌、酵母菌增菌培养
包装:5 × 105次方(1ml)心肌成纤维细胞 进口/国产
包装:5 ×105次方(1ml)心肌细胞 进口/国产
包装:5 ×105次方(1ml)心肌细胞 进口/国产
包装:5 ×105次方(1ml)心肌细胞 进口/国产
包装:5 × 105次方(1ml)心室肌细胞 进口/国产
技术原理:
DNA的半保留复制是生物进化和传代的重要途径。双链DNA在多种酶的作用下可以变性解链成单链,在DNA聚合酶与启动子的参与下,根据碱基互补配对原则复制成同样的两分子挎贝。在聚合酶链式反应实验中发现,DNA在高温时也可以发生变性解链,当温度降低后又可以复性成为双链。因此,通过温度变化控制DNA的变性和复性,并设计引物做启动子,加入DNA聚合酶、dNTP就可以完成特定基因的体外复制。( DNA高温变性低温复性)发现耐热DNA聚合同酶--Taq酶对于PCR的应用有里程碑的意义,该酶可以耐受90℃以上的高温而不失活,不需要每个循环加酶,使PCR技术变得非常简捷、同时也大大降低了成本,PCR技术得以大量应用,并逐步应用于临床。
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验相关专题 实验室很多同学都要做Real time PCR实验,实验室的师兄师姐都会有很多宝贵意见,不过也有实验室前没有做过的,查找了下资料和大家分享下关于实时荧光 Taqman 探针设计、实时荧光PCR探针的选择、引物的设计及评价。 荧光探针法是用序列特异的荧光标记探针来检测产物,探针法的出现使得定量PCR技术的特异性比常规PCR技术大大提高。目前较常提及的有TaqMan探针、FRET杂交 探针(荧光共振能量传递探针)和分子
所特有的,下游引物为通用引物就可以了。 荧光定量PCR检测方法有SYBR Green染料法和TaqMan探针法。前者需要调整引物浓度以及引物扩增效率,把引物二聚体调整到越小越好;探针法则需要设计荧光探针,这其中由于MGB探针需要碱基数量少和特异性好的特点而被推荐。 探针设计位置有3个:完全与miRNA序列相同、在miRNA与RT引物的交叉点、完全在RT引物上;这其中又有正向和反向互补两种情况。至于探针要设计在那个位置,根据自己试验情况而定,本人以为效果都差不多。 四、试验操作流程
缺陷个体。根据国际惯例,要求对易受沙门氏菌污染的食品进行分类管理,以使大多数食物不含沙门氏菌,从而有效预防沙门氏菌病。为此,人们在探索沙门氏菌检测方法的过程中,作出了不懈的努力,现将有关进展报告如下,并介绍两种快速检测沙门氏菌的试剂盒。 自19世纪后期,沙门氏菌首次被鉴定为人类的一种病原以来,检测方法学都是建立在采取感染病人的粪便或血液作为临床病料的基础上。此后的60年间,用于从食品中分离沙门氏菌的方法实质上与那些用于临床病料的方法是相同的。但至少有三个因素限制了用于
 技术资料
技术资料暂无技术资料 索取技术资料