相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 库存:
5000
- 供应商:
蒂科生物
- 检测范围:
详询
- 检测方法:
ELISA
- 应用:
科研实验
- 适应物种:
详询
- 标记物:
参考说明
- 样本:
详询
- 规格:
96T/48T
人粒细胞集落刺激因子定量分析酶联免疫检测试剂盒
本试剂盒仅供科研使用。用于体外定量检测人血清、血浆或细胞培养上清液中的G-CSF浓度。使用前请仔细阅读说明书并检查试剂组分是否完整,。如有产品包装破损或质量投拆,请在收到货一个月之内联系我们。
G-CSF简介:
粒细胞集落刺激因子(G-CSF)是一个由噬中性粒细胞和单核细胞受刺激或抵抗细菌感染后产生的天然细胞因子,主要由单核细胞和巨噬细胞在内毒素、TNF-α和 IFN-γ等的刺激后产生。在受脂蛋白、IL-1 或 TNF-α等刺激后,一些如成纤维细胞、内皮细胞、星形胶质细胞、骨基质细胞等类型的细胞都可分泌G-CSF,此个,各类肿瘤细胞系和髓系白血病细胞也能分泌G-CSF。
在人类来说,G-CSF蛋白可由两个活性明显有差异的异构体,分别来源于207个氨基酸的前体蛋白和204个氨基酸的前体蛋白。两者均有30个氨基酸的信号肽,除了在N末端第35位有3个插入的氨基酸的区别外,两个蛋白有相同的蛋白序列。据报道前体是204个氨基酸的成熟蛋白的活性比前体为207的成熟蛋白活性强十倍。
G-CSF已证明有好几方面的治疗应用,包括治疗新生儿感染、急性心肌梗塞、粒细胞减少症中粒细胞静脉注射、严重的感染和脓毒症、自身免疫性的粒细胞减少症,急性髓系白血病的治疗、艾滋的治疗及斯维茨综合症的治疗等。
检测原理:
本试剂盒采用双抗体夹心ELISA法检测样本中G-CSF的浓度。G-CSF捕获抗体已预包被于酶标板上,当加入标本或参考品时,其中的G-CSF会与捕获抗体结合,其它游离的成分通过洗涤的过程被除去。当加入生物素化的抗人G-CSF抗体后,抗人G-CSF抗体与G-CSF接合,形成夹心的免疫复合物,其它游离的成分通过洗涤的过程被除去。随后加入辣根过氧化物酶标记的亲合素。生物素与亲合素特异性结合,亲合素连接的酶就会与夹心的免疫复合物连接起来;其它游离的成分通过洗涤的过程被除去。最后加入显色剂,若样本中存在G-CSF将会形成免疫复合物,辣根过氧化物酶会催化无色的显色剂氧化成蓝色物质,在加入终止液后呈黄色。通过酶标仪检测,读其450nm处的OD值,G-CSF浓度与OD450值之间呈正比,通过参考品绘制标准曲线,对照未知样本中OD值,即可算出标本中G-CSF浓度。
人G-CSF定量分析酶联免疫检测试剂盒组成:
| 组分 |
规格(96T/48T) |
| 人G-CSF预包被板 |
12条/6条 |
| 样本分析缓冲液 |
5ml/3ml |
| 标准品稀释液 |
10ml/5ml |
| 人G-CSF标准品 |
2支/1支(冻干)* |
| 人G-CSF生物素化抗体 |
10ml/5ml |
| 亲和素连接的HRP酶 |
10ml/5ml |
| 浓缩洗涤液 20× |
30ml/15ml |
| TMB底物 |
10ml/5ml |
| 中止液 |
5ml/3ml |
| 封板胶纸 |
3/2张 |
| 说明书 |
1份 |
标本收集:
1.标本的收集请按下列流程进行操作;
A.细胞上清标本离心去除悬浮物后即可;
B.血清标本应是自然凝固后,取上清,避免在冰箱中凝固血液;
C.血浆标本,推荐用EDTA的方法收集若待测样本不能及时检测,
D.标本收集后请分装,冻存于-20℃,避免反复冻融。
2.血清标本不应添加任何防腐剂或抗凝剂;
3.标本应清澈透明,检测前样本中如有悬浮物应通过离心去除。
4.请勿使用溶血,高血脂或污染的标本检测,否则结果将不准确。
注:人血清或血浆样本请用样本分析缓冲液做倍比稀释后再检测。
注意事项:
1.试剂盒请保存在2~8℃。
2.浓缩洗涤液因在低温下可能有结晶,请水浴加热使结晶完全溶解后再配制工作液。
3.标准品复溶加样后,剩余部份请丢弃。
4.底物请勿接触氧化剂和金属。
5.加样时,请及时更换枪头,避免交叉污染。
6.严禁混用不同批号的试剂盒组份。
7.充分混匀对保证反应结果的准性很重要,在加液后请轻轻叩击边缘以保证混匀。
8.室温反应,请严格控制在25~28℃。
9.洗涤过程是至关重要的,洗涤不充分会使精确度下降并导致结果误差较大。
10.试验中标准品和样本检测时建议作双复孔。
11.加样过程中避免气泡的产生。
12.血清和血浆标本的检测时,检测抗体的孵育时间应适当延长。
检测前准备工作:
1.试剂盒自冰箱中取出后应置室温(25~28℃)平衡20分钟;每次检测后剩余试剂请及时于2~8℃保存。
2.将浓缩洗涤液用双蒸水或去离子水稀释(1份加19份水)。
3.如有5X标准品稀释液按所需用双蒸水或去离子水稀释(1份加4份水)。
4.标准品:按标签复溶体积加入标准品稀释液复溶使G-CSF终浓度达到2000pg/ml,室温反应,请严格控制在25~28℃,静置10~15分钟后轻轻混悬(建议抽吸几次)待彻底溶解,用标准品稀释液倍比梯度稀释后依次加入检测孔中。(标准曲线取七个点,最高浓度为2000 pg/ml,标准品稀释液直接加入作为0浓度.)
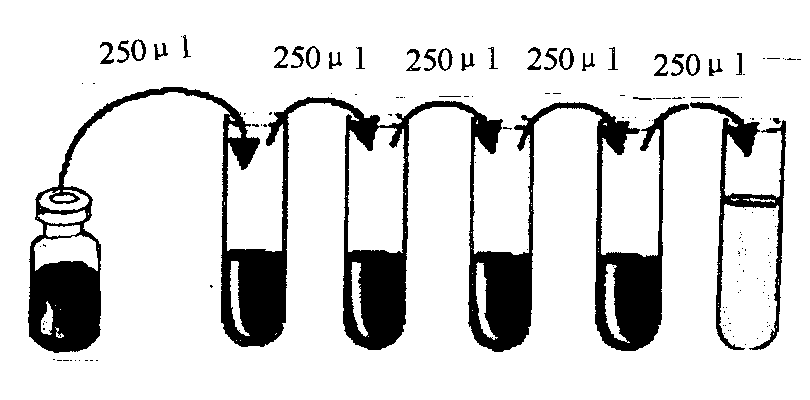
洗涤方法:
自动洗板机或人工洗板:每孔洗涤液为300ul,注入与吸出间隔15-30秒。洗板5次。最后一次洗板完成后将板倒扣着在厚吸水纸上用力拍干。
实验过程需自备的材料:
1.不同规格的加样枪及相应的枪头;
2.酶标仪;
3.自动洗板机;
4.去离子水或双蒸水;
操作步骤:
1.通过计算并确定一次性实验所需的板条数,取出所需板条放置在框架内,暂时用不到板条请放回铝箔袋密封,保存于4℃。
2.建议设置本底较正孔,即空白孔,设置方法为该孔只加TMB显色液和中止液。每次实验均需做标准品对照并画出标准曲线。
3.分别将标本或不同浓度标准品(100ul/孔)加入相应孔中,用封板胶纸封住反应孔,室温(25~28℃)孵育120分钟。对于血清或血浆标本,请加入50 ul样本分析缓冲液后加50 ul标本, 如稀释量大,请将样本与样本分析缓冲液等量加入,不足部分用标准品稀释液补充至100ul。
4.洗板5次,且最后一次置厚吸水纸上拍干。
5.加入生物素化抗体工作液(100ul/孔)。用封板胶纸封住反应孔,室温(25~28℃)孵育60分钟。
6.洗板5次,且最后一次置厚吸水纸上拍干。
7.加入亲和素链接的HRP酶工作液(100ul/孔)。用封板胶纸封住反应孔,避光室温(25~28℃)孵育20分钟。
8.洗板5次,且最后一次置厚吸水纸上拍干。
9.加入显色剂TMB100ul/孔,避光室温(25~28℃)孵育20分钟。
10.加入终止液50ul/孔,混匀后即刻测量OD450值。
结果判断:
1.复孔的值在20%的差异范围内结果才有效,复孔的值平均后可作为测量值。
2.每个标准品或标本的OD值应减去本底校正孔的OD值。
3.手工绘制标准曲线。以标准品浓度作横坐标,OD值作纵坐标,以平滑线连接各标准品的坐标点。通过标本的OD值可在标准曲线上查出其浓度。
4.若标本OD值高于标准曲线上限,应适当稀释后重测,计算浓度时应乘以稀释倍数。
典型数值和参考曲线
| 浓度pg/ml |
典型OD值1 |
典型OD值2 |
OD平均值 |
| 0 |
0.08974 |
0.11426 |
0.102 |
| 62.5 |
0.02514 |
0.52386 |
0.2745 |
| 125 |
0.4472 |
0.5062 |
0.4767 |
| 250 |
0.7541 |
0.8091 |
0.7816 |
| 500 |
1.09872 |
1.23828 |
1.1685 |
| 1000 |
1.5427 |
1.7799 |
1.6613 |
| 2000 |
2.1745 |
2.3409 |
2.2577 |
人G-CSF参考标准曲线
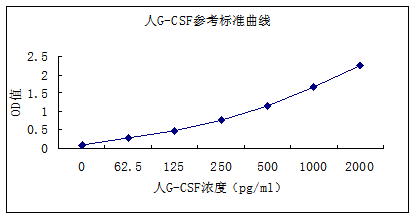
注意:本图仅供参考,应以同次试验标准品所绘标准曲线计算标本含量。
灵敏度,特异性和重复性:
1.灵敏度:多次重复结果表明,最小检出量为28.5pg/ml。
2.特异性:与人EGF,Epo,FGF acidic,FGF basic, GM-CSF, HGF, IFN-γ, IGF-I , IGF-II , IL-1, IL-2, IL-4, IL-6, IL-8,IL-10,IL-12,IL-13,KGF,LIF,M-CSF,MCP-1,SCF,TGF-α,TGF-β1.VEGF等没有交叉反应。
3.重复性:板内,板间变异系数均<10%.
参考文献:
1. Roberts, A.W. (2005) Growth Factors 23:33.
2. Lu, C.-Z. and B.-G. Xiao (2007) Front. Biosci. 12:2869.
3. Ward, A.C. (2007) Front. Biosci. 12:608.
4. Layton, J.E. et al. (2006) Front. Biosci. 11:3181.
5. Germeshausen, M. et al. (2008) Curr. Opin. Hematol. 15:332.
6. Liu, F. et al. (2000) Blood 95:3025.
7. Franzke, A. (2006) Cytokine Growth Factor Rev. 17:235
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验Warnings And Limitations This product is for research use only. Not intended for any animal or human therapeutic or diagnostic use unless otherwise stated. Follow appropriate laboratory guidelines. This product contains 0.02% sodium azide
RAT/MOUSE GROWTH HORMONE ELISA KIT
实验原理 This assay is a Sandwich ELISA based, sequentially, on: 1) capture of rat or mouse Growth Hormone molecules from samples to the wells of a microtiter plate coated by a pre-titered amount of anti-Growth Hormone
Isolation of c-Kit+ Human Amniotic Fluid Stem Cells from Second Trimester
to obtain c-Kit+ human AFS cells, starting from second trimester amniocentesis samples.
 技术资料
技术资料暂无技术资料 索取技术资料









