相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 保质期:
18个月
- 保存条件:
4℃
- 规格:
10片装
Omni-PAGE™Hepes-Tris Gels
本产品常温运输;4℃可保存18个月。切勿置于0℃以下,以免凝胶发生冻裂。
货号规格
| 产品编号 | 预制胶浓度 | 孔数 | 每孔最大上样量 | 规格 |
| LK201 | 8% | 10孔 | 60 μL | 10片装 |
| LK202 | 10% | 10孔 | 60 μL | 10片装 |
| LK203 | 12% | 10孔 | 60 μL | 10片装 |
| LK204 | 15% | 10孔 | 60 μL | 10片装 |
| LK205 | 4~15% | 10孔 | 60 μL | 10片装 |
| LK206 | 4~20% | 10孔 | 60 μL | 10片装 |
| LK207 | 8~20% | 10孔 | 60 μL | 10片装 |
| LK208 | 8% | 15孔 | 30 μL | 10片装 |
| LK209 | 10% | 15孔 | 30 μL | 10片装 |
| LK210 | 12% | 15孔 | 30 μL | 10片装 |
| LK211 | 15% | 15孔 | 30 μL | 10片装 |
| LK212 | 4~15% | 15孔 | 30 μL | 10片装 |
| LK213 | 4~20% | 15孔 | 30 μL | 10片装 |
| LK214 | 8~20% | 15孔 | 30 μL | 10片装 |
产品组分
| 组分名称 | 数量 |
| 预制胶 | 10片 |
| Hepes-Tris缓冲液粉剂 | 10包(500 mL) |
产品简介
goodOmni-PAGE™预制胶(Hepes-Tris)是一款安全、快捷、高性能的预制聚丙xi酰胺凝胶,常用于PAGE和Western Blot检测。本预制胶含有1.5 cm高度的4%浓缩胶。丙xi酰胺与甲叉双丙xi酰胺的比例为29:1,凝胶厚度为1.5 mm, 加样孔数为10孔/15孔,最大上样量为60 μL/30 μL,胶板尺寸:宽×高×厚度为98×84×4.1 mm;凝胶尺寸为:宽×高×厚度为81×74×1.5 mm。
产品特点
g
g
g
g
g
g
g
使用说明
good1. 请参考下面的分离谱图选择合适浓度的预制胶,以帮助您进行更好的蛋白电泳条带分离;
good2. 将Omni-PAGE™预制胶(Hepes-Tris)从包装袋中取出,固定在电泳槽中;
good3. 准备电泳缓冲液:每盒预制胶赠送10包电泳缓冲液粉末,每包粉末可用500 mL纯水进行溶解,得到500 mL 1×电泳液;
goodgood1×Hepes变性胶电泳液参考组分为:50 mM Tris,50 mM Hepes,0.1% SDS,2 mM EDTA,pH 7.8~8.0。
good4. 将电泳缓冲液注满电泳槽内槽,在外槽也加入电泳液,没过电泳槽底部的阳极即可;
good4. 注:预制胶加样孔中有残留的储存缓冲液,建议用1 mL移液枪吸取电泳液轻轻吹打加样孔,去除气泡和残留的储存缓冲液,以得到最佳电泳效果。
good5. 上样:将蛋白样品与5×蛋白上样缓冲液(货号:LT101或LT103)进行4:1混合均匀,加热处理。注意枪头不要戳破凝胶,不要过度插入梳孔使胶板变形造成漏液;
good6. 电泳条件:150 V,40~50 min,当溴酚蓝指示带电泳至胶板底部或实验预定位置时,即可结束电泳;
good7. 电泳结束,取出凝胶。用刀在侧边硅胶处,沿着两片玻璃的缝隙切开硅胶,即可打开玻璃板。取胶时,需在胶和玻璃条之间,沿着玻璃条划一刀,以防止发生粘连使胶破碎。
特别注意
good① a. 将Bio-Rad电泳槽中的U型密封条(如图绿色部分)拉出,注意这时的密封条两端是有突起的,突起的一面为正面,无突起的为反面;

good① b. 将密封条旋转180°(正面朝里,反面朝外),重新装回电泳槽中,注意把密封圈周边压实,防止发生漏液;

good① c. 放置好预制胶进行正常的电泳操作即可。
分离图谱(蛋白条带分子量单位:kDa)
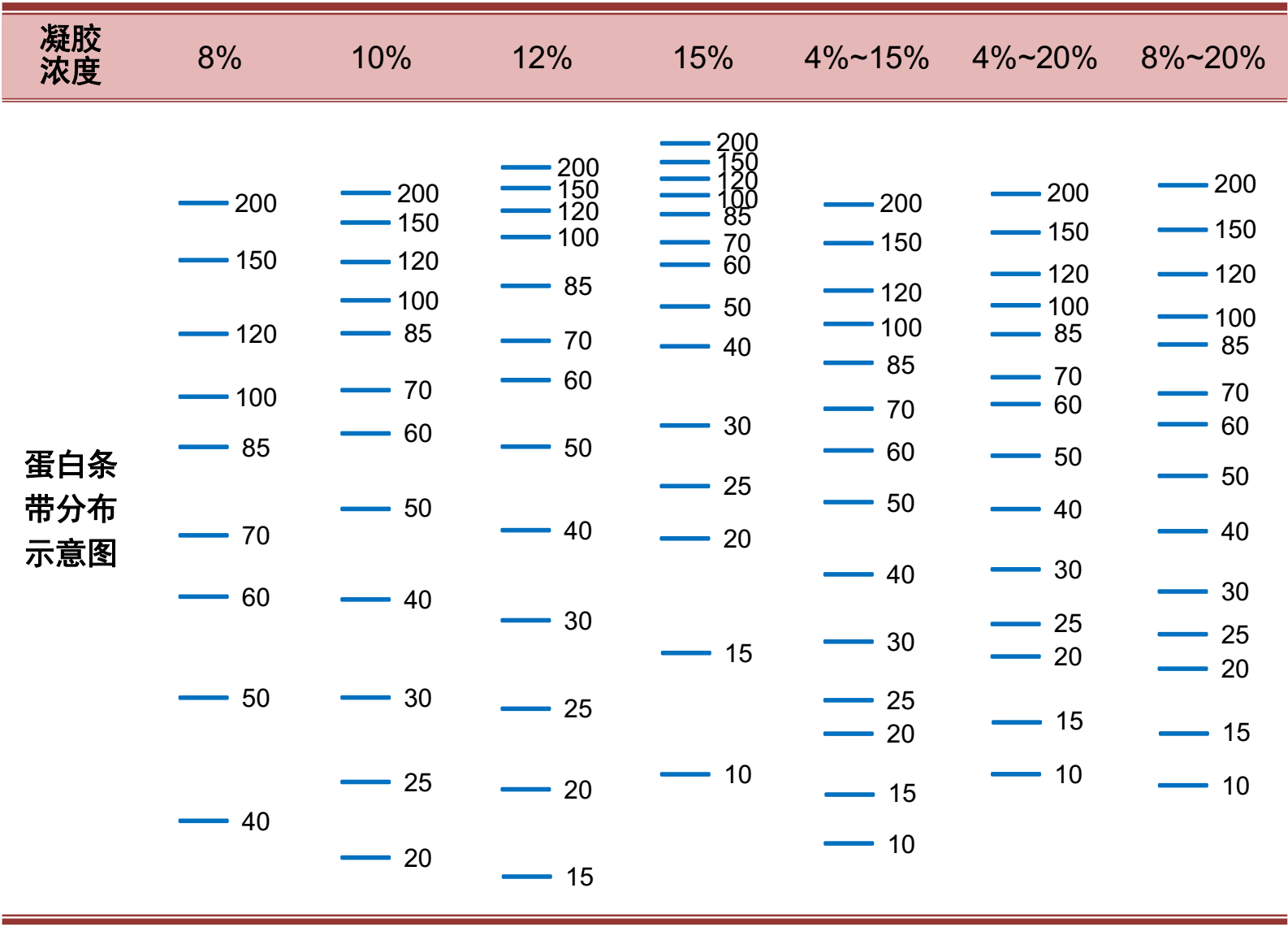
注意事项
good1. Omni-PAGE™预制胶(Hepes-Tris)使用的是中性的Hepes缓冲系统,请勿使用Tris-Glycine等其它电泳缓冲液进行电泳;
good2. 如果需要蛋白条带更加清晰、平直,可降低电压至100~120 V,适当延长电泳时间;
good3. 电泳缓冲液不建议重复使用。因为经过电泳之后,缓冲液中的离子强度、缓冲能力都发生了变化,不能确保电泳效果;
good4. 电泳结束后可以使用Tris-Glycine转膜液进行转膜。将凝胶浸泡在转膜液中10~15 min, 使凝胶中的缓冲液得到充分平衡,再进行转膜;
good5. 上样时移液器吸头不要过度插入点样孔,以免戳破凝胶造成漏液;
good6. 为了您的安全和健康,请穿实验服并戴一次性手套操作;
good7. 本产品仅限科研使用。
常见问题
good1. 蛋白电泳示踪染料溴酚蓝扭曲、电泳时间大幅度延长:
good1. ● 可能是内槽缓冲液泄漏导致。建议重新夹胶板,防止在电泳过程中内槽液面逐步降低;
good2. 使用自己配制的其它体系电泳缓冲液电泳后条带较模糊:
good1. ● 本预制胶为中性,对电泳缓冲液的要求比传统pH 8.8的分离胶要高,缓冲液配制不当,或长期放置变质, 都会对本预制胶的蛋白电泳效果产生影响;
good3. 电压为150 V电泳时,一块胶的电流在80 mA左右,2块胶的电流在140 mA左右,随着时间增加电流会逐步降低。如果电流明显不在这一范围,需检查电泳液的质量,电极是否插反及内槽电泳液是否有漏液现象;
good4. 湿转时,需120 V恒压转膜60~90 min。为达到更好的转膜效果,可以根据预制胶上残留的或膜上的预染蛋白分子量标准确定转膜效率,并对转膜条件进行适当调整。目的蛋白的分子量,凝胶浓度及转膜液中的甲醇浓度都会影响转膜效率。大蛋白尽量选择低浓度的胶。蛋白分子量100 kDa以上,建议甲醇浓度5%;10~100 kDa,建议甲醇浓度10%;10 kDa以下,建议甲醇浓度20%~30%;
good5. 电泳时泳道拖尾严重,点样孔样品滞留明显:
good1. ● 可能原因是样品处理不充分:
good1. ● a. 裂解处理不够充分。建议降低裂解前的样品浓度,或增加裂解液的比例,使样品充分裂解;
good1. ● b. 上样缓冲液处理不充分。建议对裂解后的样品进行稀释后,再进行上样缓冲液处理;
good6. 蛋白条带中间凹陷,两边突起:
good1. ● 可能原因是样品盐离子浓度或表面活性剂浓度过高。建议稀释样品或对样品进行透析后,再进行上样缓冲液处理和上样。
相关论文
good2. Ji, L., Qian, W., Gui, L., Ji, Z., Yin, P., Lin, G. N., ... & Gao, W. Q. (2020). Blockade of β-Catenin–Induced CCL28 Suppresses Gastric Cancer Progression via Inhibition of Treg Cell Infiltration. Cancer Research, 80(10), 2004-2016. (IF 12.701)
good3. LI, Jing, et al. Selenium Status in Diet Affects Acetaminophen-Induced Hepatotoxicity via Interruption of Redox Environment. Antioxidants & Redox Signaling, 2021, 34.17: 1355-1367.(IF 8.401)
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验也很贴心,针对不同的电泳槽都有详细的步骤和图示。 目前有两种梯度浓度(8-16%、4-20%)和三种固定浓度(8%、10%、12%)可供选择,规格是最常用的10孔、12孔和15 孔。10孔的上样量达50ul,几乎是其他预制胶的两倍。蛋白分离 范围请看下表,大部分蛋白都可以得到很好分离,但是如果蛋白特别大或特别小,估计就不适用了。目录价是1526元(10块),有点小贵,不过6月10日前有促销,买一送一,相当于每块76.3元。 浓度
槽都有详细的步骤和图示。 目前有两种梯度浓度(8-16%、4-20%)和三种固定浓度(8%、10%、12%)可供选择,规格是最常用的10孔、12孔和15 孔。10孔的上样量达50ul,几乎是其他预制胶的两倍。蛋白分离 范围请看下表,大部分蛋白都可以得到很好分离,但是如果蛋白特别大或特别小,估计就不适用了。目录价是1526元(10块),有点小贵。 浓度 8% 10% 12
相关专题 Mini Protean 3 Cell 小型垂直电泳简介: 凝胶数:1 或2玻板尺寸(W x L)短板10.1 x 7.3 cm间隔板10.1 x 8.2 cm凝胶大小(W x L) 手灌胶:8.3 x 7.3 cm; 预制胶: 8.6 x 6.8 cm典型上层缓冲液体积120 ml典型下层缓冲液体积180 ml典型SDS-PAGE电泳 时间45 min ( 200 V 恒压)建议电源












