相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 库存:
100
- 国食药监械注册号:
无
- 保修期:
12个月
- 现货状态:
大鼠、小鼠心率遥测系统
- 供应商:
玉研仪器公司
- 规格:
敬请来电咨询
可对大鼠、小鼠的体温、心率、活动量,进行无线式、长时间的测量和记录
植入式生理信号无线遥测系统用于长时间测量清醒无束缚的大鼠、小鼠、兔子、比格犬、猴子、鱼等多种动物的心率、体温和活动量等生理参数。使用此系统可以保证动物在笼内自由活动,不需要麻醉或束缚,这样测量到的生理信号更能反映自然状态下的动物生理状况。可用于生物节律研究和相关的生命体征监测。
植入式生理信号无线遥测系统可无线遥测和记录大鼠、小鼠的:心率、体温、活动量.
植入式生理信号无线遥测系统由植入体(E-Mitter)、接收数据转换器(Receiver)、电缆和记录分析计算机(VitalView)构成。1厘米大小的植入体E-Mitter集成了传感器、放大器和无线信号发射器,根据测量信号不同有多种规格。植入式E-Mitter转发器不需电池,由接收数据转换器(Receiver)输出电力。实验人员将植入体埋入动物皮下,生理信号被植入体采集到并转换成相应的电信号后用无线电发射出来,由饲养笼下方的接收器接收到并传递给数据转换器,完成数据转换后送入中央处理器进行数据处理。系统最多可同时连接32个接收器,完成大规模的试验。
植入体(E-Mitter)是植入在动物体内的微型设备,它集成了传感器,放大器,数字转换,无线发射的功能并解决了生物体的抗排异反应。植入体有用于测量生物心率,体温和活动量等多种参数的规格。
VitalView植入式生理信号无线遥测系统的特点:
· 无线式测量
· 植入式E-Mitter转发器没有电池
· 长期监测-植入装置后允许连续、遥测实验动物的整个生命周期
· 准确、可靠, 报告清醒无束缚动物的生理和行为数据
植入式系统 的主要技术参数:
ER4000 信号接收器
ER4000信号接收器,用于给E-Mitters充电和接收E-Mitters传回来的测量数据。适合标准的大小鼠饲养笼具。
信号接收器的主要参数
VitalView软件
激发接收器和感应器通过VitalView软件连接到电脑。最多可以记录240个数据通道,典型应用120个测试对象,对于E-mitter系统最多32个测试对象。
VitalView软件可以设置实验参数和采集数据。软件管理与硬件的连接,并且储存显示基本的图形化的数据分析。软件也提供统计形式的数据显示,可以输出数据。
Telemetry – used to monitor temperature, gross motor activity and heart rate data.
Physiological and behavioral monitoring oftransgenic mice and other laboratory animals has never been simpler. Through the use of biotelemetry and a variety of available sensors, it is possible for VitalView to monitor up to seven different physiological or behavioral parameters from a single laboratory subject
Combinations of the following parameters may be monitored for multiple laboratory subjects using VitalView:
Body Core Temperature
Heart Rate
Gross Motor Activity
Running Wheel Turns
Drinking/Licking Frequency
Feeding Behavior
Ambient Temperature
Ambient Light
E-Mitter Battery-Free Implantable Transponders
Using telemetry to provide temperature, gross motor activity and heart rate data. An E-Mitter is a small implantable transponder that is powered by capturing energy from electrical fields generated by the ER-4000 Energizer/Receiver. This allows the E-Mitter to operate without batteries and remain implanted indefinitely to monitor the subject''s temperature, activity or heart rate. As a result, high costs and downtime of explantation, refurbishment and reimplantation are avoided.
小动物心率、体温遥测系统的部分参考文献:
1.Ganeshan, Kirthana et al. “Energetic Trade-Offs and Hypometabolic States Promote Disease Tolerance.” Cell vol. 177,2 (2019): 399-413.e12. doi:10.1016/j.cell.2019.01.050
2.Li, Yongguo et al. “Secretin-Activated Brown Fat Mediates Prandial Thermogenesis to Induce Satiation.” Cell vol. 175,6 (2018): 1561-1574.e12. doi:10.1016/j.cell.2018.10.016
3.Dodd, Garron T et al. “Leptin and insulin act on POMC neurons to promote the browning of white fat.” Cell vol. 160,1-2 (2015): 88-104. doi:10.1016/j.cell.2014.12.022
4.Piñol, Ramón A et al. “Brs3 neurons in the mouse dorsomedial hypothalamus regulate body temperature, energy expenditure, and heart rate, but not food intake.” Nature neuroscience vol. 21,11 (2018): 1530-1540. doi:10.1038/s41593-018-0249-3
5.Li, Jin et al. “Neurotensin is an anti-thermogenic peptide produced by lymphatic endothelial cells.” Cell metabolism vol. 33,7 (2021): 1449-1465.e6. doi:10.1016/j.cmet.2021.04.019
6.Piñol, Ramón A et al. “Preoptic BRS3 neurons increase body temperature and heart rate via multiple pathways.” Cell metabolism vol. 33,7 (2021): 1389-1403.e6. doi:10.1016/j.cmet.2021.05.001
7.Krisko, Tibor I et al. “Dissociation of Adaptive Thermogenesis from Glucose Homeostasis in Microbiome-Deficient Mice.” Cell metabolism vol. 31,3 (2020): 592-604.e9. doi:10.1016/j.cmet.2020.01.012
8.Sustarsic, Elahu G et al. “Cardiolipin Synthesis in Brown and Beige Fat Mitochondria Is Essential for Systemic Energy Homeostasis.” Cell metabolism vol. 28,1 (2018): 159-174.e11. doi:10.1016/j.cmet.2018.05.003
9.Heine, Markus et al. “Lipolysis Triggers a Systemic Insulin Response Essential for Efficient Energy Replenishment of Activated Brown Adipose Tissue in Mice.” Cell metabolism vol. 28,4 (2018): 644-655.e4. doi:10.1016/j.cmet.2018.06.020
10.Dodd, Garron T et al. “A Hypothalamic Phosphatase Switch Coordinates Energy Expenditure with Feeding.” Cell metabolism vol. 26,2 (2017): 375-393.e7. doi:10.1016/j.cmet.2017.07.013
11.Keipert, Susanne et al. “Long-Term Cold Adaptation Does Not Require FGF21 or UCP1.” Cell metabolism vol. 26,2 (2017): 437-446.e5. doi:10.1016/j.cmet.2017.07.016
12.Wang, Tongfei A et al. “Thermoregulation via Temperature-Dependent PGD2 Production in Mouse Preoptic Area.” Neuron vol. 103,2 (2019): 309-322.e7. doi:10.1016/j.neuron.2019.04.035
13.Chavan, Rohit et al. “Liver-derived ketone bodies are necessary for food anticipation.” Nature communications vol. 7 10580. 3 Feb. 2016, doi:10.1038/ncomms10580
14.Jiang, Lin et al. “Leptin receptor-expressing neuron Sh2b1 supports sympathetic nervous system and protects against obesity and metabolic disease.” Nature communications vol. 11,1 1517. 23 Mar. 2020, doi:10.1038/s41467-020-15328-3
15.Walker, William H 2nd et al. “Acute exposure to low-level light at night is sufficient to induce neurological changes and depressive-like behavior.” Molecular psychiatry vol. 25,5 (2020): 1080-1093. doi:10.1038/s41380-019-0430-4
16.Zhang, Xue-Ying et al. “Huddling remodels gut microbiota to reduce energy requirements in a small mammal species during cold exposure.” Microbiome vol. 6,1 103. 8 Jun. 2018, doi:10.1186/s40168-018-0473-9
17.Ingiosi, Ashley M et al. “A Role for Astroglial Calcium in Mammalian Sleep and Sleep Regulation.” Current biology : CB vol. 30,22 (2020): 4373-4383.e7. doi:10.1016/j.cub.2020.08.052
18.Padilla, Stephanie L et al. “Kisspeptin Neurons in the Arcuate Nucleus of the Hypothalamus Orchestrate Circadian Rhythms and Metabolism.” Current biology : CB vol. 29,4 (2019): 592-604.e4. doi:10.1016/j.cub.2019.01.022
如只需要测量大鼠、小鼠的核心体温,可以选择植入式体温胶囊,对体温数据进行遥测:
体温测量胶囊是一款可连续监测、记录并无线传输核心体温信号的微型胶囊。大动物可其经口腔摄入进入体内,通过胃、肠道,最后由肛门排出;小动物可进行皮下植入。
使用简单方便,广泛用于多种科研领域。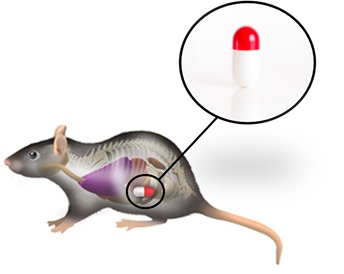
适用于多种动物,如:大鼠、小鼠、比格犬、兔子等。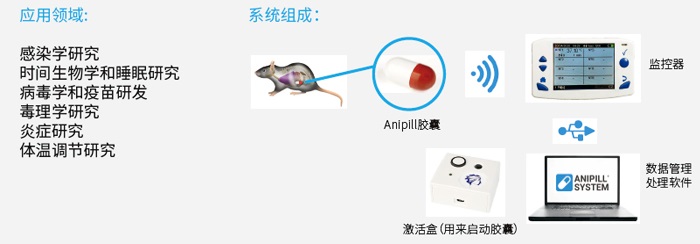
体温胶囊的主要特点:
体积小巧,食用方便,对机体无损害;
实时连续无创监测;
无线无导管测量,测试对象亦无需实时佩戴监测器,实现无任何限制测量方案;
胶囊内置存储记忆功能,可存储多达2000组数据,无需担心数据丢失;
监测器可同时监测3枚胶囊数据,且自身可最多7台并联,实现高通量测量;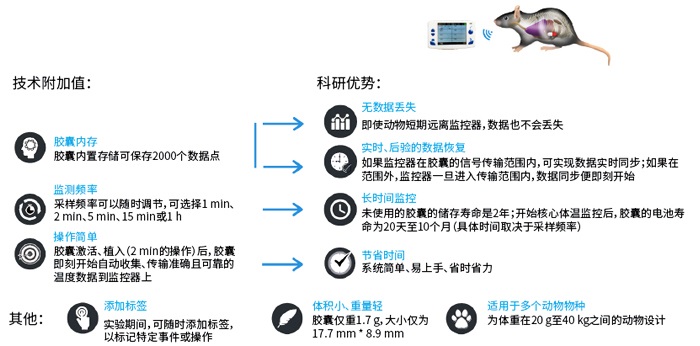
主要技术参数:
测量参数:使用温度25-45℃,精确度0.2℃,采样频率30Hz(可设定),内部可存储2000组数据;
传输参数:传输距离1-3m,传输频率433Hz;
规格参数:17.7*8.9mm,重1.7g;
可同时监测并显示3只动物体内胶囊的传输,并可通过PC/MAC观察分析;
每台监测器可存储80000组数据;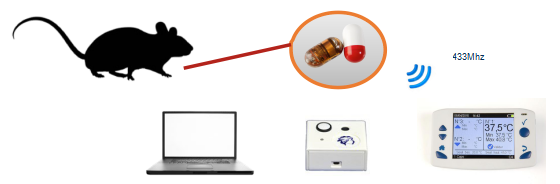
小动物体温测量胶囊的相关文献:
1.van der Vinne V, Pothecary C A, Wilcox S L, et al. Continuous and non-invasive thermography of mouse skin accurately describes core body temperature patterns, but not absolute core temperature[J]. Scientific Reports, 2020, 10(1): 20680.
2.Delezie J, Gill J F, Santos G, et al. PGC-1β-expressing POMC neurons mediate the effect of leptin on thermoregulation in the mouse[J]. Scientific Reports, 2020, 10(1): 1-12.
3.van der Vinne V, Tachinardi P, Riede S J, et al. Maximising survival by shifting the daily timing of activity[J]. Ecology letters, 2019, 22(12): 2097-2102.
4.Hong S H, Hong J H, Lahey M T, et al. A low-cost mouse cage warming system provides improved intra-ischemic and post-ischemic body temperature control–application for reducing variability in experimental stroke studies[J]. Journal of neuroscience methods, 2021, 360: 109228.
5.Belloch F B, Beltrán E, Venzala E, et al. Primary role for melatonin MT2 receptors in the regulation of anhedonia and circadian temperature rhythm[J]. European Neuropsychopharmacology, 2021, 44: 51-65.
6.Tabarean I V. Neurotensin induces hypothermia by activating both neuronal neurotensin receptor 1 and astrocytic neurotensin receptor 2 in the median preoptic nucleus[J]. Neuropharmacology, 2020, 171: 108069.
7.Fenzl A, Kulterer O C, Spirk K, et al. Intact vitamin A transport is critical for cold-mediated adipose tissue browning and thermogenesis[J]. Molecular metabolism, 2020, 42: 101088.
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验小动物心率、体温遥测系统的部分参考文献:
1.Ganeshan, Kirthana et al. “Energetic Trade-Offs and Hypometabolic States Promote Disease Tolerance.” Cell vol. 177,2 (2019): 399-413.e12. doi:10.1016/j.cell.2019.01.050
2.Li, Yongguo et al. “Secretin-Activated Brown Fat Mediates Prandial Thermogenesis to Induce Satiation.” Cell vol. 175,6 (2018): 1561-1574.e12. doi:10.1016/j.cell.2018.10.016
3.Dodd, Garron T et al. “Leptin and insulin act on POMC neurons to promote the browning of white fat.” Cell vol. 160,1-2 (2015): 88-104. doi:10.1016/j.cell.2014.12.022
4.Piñol, Ramón A et al. “Brs3 neurons in the mouse dorsomedial hypothalamus regulate body temperature, energy expenditure, and heart rate, but not food intake.” Nature neuroscience vol. 21,11 (2018): 1530-1540. doi:10.1038/s41593-018-0249-3
5.Li, Jin et al. “Neurotensin is an anti-thermogenic peptide produced by lymphatic endothelial cells.” Cell metabolism vol. 33,7 (2021): 1449-1465.e6. doi:10.1016/j.cmet.2021.04.019
6.Piñol, Ramón A et al. “Preoptic BRS3 neurons increase body temperature and heart rate via multiple pathways.” Cell metabolism vol. 33,7 (2021): 1389-1403.e6. doi:10.1016/j.cmet.2021.05.001
7.Krisko, Tibor I et al. “Dissociation of Adaptive Thermogenesis from Glucose Homeostasis in Microbiome-Deficient Mice.” Cell metabolism vol. 31,3 (2020): 592-604.e9. doi:10.1016/j.cmet.2020.01.012
8.Sustarsic, Elahu G et al. “Cardiolipin Synthesis in Brown and Beige Fat Mitochondria Is Essential for Systemic Energy Homeostasis.” Cell metabolism vol. 28,1 (2018): 159-174.e11. doi:10.1016/j.cmet.2018.05.003
厂家:瑞沃德公司),供脑切片染色。1.3.7其他辅助设备和耗材(生产厂家:瑞沃德公司)2.实验方法STEP1:动物麻醉和头部固定:动物经麻醉机诱导进入麻醉,移到定位仪装置进行头部固定和麻醉维持,稳定一会后,使用镊子夹足,测试麻醉的深度,当呼吸平缓,无压足缩回反应时,说明进入实验麻醉中期。另外开启体温维持仪进行实验期动物体温的维持(如图 1)。STEP2:左股静脉暴露和空心与孟加拉玫瑰聚乙烯导管输液,导管用线进行固定(如图 2)。STEP3:纵向切开头皮(2.0-2.5 厘米)以暴露头骨。为了避免伤口并发
注入溶液的体积。 4. 作慢性实验时,在寒冷冬季,麻醉剂在注射前应加热至动物体温水平。 四、实验动物用药量的确定及计算方法 (一)动物给药量的确定 观察一种药物对实验动物的作用时,一个重要的问题就是给动物用多大的剂量较合适。剂量太小,作用不明显,剂量太大,又可能引起动物中毒致死。可以按下述方法确定剂量: 1. 先用少量小鼠粗略地探索中毒剂量或致死剂量,然后用小于中毒量的剂量,或取致死量的若干分之一作为应用剂量,一般可取1/10~1/5。 2. 植物药粗制剂的剂量多按生药折算
 技术资料
技术资料










