相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 询价记录
- 文献和实验
- 技术资料
- 库存:
100
- 国食药监械注册号:
无
- 保修期:
12个月
- 现货状态:
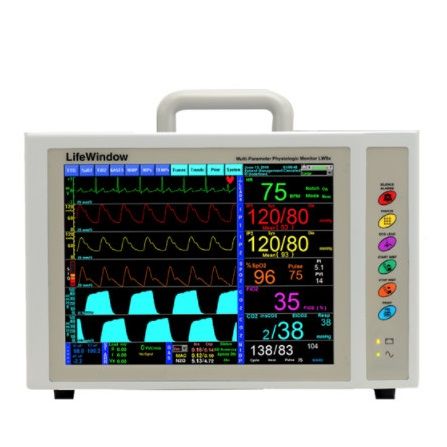
动物手术监护仪(心电、血氧、体温)
- 供应商:
玉研仪器公司
- 规格:
敬请来电咨询

大鼠、小鼠心电监护仪非常适合对大鼠、小鼠等小动物进行心电、血压、脉搏、血氧、呼吸、心率、体温等方面的检测,非常适合对术中的大小鼠等动物进行各项生理指标的监护。
主要特点:
· 适用于从小鼠、大鼠等啮齿类动物的生命体征监护;
· 可选择的检测模块:3导联心电,5导联心电,呼吸,SpO2,FiO2,CO2 DualCap,CO2 Side-Stream,
· CO2Main-Stream,NIBP,IPs,Temperatures,Recorder 等等;
· 高清晰8.4英寸薄膜电晶体液晶显示器,触屏操作,结构紧凑;
· 有线、无线网络条件下都可操作;
· 数据稳定,可靠,可信
· 波形扫描速度范围:6.25mm/s ~ 50mm/s;
· 自动检测心律失常,测 ST 段的变化;
· 屏幕可同时显示6条心电向量图;
· 铝材质坚固,耐冲击,减少电磁干扰;
· 可选打印机,兼容任何计算机,可作图表,打印机可以直接连接监护仪,或通过网络连接,以PDF 格式打印;

型号:LW9x
主要功能特点:
· 4道波形,10.4" 彩色灵敏TFT显示器;
· 简易的操作界面;
· 屏幕上显示所有监护参数的趋势图;
· 精密细致,方便携带,重量不超过12磅;
· SpO2采用数字式和自动匹配技术(SAC)
· 附带标准配件,方便仪器使用;
· 精密细致,大屏幕显示,操作方便;
· 数据稳定,可靠,可信;
· 多种功能模块可供选择:心电(3导联,5导联可选),血氧饱和度,有创血压,无创血压,心率,呼吸,呼吸末CO2,体温等;

动物监护仪,也叫做多参数动物生命体征监护仪,可用来监测不同的生理参数,如心电(3导联,5导联可选),血氧饱和度,有创血压,无创血压,心率,呼吸,呼吸末CO2,体温等数据。
适用的动物:
小鼠、大鼠、兔子、猴子、比格犬等多种实验动物;
开放式模块选择:
有多种配置方案可供选择,敬请来电咨询;
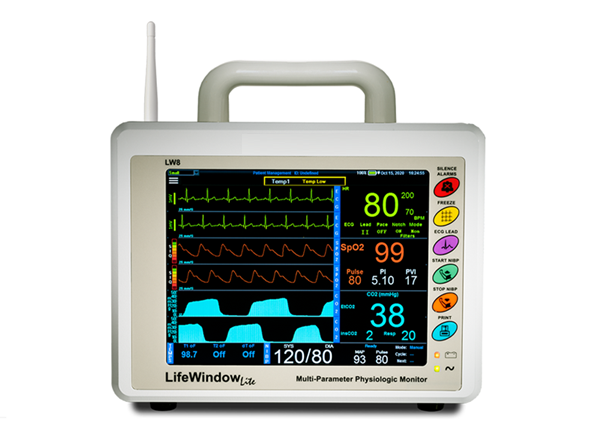
型号:LW8x
无线测量装置
可搭配遥测装置,实现对多只实验动物的无线心电数据测量和记录:
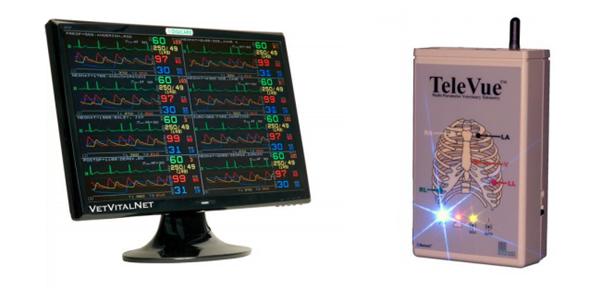
便携式动物监护仪
根据所需要参数,有十多种参数和配置可供选择:

如果需要测量大鼠、小鼠的脉搏、血氧、呼吸、体温等参数,可以选择MouseOx动物无创监护仪
MouseOx® Plus pulse oximeter以无创的方式测量小动物(幼鼠监护仪,小鼠监护仪,大鼠监护仪,豚鼠监护仪,兔监护仪, 等)的血氧饱和度,脉搏频率,动物体温,呼吸频率,脉搏幅度,呼吸幅度。所有测量都是通过一个无创的感应器。

主要应用:
• 动脉氧气饱和度,心率,呼吸率,脉搏舒张,呼吸舒张等参数的测量
• 动物麻醉状态、外科手术过程中作为监视设备
• 用于心肺功能的评价,连续监测心肺功能(心率在90-900 bpm),可作为心肺数据记录仪使用
• 新生动物体征的监测
• 肺损伤的研究,机械人工呼吸救助装置
• 休克动物模型的研究
• 中风和脑损伤的研究
• 转化型医学的研究
• 缺氧及吸入性实验的研究
• 确保动物处于适当的麻醉深度,预防手术中缺氧
如果需要对小鼠心率进行检测,可以选择小鼠心率遥测系统:
小鼠心率遥测系统
(植入式生理信号无线遥测系统)用于长时间测量清醒无束缚的大鼠、小鼠、兔子、比格犬、猴子、鱼类等多种动物的心率、体温 和 活动量等生理参数
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
- 作者
- 内容
- 询问日期
 文献和实验
文献和实验1.Suzuki R, Yamasoba D, Kimura I, et al. Attenuated fusogenicity and pathogenicity of SARS-CoV-2 Omicron variant[J]. Nature, 2022, 603(7902): 700-705.
2.Wang G, Wen B, Deng Z, et al. Endothelial progenitor cells stimulate neonatal lung angiogenesis through FOXF1-mediated activation of BMP9/ACVRL1 signaling[J]. Nature communications, 2022, 13(1): 1-16.
3.Aiba I, Noebels J L. Kcnq2/Kv7. 2 controls the threshold and bi-hemispheric symmetry of cortical spreading depolarization[J]. Brain, 2021, 144(9): 2863-2878.
4.Bachus H, Kaur K, Papillion A M, et al. Impaired tumor-necrosis-factor-α-driven dendritic cell activation limits lipopolysaccharide-induced protection from allergic inflammation in infants[J]. Immunity, 2019, 50(1): 225-240. e4.
5.Han W, Tellez L A, Perkins M H, et al. A neural circuit for gut-induced reward[J]. Cell, 2018, 175(3): 665-678. e23.
6.Lai A Y, Dorr A, Thomason L A M, et al. Venular degeneration leads to vascular dysfunction in a transgenic model of Alzheimer’s disease[J]. Brain, 2015, 138(4): 1046-1058.
7.Thomas G M, Carbo C, Curtis B R, et al. Extracellular DNA traps are associated with the pathogenesis of TRALI in humans and mice[J]. Blood, The Journal of the American Society of Hematology, 2012, 119(26): 6335-6343.
8.Dorr A, Sahota B, Chinta L V, et al. Amyloid-β-dependent compromise of microvascular structure and function in a model of Alzheimer’s disease[J]. Brain, 2012, 135(10): 3039-3050.
9.Abt M C, Osborne L C, Monticelli L A, et al. Commensal bacteria calibrate the activation threshold of innate antiviral immunity[J]. Immunity, 2012, 37(1): 158-170.
Fung Y L, Kim M, Tabuchi A, et al. Recipient T lymphocytes modulate the severity of antibody-mediated transfusion-related acute lung injury[J]. Blood, The Journal of the American Society of Hematology, 2010, 116(16): 3073-3079.
了I/R损伤概念:当组织细胞低灌流缺血后获得血液在供应时,不但未使组织细胞缺血性损害减轻或恢复后,反而加重了缺血性损伤。探索如何减少心肌I/R损伤具有重要的临床意义。 1、模型种类: 大、小鼠、心肌缺血再灌注 2、实验动物: C57BL/6J小鼠 ,雄性, 体重:22g±2g, 周龄:6-8周, 动物等级:SPF级 3、手术方法: 动物深度麻醉,确认麻醉状态后,备皮,安装好心电监护仪,消毒局部皮肤,铺洞巾后剪开肋间皮肤,钝性分离肌肉、打开
、缺点】: 美国MATRX系列动物麻醉呼吸设备是专业为动物设计的,适合大小不同的动物,输出准确,精确控制动物的呼吸麻醉,具有多项专利的安全保护设计,确保动物的安全,操作更加便捷,适用于不同实验室、动物手术室以及不同专业的实验操作人员。国宝熊猫使用的动物麻醉设备。 专业密闭呼吸回路设计,提供稳定的气体麻醉,节省麻醉气体消耗,保证实验室环境的清洁。 精确的氧气流量计,输出稳定,带有快速充氧功能。
合理的专业医疗团队。作为技术力量雄厚的现代化部队门诊部,浙江省军区门诊部先后斥巨资从美国、德国等国家引进了WOLF牌腹腔镜、多功能心电监护仪、美国纽邦breeze/e1500呼吸机、海申诗达大型男科诊疗设备。 现代医学的发展日新月异,浙江省军区门诊部泌尿外科依托总院强大的技术背景,以及便捷的信息交流渠道,时刻洞察泌尿外科国内国际前沿医疗动态,针对男性疾病的复杂多样和泌尿外科的发展攻关方向,先后引进了沃尔曼强能治疗系统、GS显微早泄神经抑制术、海申诗达康复系统、中式DS包皮微整形
 技术资料
技术资料