相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 库存:
617
- 保质期:
长期
- 供应商:
北京百奥莱博科技有限公司
特别声明:本产品及我公司所售其他产品均为科研类试剂产品,严禁用于药物、医疗及其他非科研用途。
北京百奥莱博致力于最快速、最有效的检测产品,包括北京口蹄疫病毒荧光PCR检测试剂盒(FMDV)厂商在内的动物疫病PCR检测试剂盒产品是我公司倾力打造的优势产品,欢迎选购。
名称:北京口蹄疫病毒荧光PCR检测试剂盒(FMDV)厂商
等级:科研试剂
规格:48次/盒|96次/盒
产地:国产|进口
品牌:百奥莱博
一、简介:
口蹄疫病毒实时荧光qRT-PCR检测操作说明书是按照参照OIE《Manual of Diagnostic Tests and Vaccines for Terrestrial Animals 2009》国际标准和《中国国家标准口蹄疫病毒荧光RT-PCR检测方法》(GB22915-2008)而制备的商业化检测试剂盒。试剂盒的探针报告基团为6-FAM,能对样品中口蹄疫病毒进行快速检测,具有特异性高、敏感性强和操作简便的特点。
二、用途:
本试剂盒适用于检测发病动物血清、水泡液、淋巴结等标本以及细胞培养液中所有血清型(包括A、O、C、南非1、南非2、南非3和亚洲1型)口蹄疫病毒(FMDV)RNA;适用于口蹄疫病毒感染的辅助诊断、监测及流行病学调查,其检测结果仅供参考。
三、试剂盒组成:(40T/Kit)
组份 数量 规格
荧光qRT-PCR反应液(FMDV-qRT-PCR MIX) 1管 560μL/管
酶混合物(Enzymes MIX) 1管 40μL/管
无核酸酶水(Nuclease-Free Water) 1管 500μL/管
阴性对照(NTC) 1 管 50μL/管
阳性对照(FMDV-PTC) 1 管 50μL/管
四、储存条件及有效期:
本试剂盒于-18℃以下保存,有效期为6个月。
五、荧光PCR仪器适用范围:
ABI系列,Roche系列等荧光定量PCR检测仪等。
六、样品的采集与RNA提取
6.1 样品的采集
(1) 猪病料:剪取50-100mg猪病料,加入装有500 µl PBS或生理盐水的研钵中缓慢研成匀浆,取匀浆液转移到无RNA酶污染的离心管中,6000rpm离心20sec;取上清备用。
(2) 动物血清、水泡液、淋巴结等标本以及细胞培养液:取样本至无RNA酶污染的离心管中备用。
6.2 样品RNA提取
可按常规方法提取,也可采用商品化试剂盒提取病毒RNA。
(1) 取灭菌的1.5 mL Eppendorf离心管,做好标识。
(2) 每管加入600 µL裂解液,分别加入被检样本200 µL,再加入200 µL*仿,混匀器上振荡混匀5 s,于4℃ 12000 r离心15 min。
(3) 取无RNA酶的1.5 mL Eppendorf离心管,加入-20℃预冷400µL异丙醇,吸取步骤(2)各管中的上清液转移至相应的管中,避免吸出中间层,颠倒混匀。
(4) 于4℃ 12000 r离心15 min,弃上清,倒置于吸水纸上,沾干液体;加入600µL 75%预冷乙醇,洗涤。
(5) 于4℃ 12000 r离心10 min,弃上清,倒置于吸水纸上,沾干液体。
(6) 10000 r离心10 s,用微量加样器将其吸干,室温干燥5 min~10 min。
(7) 加入10µL 无核酸降解酶的水,溶解管底的RNA,5000 r离心5 s,冰上保存备用。若需长期保存须放置-70℃ 冰箱。
注:阳性对照和阴性对照为已经抽提好的核酸(无需提取),直接取5µL加入到反应体系中即可。由于阳性对照浓度较高,建议最后在样品制备区域加入阳性对照。
七、检测步骤:
7.1 试剂的准备
从试剂盒中取出荧光qRT-PCR反应液(FMDV-qRT-PCR MIX)、酶混合物(Enzymes MIX),冰上融化并振荡混匀后,10000rpm离心10s。
设所需要的PCR反应管管数为N(N=样本数+1管阴性对照+1管阳性对照),每个测试反应体系配制如下表:
试剂 每个反应加入的量 N个反应加入的量
荧光PCR反应液 14µL N×14µL
酶混合物 1 µL N×1 µL
总量 15 µL N×15µL
计算好各试剂的使用量,加入一适当体积洁净离心管中,充分混匀,10000r离心10s,向设定的N个PCR反应管中分别加入15μL,向每管中加入处理后样品或阴性对照(NTC)和阳性对照(FMDV-PTC)5μL,10000rpm瞬时离心10秒。
7.2 real time RT-PCR反应条件
将各反应管放入定量PCR仪器的反应槽内。
推荐循环条件:
反转录(Reverse Transcription) 1循环 45℃ for 5 min
预变性 1循环 94℃ for 30 sec
PCR扩增(PCR amplification ) 40循环 94℃ for 5 sec
60℃ for 30 sec
在60℃延伸时收集荧光信号。报告基团:设置为FAM。
八、结果分析:
8.1 结果分析条件设定
直接读取检测结果。基线和阈值设定原则根据仪器噪声情况进行调整,以阈值线刚好超过正常阴性样品扩增曲线的最高点为准。
8.2 试验成立判定
(1) 阴性对照(NTC):不应产生任何的扩增曲线。
(2) 阳性对照(FMDV-PTC):均产生扩增曲线。
(3) 以上条件应同时满足,否则,此次试验视为无效。
8.3 结果判定
(1) 在试验成立的条件下,Ct值≤35的样本为阳性,表明FMDV核酸阳性。
(2) Ct值显示为无的样本为阴性样本,表明FMDV核酸阴性。
(3) 如果35<Ct值≤40,判为可疑样品。对于可疑样品,先看扩增曲线。如果扩增曲线为对数扩增曲线,则为可疑阳性,否则判为阴性。
(4) 对于可疑阳性样品,重新抽提核酸,再次进行FMDV qRT-PCR检测。如果重复扩增曲线为对数扩增曲线,判为样本阳性,表明FMDV核酸阳性;否则判为样本阴性。
九、注意事项:
(1) 初次使用前请仔细阅读说明书。并严格按照说明书步骤操作。
(2) 所有使用的离心管最好高压灭菌,而且必须不含RNA酶。
(3) PCR操作应严格按照要求分区(试剂配制区、标本处理区、PCR扩增区等),防止实验室污染。
(4) 样本提取、试剂配置、加样需在不同区的超净工作台进行,以免污染。
(5) 试剂盒里所有物品应视为污染物对待,并按照卫生部《微生物生物医学实验室生物安全通则》进行处理。
北京口蹄疫病毒荧光PCR检测试剂盒(FMDV)厂商正在火爆热销,除此之外,为您推荐下别热销产品:
·人副流感病毒2型/4型双重荧光PCR检测试剂盒
编号:SYA188
等级:科研实验专用
规格:48次/盒
一、简介:
本试剂盒用一对人副流感病毒2 型特异性引物,一对人副流感病毒4 型特异性引物,分别结合一条特异性荧光探针,用一步法双重荧光RT-PCR 技术对人副流感病毒2 型/4 型RNA 进行体外扩增检测,用于临床上对可疑感染者的病原学诊断。本试剂盒中人副流感病毒2 型的探针报告基团为FAM,人副流感病毒4 型的探针报告基团为VIC/HEX/JOE。
二、用途:
本试剂盒适用于各种咽拭子、鼻拭子样品等临床样品中人副流感病毒2型/4型的特异性检测。适用于人副流感病毒2型/4型感染的辅助诊断、监测及流行病学调查,其检测结果仅供临床参考。
三、试剂盒组成:(48T)
组份 数量 规格
人副流感2型/4型反应液(PIV2/PIV4-qRT-PCR MIX) 1管 576μL/管
qRT 酶混合物(qRT Enzymes MIX) 1管 192μL/管
无核酸酶水(Nuclease-Free Water) 1管 500μL/管
阴性对照(NTC) 1管 50μL/管
人副流感2 型/4 型阳性对照(PIV2/PIV4-PTC) 1管 50μL/管
四、储存条件及有效期:
本试剂盒于-20℃以下保存,有效期为6个月。
五、荧光PCR仪器适用范围:
ABI系列,Roche系列等荧光定量PCR检测仪等。
六、样品的采集与RNA提取
6.1 样品的采集
按照相关标准采集。标本短期内可保存于-20℃,长期保存可置-80℃,但不能超过6个月,标本运送应采用0℃冰壶。
6.1.1 血清:用一次性无菌注射器抽取静脉血2mL,注入无菌的干燥玻璃管,室温(22-25℃)放置30-60min,血标本可自发完成凝集析出血清,或直接使用水平离心机,3000rpm离心5min,吸取上层血清,转移至1.5mL灭菌离心管。
6.1.2 血浆:用一次性无菌注射器抽取静脉血2mL,注入含EDTA2Na(乙二*(代"胺")四乙酸二*)或柠檬酸*抗凝剂的玻璃管,立即轻轻颠倒玻璃管混合5-10次,使抗凝剂与静脉血充分混匀,5-10min后即可分离出血浆,转移至1.5mL灭菌离心管。
6.1.3 拭子、分泌物等样品:在装有拭子或分泌物的离心管中加入500μL PBS或生理盐水,剧烈振荡30s。棉拭子尽量挤出液体转移到无RNA酶污染的离心管中,6000rpm离心20s,取上清备用。
6.1.4 病灶组织样品:称取组织约0.1g于研磨器或组织匀浆器中研磨(最好置于冰上或加入液氮),再加1mL生理盐水研磨至无块状物,然后将样品转至1.5mL灭菌离心管中,8000rpm离心2min,取上清液于1.5mL灭菌离心管中。
6.2 RNA提取
可采购北京百奥莱博科技有限公司生产的RNA提取试剂盒(过柱法-荧光配套)或其他合适的商业化产品,并按照相应试剂盒说明进行操作。
注:阳性对照和阴性对照为已经抽提好的核酸(无需提取),直接取4μL 加入到反应体系中即可。由于阳性对照浓度较高,建议最后在样品制备区域加入阳性对照。
七、检测步骤:
7.1 试剂的准备
从试剂盒中取出荧光qRT-PCR 反应液(PIV2/PIV4-qRT-PCR MIX)、酶混合物(Enzymes MIX),冰上融化并振荡混匀后,10000rpm 离心10s。
设所需要的PCR 反应管管数为N(N=样本数+1 管阴性对照+1 管阳性对照),每个测试反应体系配制如下表:
试剂 每个反应加入的量 N个反应加入的量
荧光PCR反应液 12µL N×12µL
酶混合物 4µL N×4µL
总量 16µL N×16µL
计算好各试剂的使用量,加入一适当体积洁净离心管中,充分混匀,10000rpm 离心10s,向设定的N 个PCR 反应管中分别加入16μL,向每管中加入处理后样品/阴性对照(NTC)/阳性对照(PIV2/PIV4-PTC)4μL,10000rpm 瞬时离心10 秒。
7.2 qRT-PCR反应条件
将各反应管放入实时荧光PCR仪器的反应槽内。
推荐循环条件:
反转录(Reverse Transcription) 1循环 50℃ for 30 min
预变性 1循环 95℃ for 5 min
PCR扩增 40循环 95℃ for 10 sec
55℃ for 45 sec
在60℃延伸时收集荧光信号。报告基团:设置为FAM和VIC(若仪器无VIC通道,可选择HEX或JOE通道)。其中FAM基团检测PIV2,VIC/HEX/JOE基团检测PIV4。淬灭基团:NONE,请勿选择ROX参比荧光。
八、结果分析:
8.1 结果分析条件设定
直接读取检测结果。基线和阈值设定原则根据仪器噪声情况进行调整,以阈值线刚好超过正常阴性样品扩增曲线的最高点为准。
8.2 试验成立判定
(1) 阴性对照(NTC):FAM和VIC/HEX/JOE通道均无扩增。
(2) 阳性对照(PIV2/PIV4-PTC):FAM和VIC/HEX/JOE通道均有扩增。
以上条件应同时满足,否则,此次试验视为无效
8.3 结果判定
(1) FAM通道:Ct值≤35 PIV2核酸为阳性;Ct值显示为无的样本为阴性样本,表明PIV2核酸阴性。Ct值在35-40个循环之间,为灰区,需要进行重复试验。如果重复扩增曲线为对数扩增曲线,判为样本阳性,表明PIV2核酸阳性;否则判为样本阴性。
(2) VIC/HEX/JOE通道:Ct值≤35 PIV4核酸为阳性;Ct值显示为无的样本为阴性样本,表明PIV4核酸阴性。Ct值在35-40个循环之间,为灰区,需要进行重复试验。如果重复扩增曲线为对数扩增曲线,判为样本阳性,表明PIV4核酸阳性;否则判为样本阴性。
九、注意事项:
(1) 初次使用前请仔细阅读说明书。并严格按照说明书步骤操作。
(2) 所有使用的离心管最好高压灭菌,而且必须不含RNA 酶。
(3) PCR 操作应严格按照要求分区(试剂配制区、标本处理区、PCR 扩增区等),防止实验室污染。
(4) 样本提取、试剂配置、加样需在不同区的超净工作台进行,以免污染。
(5) 试剂盒里所有物品应视为污染物对待,并按照卫生部《微生物生物医学实验室生物安全通则》进行处理。
北京口蹄疫病毒荧光PCR检测试剂盒(FMDV)厂商关键词:百奥莱博,口蹄疫病毒荧光PCR检测试剂盒(FMDV),SYA401
·副猪嗜血杆菌(HPS)单重凝胶PCR检测试剂盒
编号:SYA570
等级:科研实验专用
规格:48次/盒
一、简介:
本试剂盒用一对副猪嗜血杆菌特异性引物,对副猪嗜血杆菌DNA进行体外扩增检测,用于临床上对可疑感染者的病原学诊断。
二、用途:
该试剂盒适合于发病猪呼吸道、血液样本中副猪嗜血杆菌(HPS)的特异性检测,用于副猪嗜血杆菌(HPS)的辅助诊断,其检测结果仅供临床参考。
三、试剂盒组成:(48T)
| 组份 | 数量 | 规格 |
| 副猪嗜血杆菌PCR反应液(HPS-PCR MIX) | 1管 | 720μL/管 |
| DNA抽提液(DNA Extraction) | 2管 | 1.5mL/管 |
| 阴性对照(NTC) | 1管 | 50μL/管 |
| 阳性对照(HPS-PTC) | 1管 | 50μL/管 |
四、储存条件及有效期:
本试剂盒于-20℃以下保存,有效期为6个月。
五、PCR仪器适用范围
ABI系列,Roche系列等PCR检测仪等。
六、样品的采集与DNA提取
6.1 样品的采集
6.1.1 血清:用一次性无菌注射器抽取静脉血2mL,注入无菌的干燥玻璃管,室温(22-25℃)放置30-60min,血标本可自发完成凝集析出血清,或直接使用水平离
心机,3000rpm离心5min,吸取上层血清,转移至1.5mL灭菌离心管。
6.1.2 血浆:用一次性无菌注射器抽取静脉血2mL,注入含EDTA2Na(乙二*(代"胺")四乙酸二*)或柠檬酸*抗凝剂的玻璃管,立即轻轻颠倒玻璃管混合5-10次,使抗凝剂
与静脉血充分混匀,5-10min后即可分离出血浆,转移至1.5mL灭菌离心管。
6.1.3 粪便样品:取粪便置于灭菌的收集管中送检。
6.1.4 病灶部位样品:取发病部位新鲜渗出物、粘液脓血送检。
注:上述样品建议经过增菌后,收集培养物用于检测。
6.2DNA提取
可采用PCR试剂盒配备的DNA抽提液,按以下说明进行DNA核酸的粗提。也可采购北京百奥莱博科技有限公司生产的DNA提取试剂盒(过柱法-凝胶配套),并按照相应
试剂盒说明进行操作。
6.2.1 培养物:取培养物50μL(培养至一定浊度)或者挑取单克隆菌落与50μL DNA抽提液充分混匀,100℃恒温10min,13000rpm离心3min,取上清5μL进行PCR
反应。
6.2.2 粪便样品:挑取米粒大小粪便于灭菌离心管中,加入0.5mL生理盐水,振荡混匀,13000rpm离心3分钟,弃上清,沉淀中加入50μL DNA抽提液充分混匀,
100℃恒温10min,13000rpm离心3min取上清5μL进行PCR反应。
6.2.3 其他液体标本:取标本2-3mL,13000rpm离心3min,弃上清,沉淀中加入50μL DNA抽提液充分混匀,100℃恒温10min,13000rpm离心3min取上清5μL进
行PCR反应。
注:阳性对照和阴性对照为已经抽提好的核酸(无需提取),直接取5µL加入到反应体系中即可。由于阳性对照浓度较高,建议最后在样品制备区域加入阳性对照。
七、检测步骤:
7.1 试剂的准备
从试剂盒中取出PCR反应液(HPS-PCR MIX),室温融化并振荡混匀后,10000rpm离心10s。
设所需要的PCR反应管管数为N(N=样本数+1管阴性对照+1管阳性对照),每个测试反应体系配制如下:
| 试剂 | 每个反应加入的量 | N个反应加入的量 |
| PCR反应液 | 15µL | N ×15µL |
向设定的N个PCR反应管中分别加入15μL PCR反应液,向每管中加入处理后样品/阴性对照(NTC)/阳性对照(HPS-PTC)5μL,10000rpm瞬时离心10秒。
7.2 PCR反应条件
将各反应管放入PCR仪器的反应槽内。推荐循环条件:
| 预变性 | 1循环 | 94℃ for 2 min |
| PCR扩增 | 35循环 | 94℃ for 30 sec 58℃ for 30 sec 72℃ for 30 sec |
八、结果分析:
(1)称取1.5g琼脂糖放于250mL锥形瓶中,加入100mL 1×TAE电泳缓冲液,微波炉加热溶解,稍冷后加入10μL染色液混匀,倒入插有梳子的制胶板中。
(2)待胶凝固后,取10μL Maker(推荐使用DL2000 Maker)点样于左侧凝胶孔中,取10μL PCR产物依次点样于凝胶孔中,电压值设定为电泳槽正负极距离
(cm)与5(V/cm)的乘积。待*酚兰指示剂电泳至凝胶中部时停止电泳并使用凝胶成像仪或紫外透照台观察结果。
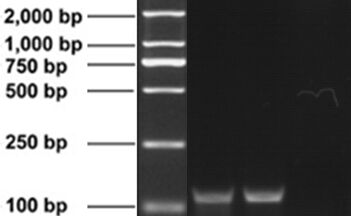
九、结果分析:
(1)阴性对照(NTC):无任何的条带(引物带除外)。
(2)阳性对照(HPS-PTC):在115bp处有条带。
(3)被检样品:在115bp处有条带为阳性样品,否则为阴性样品。
(4)以上条件应同时满足,否则,此次试验视为无效。
北京口蹄疫病毒荧光PCR检测试剂盒(FMDV)厂商关键词:百奥莱博,口蹄疫病毒荧光PCR检测试剂盒(FMDV),SYA401
BL1417 "Western blotting(小鼠/兔IgG)
吲哚-3-丙*(代"烯")酸 8-Hydroxyquinoline sulfate 1204-06-4
CYB164039 兔抗HRP-HRP(PAP)
0.1%甲**(代"胺")蓝水溶液 100ml
ARB13362 牛住肉孢子虫(SArcocystIs)定量分析
ARB10399 人可溶性转铁蛋白受体1(sTfR1)ELISA代测服务 Human soluble transferrin receptor1,stfr1 ELISA KIT
ARB14049 猴白介素17(IL-17)elisa检测操作说明书
聚乙*(代"烯")醇缩丁醛 Meglumine 63148-65-2
PY04-081 甲氧苄*嘧啶乳酸液 0.5mg/支×10支 每支添加于100ml改良SKIRROW培养基基础中
ARB11172 人单核细胞趋化蛋白3(MCP-3/CCL7)代做ELISA实验 Human monocyte chemotactic protein 3,mcp-3 ELISA KIT
BL1209 Cole氏苏木素染色液(常规染色)
ARB13186 小鼠胰岛素样生长因子2(IGF-2)免费代测 Mouse insulin-like growth factor 2,igf-2 ELISA KIT
抗酸染色液(Kinyoun冷染法) 3×50ml|3×100ml
ARB13140 小鼠总三碘甲腺原*酸(TT3)含量分析 Mouse tt3 ELISA KIT
57-30-7 Pentobarbital Sodium *
D2000 II DNA ladder(100-2000bp) 100次
ARB14127 人脂肪酸合酶(FASN)elisa检测
CYB162021 兔抗马IgG(抗血清) 0.5ml
9005-65-6 Tween-80 吐温-80
BTN121002 绿如蓝核酸染料(可见光型) DNAGREEN(Visible Light)
我公司正在火爆促销动物疫病PCR检测试剂盒系列产品,欢迎您的垂询选购北京口蹄疫病毒荧光PCR检测试剂盒(FMDV)厂商。
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验作者:陈文庆 王建超 刘华杰 高飞 张韧(北京清大天一科技有限公司 102200 )(《中国兽药杂志》 2010.44 ( 10 ): 37-41 ) 【摘要】 采用反应器全悬浮培养BHK21细胞生产口蹄疫病毒与微载体悬浮培养Vero细胞生产狂犬病毒分别与相应的转瓶培养工艺生产案例对比分析,比较悬浮培养工艺与转瓶培养工艺的生产效益。分析显示,与转瓶培养工艺相比,反应器悬浮培养工艺获得的细胞密度、病毒效价、产品的产量和质量明显提高,生产时的能耗和劳动力需求明显降低。结果表明悬浮
双球菌NG,巨细胞病毒CMV,结核分支杆菌Mtb、禽流感、阪崎肠杆菌、口蹄疫、新城疫、猪瘟、大肠埃希菌O157∶H7、沙门菌、炭疽芽孢杆菌、胸膜肺炎放线杆菌、寄生虫病等。 PCR仪的应用范围广,几乎所有的生命科学领域都要涉及:食品检测、临床检验、疾病控制、检验检疫、科研实验室、食品安全、化妆品检测、环境卫生等。国内多家试剂厂商生产了包括肝炎、性病、优生优育、呼吸道疾病、禽流感、阪崎肠杆菌、口蹄疫、新城疫、猪瘟、大肠埃希菌O157∶H7、沙门菌、炭疽芽孢杆菌、胸膜肺炎放线
试剂在整个传染病检测市场的份额比例不大,在市场占有上与化学发光和酶免等方法相比,由于灵敏度不高,并不占优势;而且基本集中在低端医院;但是就绝对市场需求量来说还是很大。就新项目而言,肠道相关的幽门螺旋杆菌和轮状病毒检测获得了一定市场。优生优育TORCH系列目前快速诊断的厂商不多,主要为弓形虫、风疹、单纯疱疹病毒I/II、巨细胞病毒IgM五项联合检测。 2. 生殖水平激素相关检测 早早孕与排卵检测项目是目前市场上针对家庭个人检测比重最大的项目,不仅在CDC、临床检验和体检中心大量使用,在家庭个人
 技术资料
技术资料暂无技术资料 索取技术资料









