相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 英文名:
HuCCT1
- 库存:
大量
- 供应商:
中乔新舟
- 细胞类型:
细胞系
- 品系:
human
- 组织来源:
human
- 相关疾病:
否
- 物种来源:
human
- 免疫类型:
否
- 细胞形态:
咨询销售
- 器官来源:
human
- 运输方式:
T25瓶运输
- 年限:
5-10年
- 生长状态:
贴壁生长
- 规格:
5 x 10^5 cells/vial
|
产品名称 |
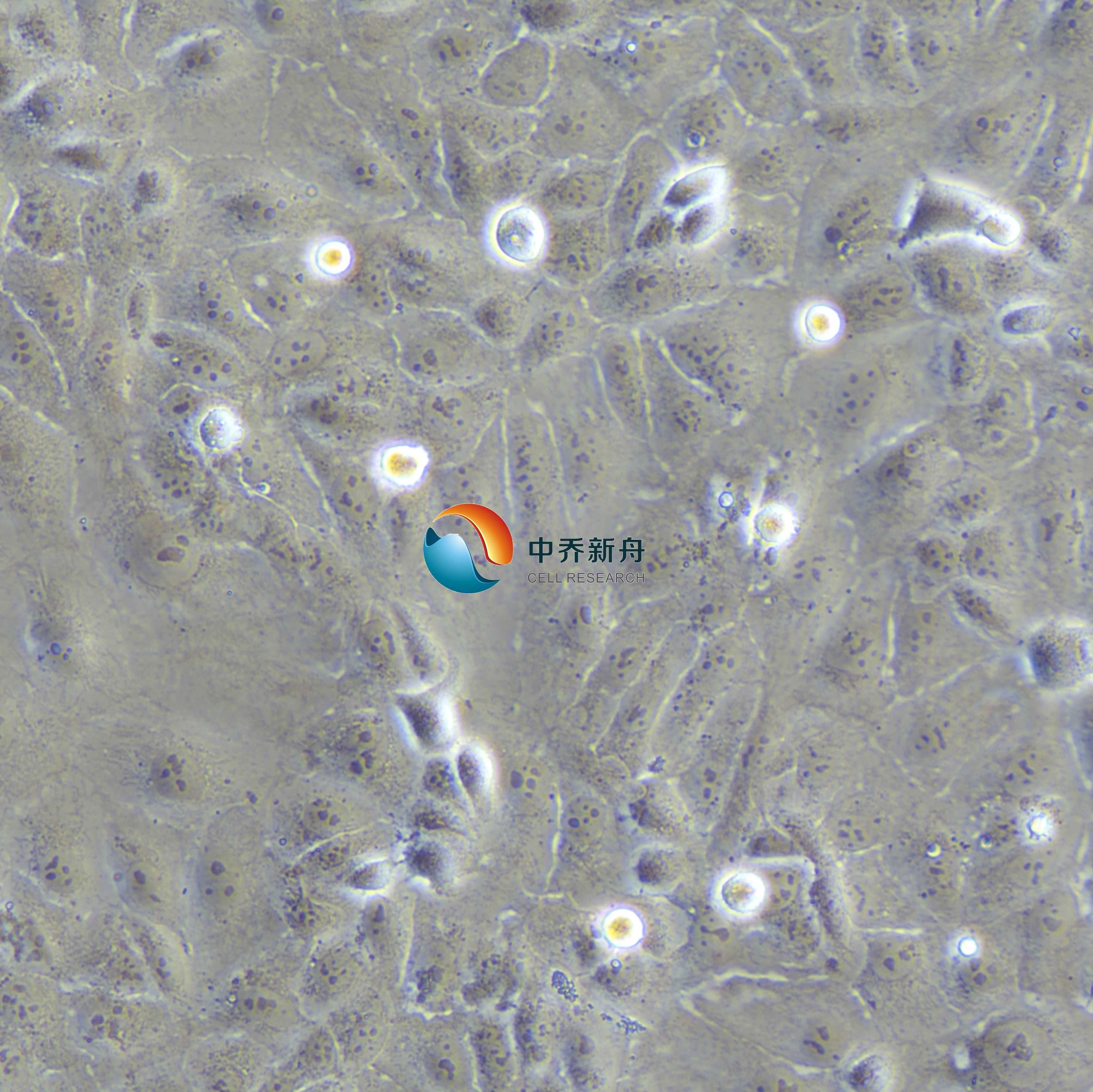
HuCCT1人胆管上皮癌细胞 |
|
货号 |
ZQ0477 |
|
产品介绍 |
HuCCT1是一种人胆管上皮癌细胞系,源自一名56岁男性患者的肝内胆管中分化腺癌,具体是从其腹水中的恶性细胞中获得。胆管癌是一种高度侵袭性的恶性肿瘤,治疗选择有限且预后不良。 HuCC-T1 细胞已广泛用于研究胆管癌的病理生理学并探索潜在的治疗方法。该细胞系对于研究各种化疗药物(包括他汀类药物)的作用特别有价值,他汀类药物已显示出抑制胆管癌细胞增殖的潜力。在涉及 HuCC-T1 的研究中,观察到匹伐他汀和阿托伐他汀等他汀类药物可显着抑制细胞增殖,特别是与吉西他滨、顺铂和 5-氟尿嘧啶 (5-FU) 等传统化疗药物联合使用时。这些药物的组合导致细胞生长的增强抑制,表明潜在的协同作用。作用机制涉及通过抑制 MAPK/ERK 信号通路诱导细胞凋亡,如裂解 caspase-3 水平升高和磷酸化 ERK (p-ERK) 水平降低所证明。这些发现表明,他汀类药物可能作为治疗胆管癌的一种有前途的辅助疗法,与现有抗癌药物一起使用时可能会改善预后。此外,HuCC-T1 细胞系的各种分子标记已被表征,包括 p53 基因状态,它在细胞周期调节和细胞凋亡中发挥着关键作用。 HuCC-T1 中精确的 p53 突变状态可以深入了解细胞系对 DNA 损伤剂的反应及其整体致瘤潜力。鉴于其分子特征,HuCC-T1 仍然是胆管癌研究的关键工具,提供对该疾病分子基础的见解并帮助开发新的治疗策略。 |
|
种属 |
人 |
|
性别/年龄 |
男/56岁 |
|
组织 |
肝脏、胆囊 |
|
疾病 |
肝内胆管癌 |
|
细胞类型 |
肿瘤细胞 |
|
形态学 |
上皮的 |
|
生长方式 |
贴壁 |
|
倍增时间 |
大约55~74小时 |
|
培养基和添加剂 |
RPMI-1640(品牌:中乔新舟 货号:ZQ-200)+10%FBS(品牌:中乔新舟 货号:ZQ500-A)+1%双抗(中乔新舟 货号:CSP006) |
|
推荐完全培养基货号 |
ZM0477 |
|
生物安全等级 |
BSL-1 |
|
STR位点信息 |
Amelogenin:X,Y |
|
培养条件 |
95%空气,5%二氧化碳;37℃ |
|
抗原表达/受体表达 |
*** |
|
基因表达 |
*** |
|
保藏机构 |
JCRB; JCRB0425 RCB; RCB1960 |
|
供应限制 |
仅供科研使用 |
上海中乔新舟生物科技有限公司成立于2011年,历经十多年发展,主要专注于细胞生物学产品的研究和开发,专注于为药企、各类科研机构及CRO企业提供符合标准规范的细胞培养服务、细胞培养基、细胞检测试剂盒、细胞培养试剂,胎牛血清和细胞生物学技术服务等。
公司一直致力于为高等院校、研究机构、医院、CRO及CDMO企业提供细胞培养完整解决方案,这些产品旨在满足细胞培养的多样需求,确保实验和研究的有效进行。引用中乔新舟(ZQXZBIO)产品和服务的文献超数千篇。

产品服务
细胞资源:原代细胞、细胞株、干细胞、示踪细胞、耐药株细胞、永生化细胞等基因工程细胞。
试剂产品:胎牛血清、完全培养基(适用于原代细胞及细胞株)、无血清培养基、基础培养基、细胞转染试剂、重组因子、胰酶和双抗等等细胞培养所有实验相关产品。
技术服务:稳转株构建、原代细胞分离、特殊培养基定制服务、细胞检测等。

目前产品已经畅销国内30多个省市,与客户建立长期的合作伙伴关系,共同实现成功。全体员工将不懈努力,继续为科研人员提供优良的产品和服务,致力成为全球细胞培养领域的参与者。
企业愿景
致力于成为国内细胞培养基产业的佼佼者,生物医药领域上游原材料的优良提供商。
企业使命
成长为专业细胞系及原代细胞培养供应商、专业细胞培养基及培养试剂生产商。
企业荣誉


风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验论文标题: LncRNA MT1JP plays a protective role in intrahepatic cholangiocarcinoma by regulating miR-18a-5p/FBP1 axis
DOI: 10.1186/s12885-021-07838-0
发表时间: 2021-02-08
期刊: BMC CANCER
影响因子: 4.43
货号: ZQ0477
产品名称: HUCCT1 cells
论文标题: Forced overexpression of FBP1 inhibits proliferation and metastasis in cholangiocarcinoma cells via Wnt/β-catenin pathway
DOI: 10.1016/j.lfs.2018.09.009
发表时间: 2018-09-04
期刊: LIFE SCIENCES
影响因子: 3.234
货号: ZQ0477
产品名称: HUCCT1 cells
PubMed=2544546; DOI=10.1007/BF02623562
Miyagiwa M., Ichida T., Tokiwa T., Sato J., Sasaki H.
A new human cholangiocellular carcinoma cell line (HuCC-T1) producing carbohydrate antigen 19/9 in serum-free medium.
In Vitro Cell. Dev. Biol. 25:503-510(1989)
DOI=10.11418/jtca1981.16.3_173
Mihara K., Miyazaki M., Fushimi K., Tsuji T., Inoue Y., Fukaya K.-i., Ohashi R., Namba M.
The p53 gene status and other cellular characteristics of human cell lines maintained in our laboratory.
Tissue Cult. Res. Commun. 16:173-178(1997)
PubMed=9290701; DOI=10.1002/(SICI)1098-2744(199708)19:4<243::AID-MC5>3.0.CO;2-D
Jia L.-Q., Osada M., Ishioka C., Gamo M., Ikawa S., Suzuki T., Shimodaira H., Niitani T., Kudo T., Akiyama M., Kimura N., Matsuo M., Mizusawa H., Tanaka N., Koyama H., Namba M., Kanamaru R., Kuroki T.
Screening the p53 status of human cell lines using a yeast functional assay.
Mol. Carcinog. 19:243-253(1997)
PubMed=20164919; DOI=10.1038/nature08768
Bignell G.R., Greenman C.D., Davies H., Butler A.P., Edkins S., Andrews J.M., Buck G., Chen L., Beare D., Latimer C., Widaa S., Hinton J., Fahey C., Fu B.-Y., Swamy S., Dalgliesh G.L., Teh B.T., Deloukas P., Yang F.-T., Campbell P.J., Futreal P.A., Stratton M.R.
Signatures of mutation and selection in the cancer genome.
Nature 463:893-898(2010)
PubMed=20215515; DOI=10.1158/0008-5472.CAN-09-3458
Rothenberg S.M., Mohapatra G., Rivera M.N., Winokur D., Greninger P., Nitta M., Sadow P.M., Sooriyakumar G., Brannigan B.W., Ulman M.J., Perera R.M., Wang R., Tam A., Ma X.-J., Erlander M., Sgroi D.C., Rocco J.W., Lingen M.W., Cohen E.E.W., Louis D.N., Settleman J., Haber D.A.
A genome-wide screen for microdeletions reveals disruption of polarity complex genes in diverse human cancers.
Cancer Res. 70:2158-2164(2010)
PubMed=21451941; DOI=10.1007/s00534-011-0376-7
Sato J., Kimura T., Saito T., Anazawa T., Kenjo A., Sato Y., Tsuchiya T., Gotoh M.
Gene expression analysis for predicting gemcitabine resistance in human cholangiocarcinoma.
J. Hepatobiliary Pancreat. Sci. 18:700-711(2011)
PubMed=21687941; DOI=10.3892/ijo.2011.1087
Kamigaki M., Sasaki T., Serikawa M., Inoue M., Kobayashi K., Itsuki H., Minami T., Yukutake M., Okazaki A., Ishigaki T., Ishii Y., Kosaka K., Chayama K.
Statins induce apoptosis and inhibit proliferation in cholangiocarcinoma cells.
Int. J. Oncol. 39:561-568(2011)
PubMed=22460905; DOI=10.1038/nature11003
Barretina J.G., Caponigro G., Stransky N., Venkatesan K., Margolin A.A., Kim S., Wilson C.J., Lehar J., Kryukov G.V., Sonkin D., Reddy A., Liu M., Murray L., Berger M.F., Monahan J.E., Morais P., Meltzer J., Korejwa A., Jane-Valbuena J., Mapa F.A., Thibault J., Bric-Furlong E., Raman P., Shipway A., Engels I.H., Cheng J., Yu G.-Y.K., Yu J.-J., Aspesi P. Jr., de Silva M., Jagtap K., Jones M.D., Wang L., Hatton C., Palescandolo E., Gupta S., Mahan S., Sougnez C., Onofrio R.C., Liefeld T., MacConaill L.E., Winckler W., Reich M., Li N.-X., Mesirov J.P., Gabriel S.B., Getz G., Ardlie K., Chan V., Myer V.E., Weber B.L., Porter J., Warmuth M., Finan P., Harris J.L., Meyerson M.L., Golub T.R., Morrissey M.P., Sellers W.R., Schlegel R., Garraway L.A.
The Cancer Cell Line Encyclopedia enables predictive modelling of anticancer drug sensitivity.
Nature 483:603-607(2012)
三句话读懂一篇 CNS,剪接体靶向疗法诱导癌细胞「自杀」,皮炎瘙痒突然加重的机制,免疫调节因子 STING 感知疼痛机制...
「迷惑战术」令癌细胞自杀 2021 年 1 月 13 日,美国休斯敦贝勒医学院 Thomas F. Westbrook 团队在 Cell 杂志发表论文 Spliceosome-targeted therapies trigger an antiviral immune response in triple-negative breast cancer,利用一种新颖的剪接体靶向疗法(spliceosome-targeted therapies),令异常的 RNA 长链堆积在细胞质,通过激活人体抗病
癌细胞真的可以被「饿」死吗?Nature 报道该方法已上临床试验,但禁食模拟饮食≠禁食!
近年来「饿死癌细胞」成为了炙手可热的研究领域,在大众和科研工作者中都具有非常高的关注度。尽管学术媒体充分报道了相关疗法的局限性,可挨饿治癌症的谣言也开始流传。 毫无疑问,由于癌细胞需要大量的能量以及营养供其生长,让癌细胞「饥饿」的确能够在一定程度上抑制癌症的生长。但我们对「饥饿」疗法的了解还相当有限,大量研究也只是停留在动物和细胞层面,而且局限在肿瘤所在的微环境。因为我们无法在让癌细胞挨饿的同时不饿着正常的细胞,所以目前并没有安全有效的「禁食」疗法被应用到癌症的临床治疗中来。 如何利用癌细胞
恶性肿瘤的主要生物学特性之一是转移性,建立与临床表现相近的动物模型是研究的关键环节。人体肿瘤移植于裸小鼠建立人癌异种移植动物模型为深入研究提供了可能。原位移植可为人体肿瘤生长提供相似的微环境,更利于肿瘤恶性行为的表现,因此,大多采用原位移植的方法建立肿瘤转移动物模型。 根据我们多年的肿瘤模型构建经验,为大家介绍几种我们常遇到的几种肿瘤模型构建方法,以供参考。 一、人肝癌原位移植模型 将人肝癌细胞株(如:HepG2等)传代培养后,收集对数生长期的细胞制成
 技术资料
技术资料暂无技术资料 索取技术资料