相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 询价记录
- 文献和实验
- 技术资料
- 国食药监械注册号:
无
- 库存:
100
- 供应商:
玉研科学仪器有限公司
- 现货状态:
大鼠足趾肿胀测定仪,大鼠肿胀测量仪,小鼠肿胀测量仪
- 保修期:
12个月
- 规格:
请来电咨询
在类风湿性关节炎、水肿的中枢发展及其通过药理学过程的改变的研究中,测量大鼠足爪的炎症过程被证明具有重要价值。
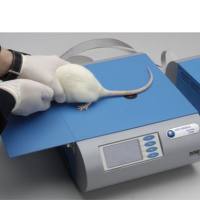
Ugo肢体肿胀测量仪在图形LCD读数上显示准确的爪子体积。微小差异由原创设计的传感器检测。
主要用途:
测量肢体末端的体积,用于炎症肿胀程度的研究。可用于风湿关节炎、水肿等多种药理实验,精确测量大鼠、小鼠的肢体肿胀情况。自上世纪60年代起,已经有超过1000篇的引用文献。
肢体肿胀测量仪微处理器控制的仪器主要特点:
计算机兼容性:直接连接到PC(通过包含的52050软件)
体积测量水池:
测量池由两个垂直互连的有机玻璃管组成;将动物爪子浸入较大的管子(直径1.8厘米)中以测量排水量。还包 括一根较小直径 (1.3 厘米) 的管子,用于小鼠爪子。
直径较小的侧管包含传感 器,用于测量两个垂直导线电极之间的电导。
电导与水位成线性比例,因此可置换得到体积。
数据采集:
37140测量仪为微处理器控制led,具有直接PC输出功能。内部存储的数据可以路由到PC串行(RS232)或USB端口(通过适配器)。
通信由专用软件,一种基于Windows®的数据采集软件包,Cat52050-02管理,可将数据存储到单个文件(以.csv 格式)中,以便于管理Excel或其他统计分析软件包。




部分参考文献:




敬请来电咨询。
敬请关注玉研仪器微信号:

风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
- 作者
- 内容
- 询问日期
 文献和实验
文献和实验1、Bang, Sangsu et al. “GPR37 regulates macrophage phagocytosis and resolution of inflammatory pain.” The Journal of clinical investigation vol. 128,8 (2018): 3568-3582. doi:10.1172/JCI99888
IF: 19.46
2、Bang, Sangsu et al. “Activation of GPR37 in macrophages confers protection against infection-induced sepsis and pain-like behaviour in mice.” Nature communications vol. 12,1 1704. 17 Mar. 2021, doi:10.1038/s41467-021-21940-8
IF: 17.70
3、Hemed-Shaked, Maayan et al. “MTADV 5-MER peptide suppresses chronic inflammations as well as autoimmune pathologies and unveils a new potential target-Serum Amyloid A.” Journal of autoimmunity vol. 124 (2021): 102713. doi:10.1016/j.jaut.2021.102713
IF: 14.51
4、Romani, Luciana F A et al. “Physicochemical characterization, the Hirshfeld surface, and biological evaluation of two meloxicam compounding pharmacy samples.” Journal of pharmaceutical analysis vol. 8,2 (2018): 103-108. doi:10.1016/j.jpha.2017.12.006
IF: 14.03
5、Kwon, Hyuk-Kwon et al. “A cell-penetrating peptide blocks Toll-like receptor-mediated downstream signaling and ameliorates autoimmune and inflammatory diseases in mice.” Experimental & molecular medicine vol. 51,4 1-19. 26 Apr. 2019, doi:10.1038/s12276-019-0244-0
IF: 12.15
6、Allen, Brian D et al. “Hyperadrenocorticism of calorie restriction contributes to its anti-inflammatory action in mice.” Aging cell vol. 18,3 (2019): e12944. doi:10.1111/acel.12944
IF: 11.01
7、Mzoughi, Zeineb et al. “Optimized extraction of pectin-like polysaccharide from Suaeda fruticosa leaves: Characterization, antioxidant, anti-inflammatory and analgesic activities.” Carbohydrate polymers vol. 185 (2018): 127-137. doi:10.1016/j.carbpol.2018.01.022
IF: 10.72
8、Ilari, Sara et al. “Antioxidant modulation of sirtuin 3 during acute inflammatory pain: The ROS control.” Pharmacological research vol. 157 (2020): 104851. doi:10.1016/j.phrs.2020.104851
IF: 10.33
9、Horváth, Ádám et al. “Analgesic effects of the novel semicarbazide-sensitive amine oxidase inhibitor SZV 1287 in mouse pain models with neuropathic mechanisms: Involvement of transient receptor potential vanilloid 1 and ankyrin 1 receptors.” Pharmacological research vol. 131 (2018): 231-243. doi:10.1016/j.phrs.2018.02.006
IF: 10.33
10、Pohóczky, Krisztina et al. “Discovery of novel targets in a complex regional pain syndrome mouse model by transcriptomics: TNF and JAK-STAT pathways.” Pharmacological research vol. 182 (2022): 106347. doi:10.1016/j.phrs.2022.106347
IF: 10.33
11、Zhang, Yan-Yu et al. “(9S,13R)-12-oxo-phytodienoic acid attenuates inflammation by inhibiting mPGES-1 and modulating macrophage polarization via NF-κB and Nrf2/HO-1 pathways.” Pharmacological research vol. 182 (2022): 106310. doi:10.1016/j.phrs.2022.106310
IF: 10.33
12、Guo, Bin et al. “Elucidation of the anti-inflammatory mechanism of Er Miao San by integrative approach of network pharmacology and experimental verification.” Pharmacological research vol. 175 (2022): 106000. doi:10.1016/j.phrs.2021.106000
IF: 10.33
13、Winters, Bryony L et al. “Inflammation induces developmentally regulated sumatriptan inhibition of spinal synaptic transmission.” British journal of pharmacology vol. 177,16 (2020): 3730-3743. doi:10.1111/bph.15089
IF: 9.47
14、Gusmao-Silva, Guilherme et al. “Hsp65-Producing Lactococcocus lactis Prevents Antigen-Induced Arthritis in Mice.” Frontiers in immunology vol. 11 562905. 23 Sep. 2020, doi:10.3389/fimmu.2020.562905
IF: 8.79
15、Miranda, Joana P et al. “The Secretome Derived From 3D-Cultured Umbilical Cord Tissue MSCs Counteracts Manifestations Typifying Rheumatoid Arthritis.” Frontiers in immunology vol. 10 18. 5 Feb. 2019, doi:10.3389/fimmu.2019.00018
IF: 8.79
长期的实验时,应每隔7~10天称量一次。小鼠、大鼠:称量可用普通的天平或者电子秤称重。兔、豚鼠:可直接放在婴儿秤上称重,从婴儿秤圆形刻度盘上读取动物体重。犬:经训练后可直接放在磅秤上称重。未经驯服的犬,先将犬嘴绑好,由实验员把犬抱起站在磅秤上称重,记下读数,减去实验员体重,即为动物体重。二、体温的测定方法动物体温测定可采用普通体温计(肛表、口表)或半导体温度计,为防止测定过程中动物挣扎,以至于挫伤肠壁或折断体温计,在测定前应先固定好动物。肛表测温可由实验者右手固定体温计,3分钟后取出观察读数。半导体点
在过去20年中,研究科学家们一直在寻找更加精确的无创测量小鼠或大鼠血压的方法。更加精确的用无创的方法测量啮齿动物的收缩压、舒张压、心率、和其他一些血流的参数,对于临床研究是很有价值的。 一、有创方法测量血压 有创血压是评价无创血压的金标准。当评价无创血压时,有创血压的测量是从动物颈动脉测量的。 利用遥测方法测量到血压也是非常可靠和精确的,它也被用来评价无创血压的真实性。这种方法通过在动物体内埋藏植入子来测量无创血压,这种方法测量到的动物血压与直接方法测量的血压
盐水中混合,经37℃培养5~10分钟放4℃过夜,取细胞悬计数,外周血淋巴细胞中约70%~80%淋巴细胞结成花环即为T细胞。目前此方法已用来分离T细胞,而不用做T细胞计数。 (2)用单克隆抗体计数T细胞:将人的PBM分成三等份,分别用小鼠抗人CD3、CD4和CD8的单克隆抗体作第一抗体与细胞结合,再用FITC标记的兔抗小鼠IgG抗体作第二抗体进行间接免疫荧光染色,在荧光显微镜下或流式细胞仪检测结果,在PBM中被CD3抗体染上荧光的细胞称为CD3+细胞即总T细胞。正常人在PBM中T细胞占70%~80
 技术资料
技术资料