万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 英文名:
KU812
- 库存:
大量
- 供应商:
中乔新舟
- 细胞类型:
细胞系
- 品系:
human
- 组织来源:
human
- 相关疾病:
否
- 物种来源:
human
- 免疫类型:
否
- 细胞形态:
咨询销售
- 器官来源:
human
- 运输方式:
T25瓶运输
- 年限:
5-10年
- 生长状态:
悬浮生长
- 规格:
5 x 10^5 cells/vial
|
产品名称 |
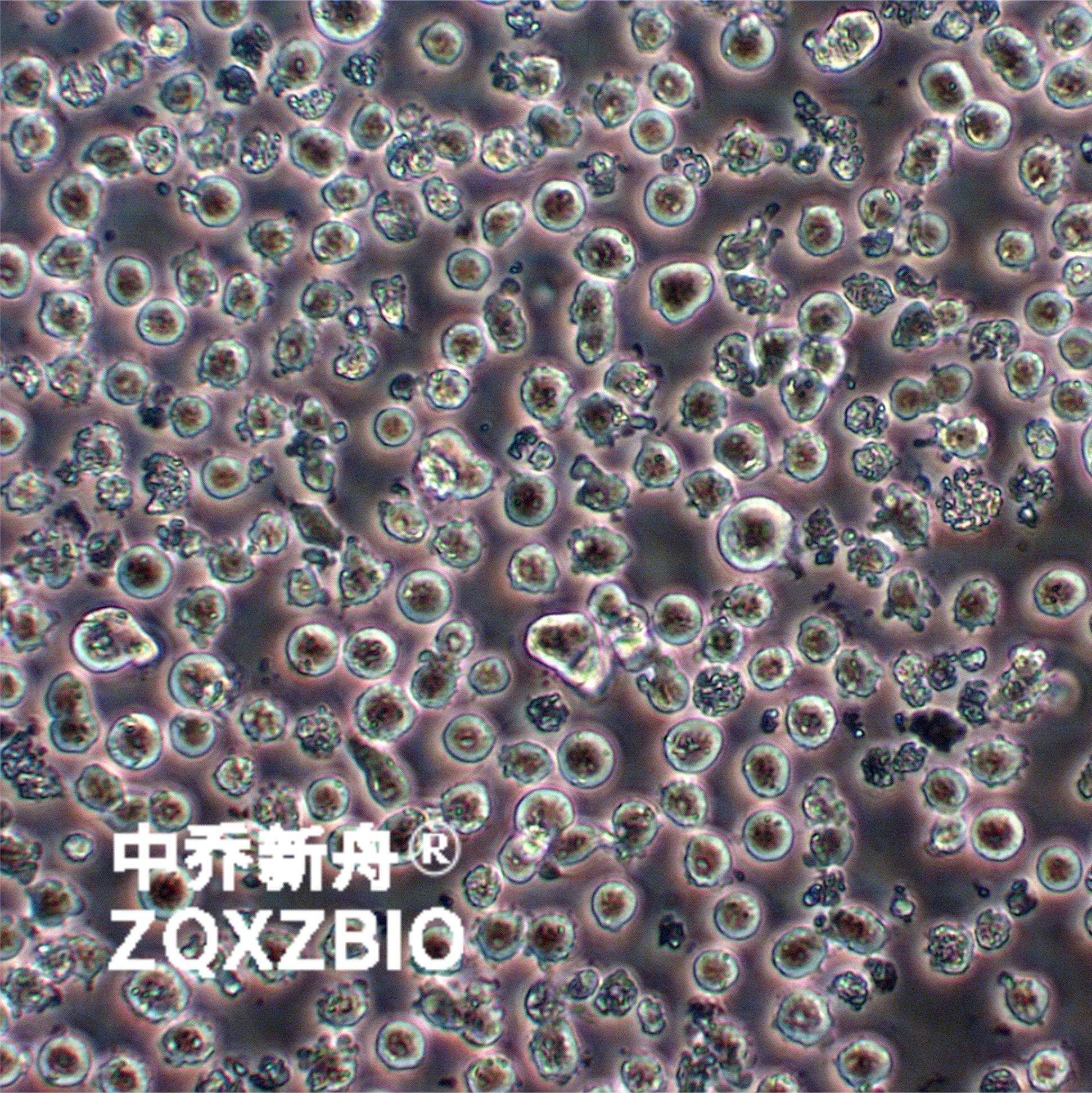
KU812人外周血嗜碱性白血病细胞 |
|
货号 |
ZQ0427 |
|
产品介绍 |
KU812 是从一名 38 岁亚洲男性慢性粒细胞白血病 (cml) 患者的外周血中分离出来的嗜碱性粒细胞。这些细胞至少含有一条 Ph1(费城)染色体。该细胞系具有嗜碱性白细胞的一些特征(Fc 受体、嗜碱性颗粒、组胺产生),并且淋巴标记物呈阴性。该细胞系具有嗜碱性白细胞的一些特征(Fc 受体、嗜碱性颗粒、组胺产生),并且淋巴标记物呈阴性。可用于免疫学和免疫系统疾病研究。 |
|
种属 |
人 |
|
性别/年龄 |
男/38岁 |
|
组织 |
外周血 |
|
疾病 |
慢性粒细胞白血病Cml |
|
细胞类型 |
肿瘤细胞 |
|
形态学 |
成髓细胞 |
|
生长方式 |
悬浮 |
|
倍增时间 |
大约20~100小时 |
|
培养基和添加剂 |
IMDM(品牌:中乔新舟 货号:ZQ-900)+20%胎牛血清(中乔新舟 货号:ZQ0500)+1%P/S(中乔新舟 货号:CSP006) |
|
推荐完全培养基货号 |
ZM0427 |
|
生物安全等级 |
BSL-1 |
|
STR位点信息 |
Amelogenin:X,Y CSF1PO:12,13 D12S391:17,17 D13S317:8,8 D16S539:9,9 D18S51:13,13 D19S433:13,14 D21S11:30,31.2 D2S1338:18,18 D3S1358:15,15 D5S818:10,10 D6S1043:11,11 D7S820:12,12 D8S1179:11,15 FGA:22,24 Penta E:5,19 TH01:9,9 TPOX:12,12 vWA:15,15; |
|
培养条件 |
95%空气,5%二氧化碳;37℃ |
|
抗原表达/受体表达 |
*** |
|
基因表达 |
*** |
|
保藏机构 |
ATCC; CRL-2099 BCRC; 60502 BCRJ; 0261 DSMZ; ACC-378 ECACC; 90071807 |
|
供应限制 |
仅供科研使用 |
上海中乔新舟生物科技有限公司成立于2011年,历经十多年发展,主要专注于细胞生物学产品的研究和开发,专注于为药企、各类科研机构及CRO企业提供符合标准规范的细胞培养服务、细胞培养基、细胞检测试剂盒、细胞培养试剂,胎牛血清和细胞生物学技术服务等。
公司一直致力于为高等院校、研究机构、医院、CRO及CDMO企业提供细胞培养完整解决方案,这些产品旨在满足细胞培养的多样需求,确保实验和研究的有效进行。引用中乔新舟(ZQXZBIO)产品和服务的文献超数千篇。

产品服务
细胞资源:原代细胞、细胞株、干细胞、示踪细胞、耐药株细胞、永生化细胞等基因工程细胞。
试剂产品:胎牛血清、完全培养基(适用于原代细胞及细胞株)、无血清培养基、基础培养基、细胞转染试剂、重组因子、胰酶和双抗等等细胞培养所有实验相关产品。
技术服务:稳转株构建、原代细胞分离、特殊培养基定制服务、细胞检测等。

目前产品已经畅销国内30多个省市,与客户建立长期的合作伙伴关系,共同实现成功。全体员工将不懈努力,继续为科研人员提供优良的产品和服务,致力成为全球细胞培养领域的参与者。
企业愿景
致力于成为国内细胞培养基产业的佼佼者,生物医药领域上游原材料的优良提供商。
企业使命
成长为专业细胞系及原代细胞培养供应商、专业细胞培养基及培养试剂生产商。
企业荣誉


风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验PubMed=3858609; DOI=10.1016/0145-2126(85)90060-8
Kishi K.
A new leukemia cell line with Philadelphia chromosome characterized as basophil precursors.
Leuk. Res. 9:381-390(1985)
PubMed=3332852; DOI=10.1016/S0950-3536(87)80037-9
Keating A.
Ph positive CML cell lines.
Baillieres Clin. Haematol. 1:1021-1029(1987)
PubMed=2540861; DOI=10.1182/blood.V73.7.2003.2003
Nakazawa M., Mitjavila-Garcia M.-T., Debili N., Casadevall N., Mayeux P., Rouyer-Fessard P., Dubart-Kupperschmitt A., Romeo P.-H., Beuzard Y., Kishi K., Breton-Gorius J., Vainchenker W.
KU 812: a pluripotent human cell line with spontaneous erythroid terminal maturation.
Blood 73:2003-2013(1989)
DOI=10.11418/jtca1981.15.4_211
Matsuo Y., Okochi A., Ariyasu T., Iimura E., Ohno T.
Identification of cell lines with variable numbers of tandem repeat (VNTR) amplified by polymerase chain reaction.
Tissue Cult. Res. Commun. 15:211-219(1996)
PubMed=9290701; DOI=10.1002/(SICI)1098-2744(199708)19:4<243::AID-MC5>3.0.CO;2-D
Jia L.-Q., Osada M., Ishioka C., Gamo M., Ikawa S., Suzuki T., Shimodaira H., Niitani T., Kudo T., Akiyama M., Kimura N., Matsuo M., Mizusawa H., Tanaka N., Koyama H., Namba M., Kanamaru R., Kuroki T.
Screening the p53 status of human cell lines using a yeast functional assay.
Mol. Carcinog. 19:243-253(1997)
PubMed=9510473; DOI=10.1111/j.1349-7006.1998.tb00476.x
Hosoya N., Hangaishi A., Ogawa S., Miyagawa K., Mitani K., Yazaki Y., Hirai H.
Frameshift mutations of the hMSH6 gene in human leukemia cell lines.
Jpn. J. Cancer Res. 89:33-39(1998)
PubMed=9644295; DOI=10.1159/000040837
Kaneko H., Horiike S., Sasai Y., Iwai T., Nakao M., Yokota S., Taniwaki M., Kashima K., Misawa S.-i.
Rare alteration of genomic structure or expression of the DPC4 gene in myelogenous leukemias.
Acta Haematol. 99:187-190(1998)
PubMed=10071072; DOI=10.1016/S0145-2126(98)00171-4
Drexler H.G., MacLeod R.A.F., Uphoff C.C.
Leukemia cell lines: in vitro models for the study of Philadelphia chromosome-positive leukemia.
Leuk. Res. 23:207-215(1999)
PubMed=10576511; DOI=10.1016/s0145-2126(99)00131-9
Uphoff C.C., Habig S., Fombonne S., Matsuo Y., Drexler H.G.
ABL-BCR expression in BCR-ABL-positive human leukemia cell lines.
Leuk. Res. 23:1055-1060(1999)
DOI=10.1016/B978-0-12-221970-2.50457-5
Drexler H.G.
The leukemia-lymphoma cell line factsbook.
(In) ISBN 9780122219702; pp.1-733; Academic Press; London (2001)
PubMed=11264164; DOI=10.1182/blood.v97.7.1999
Kano Y., Akutsu M., Tsunoda S., Mano H., Sato Y., Honma Y., Furukawa Y.
In vitro cytotoxic effects of a tyrosine kinase inhibitor STI571 in combination with commonly used antileukemic agents.
Blood 97:1999-2007(2001)
PubMed=11416159; DOI=10.1073/pnas.121616198
Masters J.R.W., Thomson J.A., Daly-Burns B., Reid Y.A., Dirks W.G., Packer P., Toji L.H., Ohno T., Tanabe H., Arlett C.F., Kelland L.R., Harrison M., Virmani A.K., Ward T.H., Ayres K.L., Debenham P.G.
Short tandem repeat profiling provides an international reference standard for human cell lines.
Proc. Natl. Acad. Sci. U.S.A. 98:8012-8017(2001)
PubMed=15843827; DOI=10.1038/sj.leu.2403749
Andersson A., Eden P., Lindgren D., Nilsson J., Lassen C., Heldrup J., Fontes M., Borg A., Mitelman F., Johansson B., Hoglund M., Fioretos T.
Gene expression profiling of leukemic cell lines reveals conserved molecular signatures among subtypes with specific genetic aberrations.
Leukemia 19:1042-1050(2005)
PubMed=16408098; DOI=10.1038/sj.leu.2404081
Quentmeier H., MacLeod R.A.F., Zaborski M., Drexler H.G.
JAK2 V617F tyrosine kinase mutation in cell lines derived from myeloproliferative disorders.
Leukemia 20:471-476(2006)
PubMed=20164919; DOI=10.1038/nature08768
Bignell G.R., Greenman C.D., Davies H., Butler A.P., Edkins S., Andrews J.M., Buck G., Chen L., Beare D., Latimer C., Widaa S., Hinton J., Fahey C., Fu B.-Y., Swamy S., Dalgliesh G.L., Teh B.T., Deloukas P., Yang F.-T., Campbell P.J., Futreal P.A., Stratton M.R.
Signatures of mutation and selection in the cancer genome.
Nature 463:893-898(2010)
PubMed=20215515; DOI=10.1158/0008-5472.CAN-09-3458
Rothenberg S.M., Mohapatra G., Rivera M.N., Winokur D., Greninger P., Nitta M., Sadow P.M., Sooriyakumar G., Brannigan B.W., Ulman M.J., Perera R.M., Wang R., Tam A., Ma X.-J., Erlander M., Sgroi D.C., Rocco J.W., Lingen M.W., Cohen E.E.W., Louis D.N., Settleman J., Haber D.A.
A genome-wide screen for microdeletions reveals disruption of polarity complex genes in diverse human cancers.
Cancer Res. 70:2158-2164(2010)
PubMed=20809971; DOI=10.1186/1755-8166-3-15
Virgili A., Nacheva E.
Genomic amplification of BCR/ABL1 and a region downstream of ABL1 in chronic myeloid leukaemia: a FISH mapping study of CML patients and cell lines.
Mol. Cytogenet. 3:15.1-15.12(2010)
PubMed=22460905; DOI=10.1038/nature11003
Barretina J.G., Caponigro G., Stransky N., Venkatesan K., Margolin A.A., Kim S., Wilson C.J., Lehar J., Kryukov G.V., Sonkin D., Reddy A., Liu M., Murray L., Berger M.F., Monahan J.E., Morais P., Meltzer J., Korejwa A., Jane-Valbuena J., Mapa F.A., Thibault J., Bric-Furlong E., Raman P., Shipway A., Engels I.H., Cheng J., Yu G.-Y.K., Yu J.-J., Aspesi P. Jr., de Silva M., Jagtap K., Jones M.D., Wang L., Hatton C., Palescandolo E., Gupta S., Mahan S., Sougnez C., Onofrio R.C., Liefeld T., MacConaill L.E., Winckler W., Reich M., Li N.-X., Mesirov J.P., Gabriel S.B., Getz G., Ardlie K., Chan V., Myer V.E., Weber B.L., Porter J., Warmuth M., Finan P., Harris J.L., Meyerson M.L., Golub T.R., Morrissey M.P., Sellers W.R., Schlegel R., Garraway L.A.
The Cancer Cell Line Encyclopedia enables predictive modelling of anticancer drug sensitivity.
Nature 483:603-607(2012)
Jurkat细胞(人外周血白血病T细胞),是一种悬浮细胞。我的经验如下:1、培养液:RPMI1640,15%小牛血清,2%Na2CO3,1%HEPES,青霉素100IU/1ml,庆大霉素100IU/ml;2、培养条件:5%CO2,37度,30%湿度;3、细胞复苏:要快速将冻存管放入37度水中,不断轻轻摇晃,直到细胞完全溶解,加入10ml左右的培养液,800~1000rpm,10分钟离心,之后倒掉液体,加入新的培养基就可以进行培养了;4、细胞培养:起初进行传代时由于细胞刚刚复苏,长得比较
并杀伤异化或者被感染的自身细胞,但是与 CTL 不同,它可以识别 MHC I缺失的细胞,与 CTL 互补。人和小鼠的 NK 细胞表面标志物差异较大,在流式检测中所用的抗体也有所不同。人外周血NK细胞主要通过 CD16(Cat#E-AB-F1005)和CD56(Cat#E-AB-F1006)来确定,双阳的细胞被认为是 NK 细胞。在小鼠中,通用的表面标志物是CD49b(Cat#E-AB-F0988),而对于免疫学研究中最常用的 C57BL/6 小鼠,还有专门的 NK 表面标志物 NK1.1(CD
特点是能够将两种性质完全不同的外源多肽或蛋白质,分别与T4衣壳表面上的外壳蛋白SOC(9 ku)和HOC(40 ku)融合而直接展示于T4噬菌体的表面,因此它表达的蛋白不需要复杂的蛋白纯化,避免了因纯化而引起的蛋白质变性和丢失。其病毒颗粒在宿主细胞内组装,不经过分泌途径,因而其表面展示多肽的范围更广,尤其适用于那些不能被大肠杆菌分泌的复杂蛋白质。值得关注的是,SOC与HOC蛋白的存在与否并不影响T4的生存和繁殖。SOC和HOC在噬菌体组装时可优于DNA的包装而装配于衣壳的表面。事实上,在DNA包装被抑制
 技术资料
技术资料暂无技术资料 索取技术资料