相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 询价记录
- 文献和实验
- 技术资料
- 国食药监械注册号:
无
- 库存:
100
- 供应商:
玉研仪器公司
- 现货状态:
现货
- 保修期:
12个月
- 规格:
敬请来电咨询
气管插管平台主要用来在经口气管插管手术中,对小鼠、大鼠进行固定,能够将老鼠调节到合适的角度,有利于手术操作,减少实验时间,提供成功率。

型号:CG-04M
另外,可选配大小鼠气管插管喉镜、大小鼠气管插管工具包套装、大小鼠气管插管等工具,能更便捷的完成手术。
大鼠、小鼠喉镜
大小鼠气管插管工具包套装
气管插管平台(多种款式和型号可选)

CG-02M型,适合做小鼠,外尺寸:20*15*20cm
CG-02R型,适合做大鼠,外尺寸:22*21*28cm
适用于大、小鼠的气管插管手术操作
型号:CG-06M
多角度可调;
大小鼠通用,尺寸约:20*15*15cm
小鼠气管插管平台(小鼠型)
型号:T-100S
尺寸:20*12cm
材质:PE板
附件:不锈钢丝,可勾住麻醉状态的小鼠门齿,进行气管插管或喉部的其他实验
小动物多功能操作台
关键词:老鼠手术台,大小鼠手术台,动物手术台,动物手术板,气体麻醉机,气管插管工作台,大小鼠操作台
型号:T-100A
产品特点:
· 圆形、吸盘式底座,固定牢固;
· 尺寸为250×200×130mm;
· 带四个脚爪和一个门齿固定螺栓;
· 360°多角度均可偏转;
· 前后倾角均为40°;
也可以选择:动物手术创口牵开器
可用于小动物(小鼠、大鼠)的胸腔、腹腔、颈部或其他创口的牵开手术。系统采用模块化组合设计,搭配灵活,操作方便。
根据需要,可选择大鼠、小鼠常规型手术板:
多种手术板可供选择:
小鼠手术板

型号:30151
尺寸:22*12cm
材质:PE板
附件:带6个固定螺栓
型号:30153
尺寸:22*12cm
材质:PE板
附件:带6个固定螺栓盒气体麻醉面罩
大鼠手术板

型号:30150
尺寸:33*25cm
材质:PE板
附件:带11个固定螺栓
型号:30152
带大小鼠麻醉面罩
尺寸:33*25cm
材质:PE板
附件:带11个固定螺栓,带双层气体麻醉面罩

型号:30120
尺寸:24*13cm(大鼠、小鼠通用)
材质:PVC材质
附件:带5个固定螺栓,可根据需求定制尺寸
大小鼠通用型不锈钢手术板
型号:30350
尺寸:30*20cm
材质:304不锈钢
附件:带11个固定螺栓
大小鼠通用,不锈钢手术板(带夹子)
型号:30351
尺寸:30*20cm
材质:304不锈钢
附件:带4个夹子,1个固定螺栓
大小鼠通用,不锈钢手术板(带固定柱子)
型号:30355
尺寸:30*20cm
材质:304不锈钢
附件:带5个固定柱子
保温型不锈钢手术板
型号:T-30350
在不锈钢手术板基础上可增配加热模块,控制手术板温度在20-50°C
整体尺寸:30*20*10cm
材质:304不锈钢
附件:带11个固定螺栓
根据需要,有多种大鼠、小鼠固定器可供选择:
大鼠、小鼠尾注射固定器可用于大鼠、小鼠尾静脉注射或取血。
多种规格(尺寸)可选:
根据小鼠体重,选择合适的规格:15-25g,25-35g,35-50g,50-70g;
根据大鼠体重,选择合适的规格:150-250g;250-350g,350-450g,450-600g;
多种款式可选:
简易式固定器
主要规格: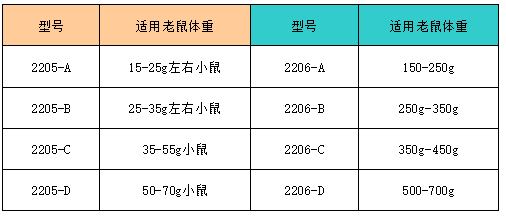
平板式大小鼠固定器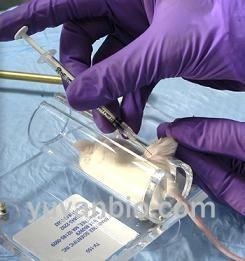
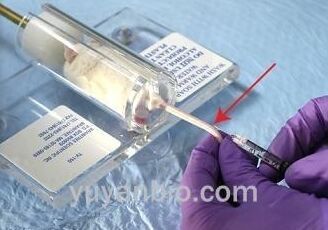
主要规格:
平板式固定器 主要特点:
结构简单,使用方便
有机玻璃制作,透明材质,方便观察动物的活动反应;
平板式设计,防滑处理;
固定方便,捏住鼠尾直接拉进鼠桶,盖上螺帽即可,省时省里;
清洗方便;
PC材质固定器
型号:2401
型号:2401-A
主要规格:
不锈钢固定器
主要规格:
小鼠分体式固定器
主要规格:
痛觉、触觉测试用老鼠固定器
可用于大鼠的面部、背部、腹部的刺痛实验;
可根据老鼠的体重订做合适的尺寸;
支架式固定架
主要特点:
尾注射部位带倾角,使用方便;
固定筒、架分开设计,更换不同尺寸的固定筒较为方便;
小鼠支架式固定器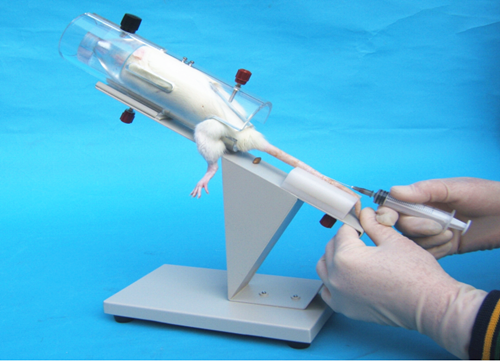
主要规格:
使用方法:
1.固定架的组装
(1)支架与底板 用配带在支架上的两个螺丝,将支架与底板连接,使用2号孔和3号孔。
(2)支架与鼠筒 将大鼠筒插在支架上端的燕尾槽中,插好后将下面的紧固螺丝旋紧。
2.调整
(1)装鼠调整 将滑动筒塞取下,将空管放平让大鼠自己从筒后端钻入,随后将滑动筒塞从前端塞上稍加固定,再把大鼠的两个后腿分别从出腿道槽中拉出,旋转腰臀压板调整螺丝,使腰臀压板压住鼠臂部使其后腿无法抽出,随后调整滑动筒塞和腰臀压板位置使其大鼠处在一个较舒适而又起到固定作用状态。
(2)鼠筒位置调整 鼠筒可在燕尾槽中进行位置滑动调整,以解决不同大小的鼠鼠尾长度不同的问题,定好后旋紧下端的螺丝。
(3)垫块位置的调整 鼠尾垫块可通过垫块下的调整螺丝进行左右调整,保证鼠尾居中,如果通过燕尾槽位置还不能达到调整尾长度问题,也可卸下鼠尾垫块改用另外两个螺孔进行调整。
3.使用
装鼠后各位置调整到合适状态,将鼠尾用左手的拇指与食指捏住拉直,左拧或右拧90°并以垫块为依托稳定,右手的注射器针尖(5号针头)延鼠尾血管方向(小于 30°),向前推进刺入后先缓注少量药液,如无阻力表示针头已进入静脉,可继续注入。注意此时左手一定不能松,右手推药时针头微向左下方用力,避免因药物刺激引起鼠尾摆动使针脱出,如长期给药时应从鼠尾的下五分之一处(约距尾尖3-4mm)开始向上打,保证血管上部的畅通。如习惯用食指中指扶上端,拇指无名指挟下端的注射方法时可将垫块卸掉(应注意保管)
如需进行尾静脉注射和采血,可选择:大鼠、小鼠尾静脉可视固定器
专门为小鼠、大鼠尾静脉注射和采血实验而设计
主要特点:
· 配备快装款式的鼠筒,可实现快速固定老鼠,稳定老鼠情绪,实现平稳注射;
· 使用按压方式阻断部分静脉,让尾部血管充盈;
· 使用特制的黄光照射鼠尾,使鼠尾的血管显现、易于观察;
· 在放大镜的辅助下将针尖刺入血管,做到有的放矢,不再是单凭手感的盲打;
· 易用判断:进针之后,摆动针头,看血管是否跟着针头摆动,就可以判断针头是否插在血管之中;
· 不需要上百次的反复锻炼,就能轻松进行小鼠尾静脉的穿刺和注射实验;

风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
- 作者
- 内容
- 询问日期
 文献和实验
文献和实验部分参考文献:
1、尹琴,梅凤,郭安琪,刘萍,易莉萍,范存愈,杨洁,余贻汉,张继先,凌瑞杰.呼吸机联合非暴露式气管滴注大鼠矽肺模型的建立[J].中国职业医学,2022,49(05):548-552.DOI:10.20001/j.issn.2095-2619.20221012.
2、曹曦元. BMMSCs通过上调肺内Tyro3的表达改善哮喘的机制研究[D].中国人民解放军海军军医大学,2022.DOI:10.26998/d.cnki.gjuyu.2022.000189.
3、汪跃国. Poldip2在LPS诱导的急性肺损伤中的作用及分子机制研究[D].安徽医科大学,2021.DOI:10.26921/d.cnki.ganyu.2021.001279.
4、陈婷. 防治非感染性呼吸系统炎症的吸入制剂研究[D].广东药科大学,2021.DOI:10.27690/d.cnki.ggdyk.2021.000097.
5、刘杰仪. 甘油三酯在哮喘气道炎症中的作用及机制探讨[D].南方医科大学,2021.DOI:10.27003/d.cnki.gojyu.2021.000549.
6、刘培培. 间充质干细胞来源外泌体抑制巨噬细胞焦亡减轻急性肺损伤及参附注射液治疗肺纤维化的研究[D].北京协和医学院,2021.DOI:10.27648/d.cnki.gzxhu.2021.000187.
7、金鹏峰. 不同分子量透明质酸的分离纯化及其在急性肺损伤中的作用研究[D].浙江工业大学,2020.DOI:10.27463/d.cnki.gzgyu.2020.001427.
8、黄帅波. 小鼠TGFβ-Smad2/3信号通路在心肌梗死后心脏重构中的作用及机制研究[D].中国人民解放军海军军医大学,2019.
9、李淼. 治疗雾霾致肺损伤的肺吸入给药系统研究[D].军事科学院,2018.
10、[1]陈珊珊. 人肺组织靶向甲强龙纳米脂质体对AE-IPF大鼠的疗效验证[D].苏州大学,2017.
这样呢?继续看图。这是总流量控制器,可以看到最大是 25*100 cc/min,也就是 2.5 L/min,对于 200 g 的大鼠或 500 g 以上的兔子麻醉会容易一点,因为它们体重大,对麻醉耐受比 20 g 的小鼠强。这个气流所能挥发出的麻醉药浓度对于 20 g 的小鼠来说就相当大了。所以,我遇到的第一个困难就是小鼠诱导完之后放在麻醉机鼻罩下小鼠呼吸就停止了,一旦发现小鼠呼吸停止,除非迅速气管插管,否者是很难复苏过来的。即使复苏过来了也不能再继续下面的实验了。当然也可以气管插管(这样就不怕麻醉
类动物手术器械一套、兔手术台、气管插管、动脉插管、膀胱漏斗或输尿管导管、注射器(2ml,20ml)及针头;生理盐水、20%葡萄糖溶液、1:10,000去甲肾上腺素、速尿、垂体后叶激素、尿糖试纸。 【实验步骤】 图25 尿量检测装置示意图 1. 仪器 连接及参数如图25所示,先将记滴器连至处理系统或多用仪的记滴输入,再用外接线将记滴信号和时间标记信号输入信号处理系统的外接信号输入插口,由处理系统分别记
,补充氯胺酮75~100mg/kg(ip)持续麻醉;阿托品20~30μg/kg腹腔注射,减少气道分泌物。 5、固定大鼠仰卧于手术台上。剪除颈部及胸部被毛。 6、纵形剪开颈部皮肤约1.5~2cm,分离皮下组织及肌肉。 7、显露气管及其上甲状腺腺体。 8、于腺体后方钝性分离气管并带线,注意勿损伤腺体及血管。 9、提起丝线,剪刀于气管环之间剪开气管半周。 10、行气管插管,接呼吸机。调整呼吸频率、吸呼比及潮气量(根据呼吸机使用指南及大鼠表现调节)。 11、胸骨左
 技术资料
技术资料