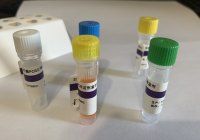
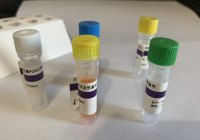
相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 库存:
130
- 英文名:
Streptococcus Suis Detection Kit
- 保质期:
1年
- 供应商:
上海晅科生物科技有限公司
- 保存条件:
-20℃
- 规格:
50T
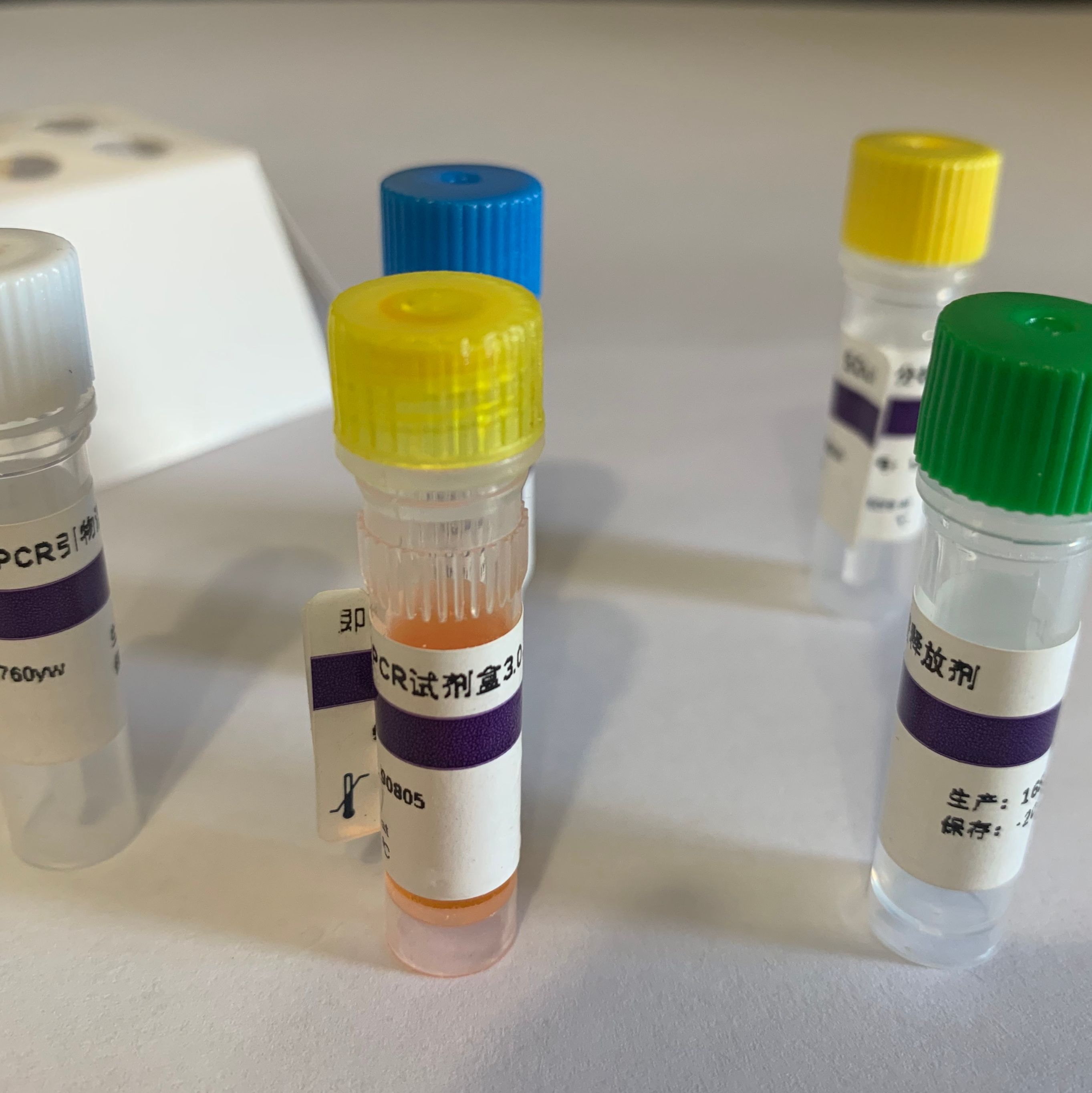
英文名称:Streptococcus Suis Detection Kit
猪链球菌(Streptococcus suis)是一种重要的人畜共患病病原体,可引起多种疾病,包括脑膜炎、关节炎、心内膜炎、败血症、肺炎等。根据细菌的荚膜多糖抗原可降之分为 35 个血清型,即 1~34 型和 1/2 型。本试剂盒适用于检测扁桃体、内脏或肌肉、咽拭子等样本中的猪链球菌通用型,用于猪链球菌通用型感染的辅助检测。
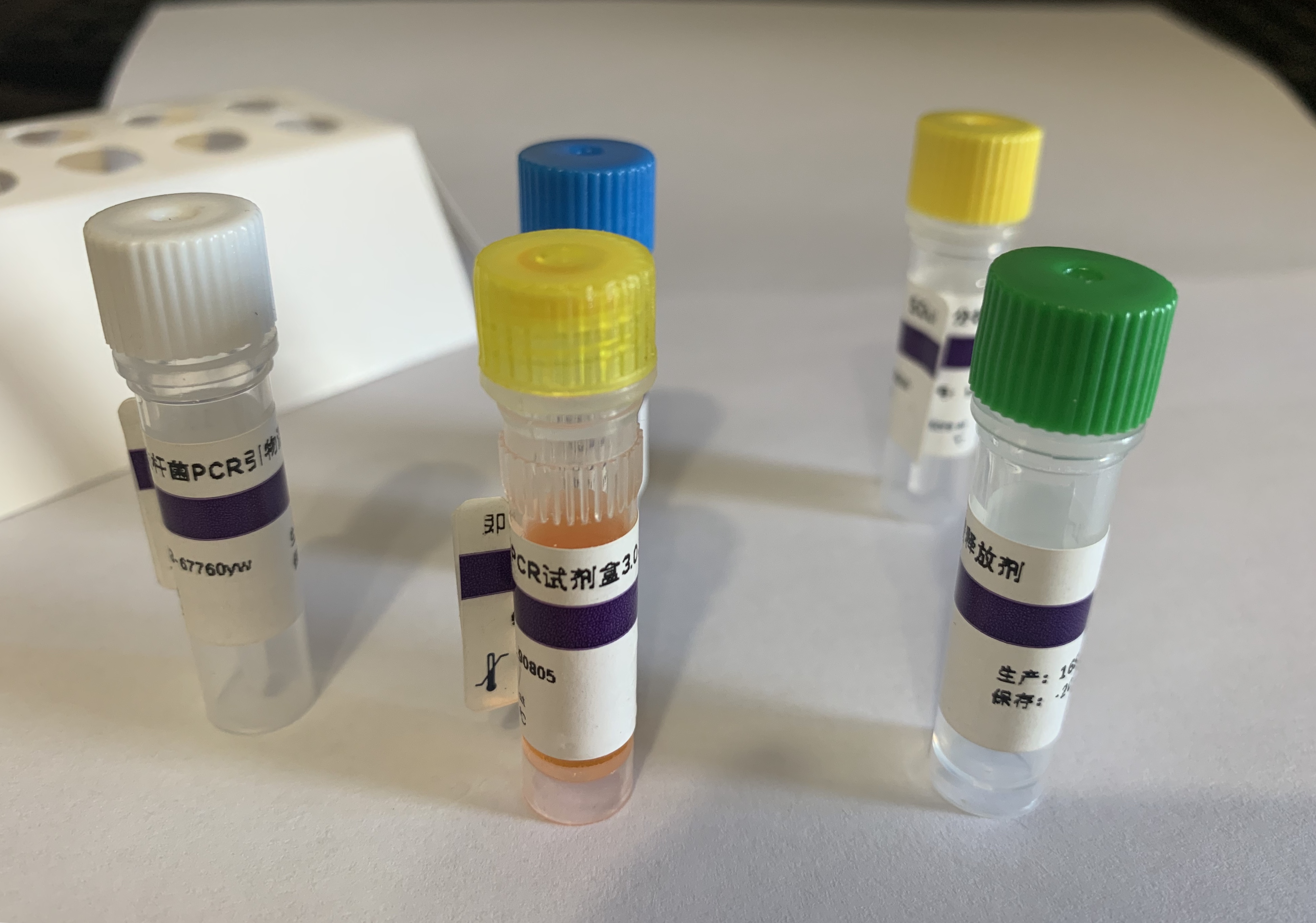
本试剂盒采用 TaqMan 探针法实时荧光 PCR 技术,设计一对猪链球菌通用型特异性引物,结合一条特异性探针,用荧光 PCR 技术对猪链球菌通用型的 DNA 进行体外扩增检测,用于对可疑感染病料的病原学检测。
猪链球菌通用型(SS-U)核酸检测试剂盒(探针法荧光PCR)试剂组成:
| 包装规格 | 50T/盒 | |
| SS-U 反应液 | 500μL×2 管 | |
| 酶液 | 50μL×1 管 | |
| SS-U 阳性质控品 | 50μL ×1 管 | |
| 阴性质控品 | 250μL ×1 管 |
储存条件及有效期:-20℃±5℃,避光保存、运输、反复冻融次数不超过 5 次,有效期 12 个月。
适用仪器:ABI7500、安捷伦 MX3000P/3005P、LightCycler、Bio-Rad、Eppendorf 等系列荧光定量 PCR 检测仪。
标本采集:扁桃体、内脏或肌肉样品采集:用无菌的剪刀和镊子剪取待检样品 1.0g 于研钵中充分研磨,再加 5mLPBS 混匀,然后将组织悬液转入无菌离心管中编号备用。 生猪拭子样品采集:咽喉拭子采样,采样时要将拭子深入喉头及上颚来回刮 3 次~5 次,取咽喉分泌液。其他样品采集可参考GB/T 19915.7-2005 采集方法。
保存和运输:采集或处理好的样品在 2℃~8℃条件下保存应不超过 24 h;若需长期保存,应放置-70℃以下保存,冻融不超过 3 次。
使用方法:
1. 样品处理(样本处理区)
1.1 样本前处理 扁桃体、内脏或肌肉样品:用无菌的剪刀和镊子剪取待检样品 1.0g 于研钵中充分研磨,再加 5mLPBS 混匀, 然后将组织悬液转入无菌离心管中编号备用。生猪拭子样品:咽喉拭子采样,采样时要将拭子深入喉头及上颚来回刮 3 次~5 次,取咽喉分泌液备用。其他样品前处理可参考 GB/T 19915.7-2005。
1.2 核酸提取 推荐采用公司生产的核酸提取试剂(离心柱法)进行核酸提取,请按照试剂说明书进行操作。
2. 试剂配制(试剂准备区) 根据待检测样本总数,设所需要的 PCR 反应管管数为 N(N=样本数+1 管阴性对照+1 管阳性对照;样品每满 10 份,多配制 1 份),每测试反应体系配制如下表: 试剂 SS-U 反应液 酶液 用量 19μL 1μL 将混合好的测试反应液分装到 PCR 反应管中,20μL/管。
3. 加样(样本处理区) 将步骤 1 提取的核酸、阳性质控品、阴性质控品各取 5μL,分别加入相应的反应管中,盖好管盖,混匀, 短暂离心。
4. PCR 扩增(核酸扩增区)
4.1 将待检测反应管置于荧光定量 PCR 仪反应槽内;
4.2 设置好通道、样品信息,反应体系设置为 25μL; 荧光通道选择: 检测通道(Reporter Dye)FAM, 淬灭通道(Quencher Dye)NONE,ABI 系列仪器请勿选择 ROX 参比荧光,选择 None 即可。
4.3 推荐循环参数设置: 步骤 循环数 温度 时间 收集荧光信号 1 1 cycle 95℃ 2min 否 2 45 cycles 95℃ 15sec 否 60℃ 30sec 是 5. 结果分析判定
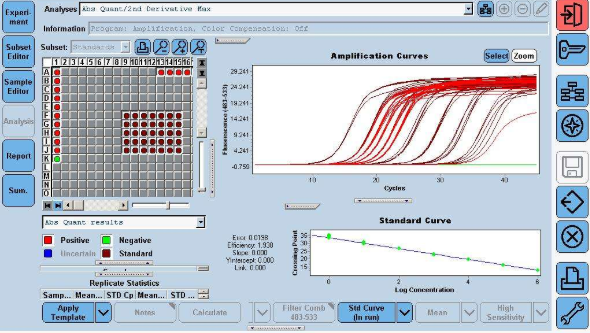
5.1 结果分析条件设定(请参照各仪器使用说明书进行设置,以分析 ABI7500 仪器为例) 反应结束后自动保存结果,根据分析后图像调节 Baseline 的 Start 值、End 值以及 Threshold 值(用户可根据实际情况自行调整,Start 值可设在 3~15、End 值可设在 5~20,使阈值线位于扩增曲线指数期,阴性质控品的扩增曲线平直或低于阈值线),点击 Analyze 自动获得分析结果。
5.2 结果判断 阳性:检测通道 Ct 值≤40,且曲线有明显的指数增长曲线; 阴性:样本检测结果 Ct 值>40 或无 Ct 值。
5.3 质控标准 阴性质控品:无特异性扩增曲线或无 Ct 值显示; 阳性质控品:扩增曲线有明显指数增长期,且 Ct 值≤32; 以上条件应同时满足,否则实验视为无效。
6. 检测方法的局限性
1. 样本检测结果与样本收集、处理、运送以及保存质量有关;
2. 样本提取过程中没有控制好交叉污染,会出现假阳性结果;
3. 阳性对照、扩增产物泄漏,会导致假阳性结果;
4. 病原体在流行过程中基因突变、重组,会导致假阴性结果;
5. 不同的提取方法存在提取效率差异,会导致假阴性结果;
6. 试剂运输,保存不当或试剂配制不准确引起的试剂检测效能下降,出现假阴性或定量检测不准确的结果;
7. 本检测结果仅供参考,如须确诊请结合临床症状以及其他检测手段。
注意事项
1. 所有操作严格按照说明书进行;
2. 试剂盒内各种组分使用前应自然融化,完全混匀并短暂离心;
3. 反应液应避光保存;
4. 反应中尽量避免气泡存在,管盖需盖紧;
5. 使用一次性吸头、一次性手套和各区专用工作服;
6. 样本处理、试剂配制、加样需在不同区进行,以免交叉污染;
7. 实验完毕后用 10%次氯酸或 75%酒精或紫外灯处理工作台和移液器;
8. 试剂盒里所有物品应视为污染物对待,并按照《微生物生物医学实验室生物安全通则》进行处理。
相关产品:
| 微量包涵体纯化试剂盒 |
| 大量包涵体纯化试剂盒 |
| 单链DNA制备试剂盒(5端磷酸标记-Lambda外切酶法) |
| SYBR Realtime Rolling Circle Amplification Kit (Bst DNA Polymerase)染料法实时RCA试剂盒(Bst法) |
| 单链DNA环化试剂盒 |
| Error-Prone Rolling Circle Amplification Kit (Bst)易错滚环扩增试剂盒(Bst法) |
| 2×RCA MasterMix(Rolling Cycle Amplification,滚环扩增)(停产,升级为221080-50) |
| 易错RCA滚环扩增试剂盒(phi29法) |
| Sarcosyl-PAGE电泳试剂盒(PEG修饰蛋白专用) |
| SDS-PAGE电泳试剂盒(双色) |
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验实时荧光定量 PCR 技术(Quantitative Real-time PCR,简称 qPCR)是在 PCR 扩增过程中,通过实时监测荧光信号的变化,达到对待检测样本中初始模板定量分析的方法。当前 qPCR 技术被广泛应用于临床疾病诊断,动物疾病监测,食品安全分析等领域。随着 2020 年新冠疫情在全球的蔓延,qPCR 技术更是因其检测通量高,速度快,操作简便等优势成为新冠病毒核酸检测的有效方法被众人所熟知。 那么为了得到可靠、准确的检测结果,我们需要注意哪些方面呢?其实决定一次实验成功
总的说来,荧光检测技术可大致分为两大类:通用型的荧光染料检测法和高特异性的荧光探针法。 前者主要是利用荧光染料(如SYBR Green I)与双链DNA分子结合发光的特性来指示扩增产物的增加,优点是:无需另外设计荧光探针 ,无需特别优化条件,简便易行,成本较低,能适用于任何一款定量 PCR 仪,缺点是专一性不如探针法; 而后者则利用荧光标记的特异性探针或者引物来识别模版,优点是特异性更高,适用于扩增序列专一检测(见下表),不过增加了荧光探针的成本。
光检测仪器透过PCR管壁能直接检测到荧光信号的波长和长度变化。 主要有以下优点: 1、探针特异性强,假阳性率低; 2、操作快速,不需要PCR后处理; 3、定量范围宽,HBV 0.4fg-4000fg/ml(102-106 Dane′s particle/ml); 4、闭管操作,PCR产物污染少; 5、灵敏度高。 主要方法有: 1、荧光探针法:进行荧光PCR检测时,要求荧光探针必须完全与靶基因互补,长度以20-30个碱基为宜,必要时3′端磷酸化封闭,以防在扩增时作为引物延伸。该方法利用Taq
 技术资料
技术资料暂无技术资料 索取技术资料