相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 库存:
180
- 英文名:
Avian Influenza Virus subtype N3 Detection Kit
- 保质期:
1年
- 供应商:
上海晅科生物科技有限公司
- 保存条件:
-20℃
- 规格:
50T
英文名称:Avian Influenza Virus subtype N3 Detection Kit
禽流感是禽类流行型感冒的简称,它是由甲型流感病毒的一种亚型(也称禽流感病毒)引起的一种急性传染病, 经变异后也能感染人类,被国际兽疫局定为甲类传染病。禽流感病毒(AIV)为正粘病毒科甲型流感病毒属,单股 负链 RNA 病毒。依据其外膜血凝素(H)和神经氨酸酶(N)蛋白可分为 H 亚型和 N 亚型,目前已发现 18 个 HA 和11 个 NA 亚型。 本试剂盒适用于检测拭子样品、气管、肺、脑、肠(包括内容物)、肝、脾、肾、心等组织脏器中 N3 亚型禽流感病毒 RNA,适用于 N3 亚型禽流感病毒感染的诊断、检疫、检测、监测和流行病学调查等。
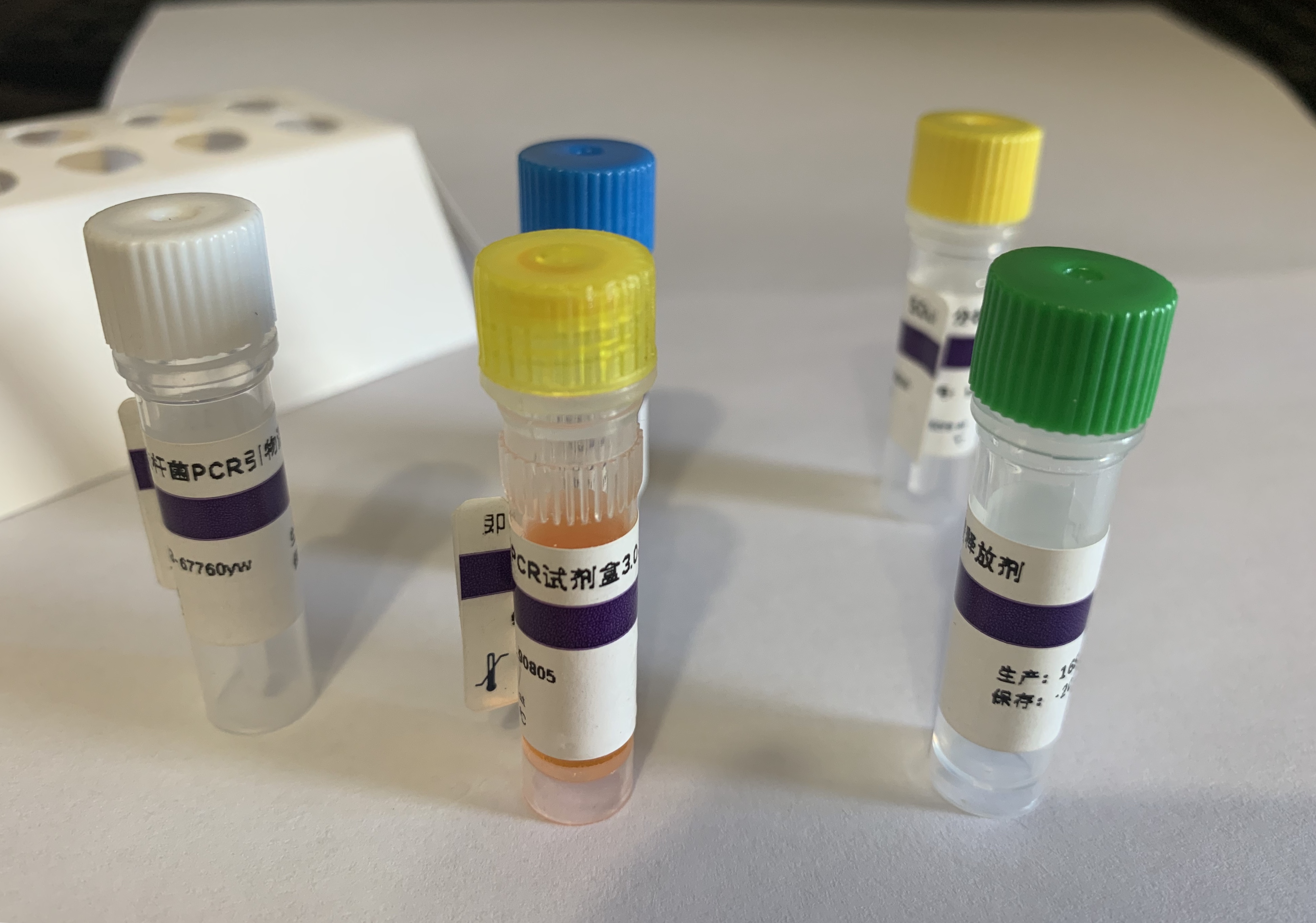
本试剂盒针对禽流感病毒 N3 亚型 NA 基因高度保守区域设计特异性引物和探针,用一步法荧光 RT-PCR 技术对禽流感病毒 N3 亚型 RNA 进行体外扩增检测,用于对可疑感染病料的病原学检测。
禽流感病毒 N3 亚型(AIV-N3)核酸检测试剂盒(探针法荧光PCR)试剂组成:
| 包装规格 | 25T/盒 | 50T/盒 |
| AIV-N3 反应液 | 500μL×1 管 | 500μL×2 管 |
| 酶液 | 25μL×1 管 | 50μL×1 管 |
| AIV-N3 阳性质控品 | 250μL ×1 管 | 250μL ×1 管 |
| 阴性质控品 | 250μL ×1 管 | 250μL ×1 管 |
储存条件及有效期:-20℃±5℃,避光保存、运输、反复冻融次数不超过 5 次,有效期 12 个月。
适用仪器:ABI7500、安捷伦 MX3000P/3005P、LightCycler、Bio-Rad、Eppendorf 等系列荧光定量 PCR 检测仪。
标本采集:拭子样品:采集咽喉拭子时将拭子每人喉头及上颚裂来回刮 2 次~3 次并旋转,取分泌液;采集泄殖腔拭子时将拭子深入泄殖腔至少旋转 3 圈并沾取少量粪便;将采样后的拭子分别放入盛有 1.2 mL 样品稀释液(配制方法见 GB/T 18936-2020 高致病性禽流感诊断技术)的 2 mL 采样管中,编号并填写相应采样单。 发病禽鸟可无菌采集气管、肺、脑、肠(包括内容物)、肝、脾、肾、心等组织脏器,装入 15 mL 或 50 mL 带螺口的有机材料保存管中,编号并填写相应采样单。
保存和运输:采集或处理好的样品在 2℃~8℃条件下保存应不超过 24 h;若需长期保存,应放置-70℃以下保存,冻融不超过 3 次。
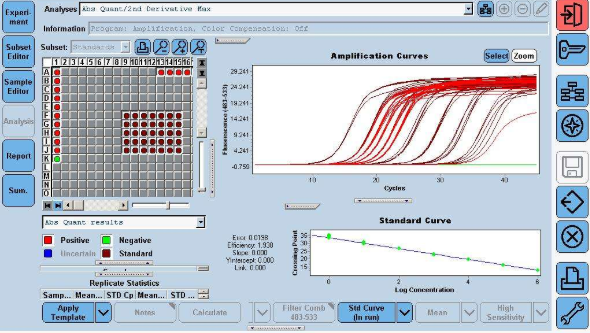
使用方法:
1. 样品处理(样本处理区) 1.1 样本前处理 将棉拭子充分捻动、挤干后弃去拭子;粪便,研碎的组织加 PBS 充分研磨,按照 1g 组织加 10 mL PBS 的比例配成悬液。样品液经 3 000 r/min 离心 10 min,取上清作为核酸检测材料。 1.2 核酸提取 推荐采用公司生产的核酸提取或纯化试剂(磁珠法或离心柱法)进行核酸提取, 请按照试剂说明书进行操作。
2. 试剂配制(试剂准备区) 根据待检测样本总数,设所需要的 PCR 反应管管数为 N(N=样本数+1 管阴性对照+1 管阳性对照;反应管数每满 10 份,多配制 1 份),每测试反应体系配制如下表: 试剂 AIV-N3 反应液 酶液 用量 19μL 1μL 将混合好的测试反应液分装到 PCR 反应管中,20μL/管。
3. 加样(样本处理区) 将步骤 1 提取的核酸、阳性质控品、阴性质控品各取 5μL,分别加入相应的反应管中,盖好管盖,混匀, 短暂离心。
4. PCR 扩增(核酸扩增区) 4.1 将待检测反应管置于荧光定量 PCR 仪反应槽内; 4.2 设置好通道、样品信息,反应体系设置为 25μL;荧光通道选择:检测通道(ReporterDye)FAM,淬灭通道 (QuencherDye)NONE,ABI 系列仪器请勿选择 ROX 参比荧光,选择 None 即可。 4.3 推荐循环参数设置: 步骤 循环数 温度 时间 收集荧光信号 1 1 cycle 50℃ 10min 否 2 1 cycle 95℃ 2min 否 3 45 cycles 95℃ 15sec 否 60℃ 30sec 是
5. 结果分析判定 5.1 结果分析条件设定(请参照各仪器使用说明书进行设置,以分析 ABI7500 仪器为例) 反应结束后自动保存结果,根据分析后图像调节 Baseline 的 Start 值、End 值以及 Threshold 值(用户可根据实际情况自行调整,Start 值可设在 3~15、End 值可设在 5~20,使阈值线位于扩增曲线指数期,阴性质控品的扩增曲线平直或低于阈值线),点击 Analyze 自动获得分析结果。 5.2 结果判断 阳性:检测通道 Ct 值≤40,且曲线有明显的指数增长曲线; 阴性:样本检测结果无 Ct 值,且无特异性扩增曲线; 可疑:样本检测结果 40<Ct 值≤45,建议重复检测,如果检测通道仍为 40
6. 检测方法的局限性
1. 样本检测结果与样本收集、处理、运送以及保存质量有关;
2. 样本提取过程中没有控制好交叉污染,会出现假阳性结果;
3. 阳性对照、扩增产物泄漏,会导致假阳性结果;
4. 病原体在流行过程中基因突变、重组,会导致假阴性结果;
5. 不同的提取方法存在提取效率差异,会导致假阴性结果;
6. 试剂运输,保存不当或试剂配制不准确引起的试剂检测效能下降,出现假阴性或定量检测不准确的结果;
7. 本检测结果仅供参考,如须确诊请结合临床症状以及其他检测手段。
注意事项
1. 所有操作严格按照说明书进行;
2. 试剂盒内各种组分使用前应自然融化,完全混匀并短暂离心;
3. 反应液应避光保存;
4. 反应中尽量避免气泡存在,管盖需盖紧;
5. 使用一次性吸头、一次性手套和各区专用工作服;
6. 样本处理、试剂配制、加样需在不同区进行,以免交叉污染;
7. 实验完毕后用 10%次氯酸或 75%酒精或紫外灯处理工作台和移液器;
8. 试剂盒里所有物品应视为污染物对待,并按照《微生物生物医学实验室生物安全通则》进行处理。
相关产品:
| 脑膜炎奈瑟菌通用型(NM-U)核酸检测试剂盒(荧光PCR法) |
| 脑膜炎奈瑟菌W135群(NM-W135)核酸检测试剂盒(荧光PCR法) |
| 双歧杆菌(BD)核酸检测试剂盒(荧光PCR法) |
| 百日咳杆菌(BP)核酸检测试剂盒(荧光PCR法) |
| 产肠毒素性大肠杆菌(ETEC)核酸检测试剂盒(荧光PCR法) |
| 肠集聚性大肠杆菌(EAEC)核酸检测试剂盒(荧光PCR法) |
| 肠侵袭性大肠杆菌(EIEC)核酸检测试剂盒(荧光PCR法) |
| 肉毒杆菌A型(CB-A)核酸检测试剂盒(荧光PCR法) |
| 肉毒杆菌B型(CB-B)核酸检测试剂盒(荧光PCR法) |
| 肉毒杆菌E型(CB-E)核酸检测试剂盒(荧光PCR法) |
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验实时荧光定量 PCR 技术(Quantitative Real-time PCR,简称 qPCR)是在 PCR 扩增过程中,通过实时监测荧光信号的变化,达到对待检测样本中初始模板定量分析的方法。当前 qPCR 技术被广泛应用于临床疾病诊断,动物疾病监测,食品安全分析等领域。随着 2020 年新冠疫情在全球的蔓延,qPCR 技术更是因其检测通量高,速度快,操作简便等优势成为新冠病毒核酸检测的有效方法被众人所熟知。 那么为了得到可靠、准确的检测结果,我们需要注意哪些方面呢?其实决定一次实验成功
(PTMs) 进一步促进了从基因组水平到蛋白质组复杂性的增加。PTMs 是一种化学修饰,在功能蛋白质组中发挥关键作用,因为它们调节活性、定位以及与其他细胞分子(如蛋白质、核酸、脂质和辅助因子)的相互作用。图示:翻译后修饰是增加蛋白质组多样性的关键机制。虽然基因组包含 20,000 至 25,000 个基因,但蛋白质组估计包含超过 100 万个蛋白质。转录和 mRNA 水平的变化增加了转录组相对于基因组的大小,无数不同的翻译后修饰相对于转录组和基因组都以指数方式增加了蛋白质组的复杂性。此外,人类
的基因重组。迄今为止,全球流行的HIV根据血清学反应和病毒核酸序列测定可分为二型,HIV-1型和HIV-2型。在HIV-1型内,根据编码包膜蛋白的env基因和编码壳蛋白的gag基因序列的同源性又进一步分为三个组,M组(main即主要组)、O组(outline即外围组)和N组(new,ornon-M,non-O新组或非M非O组),M组内又可分为A-J10个亚型。在HIV-1和HIV-2二型之间,其核苷酸序列只有45%的同源性。在HIV-1型内,各亚型之间的基因离散率是20-35%、同一亚型内的基因离散
 技术资料
技术资料暂无技术资料 索取技术资料