相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 品系:
细胞系
- 供应商:
中乔新舟
- 库存:
1000
- 英文名:
CCRF-SB
- 生长状态:
悬浮
- 年限:
液氮长期
- 运输方式:
常温运输
- 物种来源:
人
- 规格:
5 x 10^5 cells/vial
|
产品名称 |
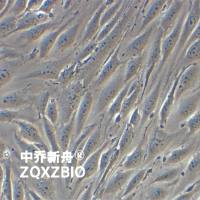
CCRF-SB人B淋巴母细胞 |
|
货号 |
ZQ1117 |
|
产品介绍 |
CCRF-SB是一种人B淋巴母细胞系,最初从一位11岁患有急性淋巴细胞白血病(ALL)的男孩的外周血中分离出来。这种细胞系在白血病和免疫学研究中具有重要的应用价值。它们可用于免疫系统紊乱和免疫学研究。 |
|
种属 |
人 |
|
性别/年龄 |
男/11岁 |
|
组织 |
外周血 |
|
疾病 |
急性淋巴细胞白血病 |
|
细胞类型 |
B淋巴母细胞 |
|
形态学 |
淋巴母细胞 |
|
生长方式 |
悬浮 |
|
培养基和添加剂 |
DMEM (中乔新舟 货号:ZQ-100)+10%胎牛血清(中乔新舟 货号:ZQ500-A)+1%P/S(中乔新舟 货号:CSP006) |
|
推荐完全培养基货号 |
ZM1117 |
|
生物安全等级 |
BSL-1 |
|
培养条件 |
95%空气,5%二氧化碳;37℃ |
|
STR位点信息 |
Amelogenin :X,Y CSF1PO :10,12 D2S1338 :17,18 D3S1358 :16,17 D5S818: 11,12 D7S820 :11,12 D8S1179 :9,15 D13S317: 10,12 D16S539: 9,13 (ATCC=CCL-120; PubMed=25877200) :13 (JCRB=IFO50026; JCRB=JCRB0032) D18S51: 9,14 D19S433: 14,16 D21S11: 27,28 FGA :25 Penta D: 9,12 Penta E:6,13 TH01 :9,10 TPOX: 8 vWA :18 |
|
抗原表达/受体表达 |
*** |
|
基因表达 |
*** |
|
保藏机构 |
ATCC; CCL-120 |
|
供应限制 |
仅供科研使用 |
上海中乔新舟生物科技有限公司成立于2011年,历经十多年发展,主要专注于细胞生物学产品的研究和开发,专注于为药企、各类科研机构及CRO企业提供符合标准规范的细胞培养服务、细胞培养基、细胞检测试剂盒、细胞培养试剂,胎牛血清和细胞生物学技术服务等。
公司一直致力于为高等院校、研究机构、医院、CRO及CDMO企业提供细胞培养完整解决方案,这些产品旨在满足细胞培养的多样需求,确保实验和研究的有效进行。引用中乔新舟(ZQXZBIO)产品和服务的文献超数千篇。

产品服务
细胞资源:原代细胞、细胞株、干细胞、示踪细胞、耐药株细胞、永生化细胞等基因工程细胞。
试剂产品:胎牛血清、完全培养基(适用于原代细胞及细胞株)、无血清培养基、基础培养基、细胞转染试剂、重组因子、胰酶和双抗等等细胞培养所有实验相关产品。
技术服务:稳转株构建、原代细胞分离、特殊培养基定制服务、细胞检测等。

目前产品已经畅销国内30多个省市,与客户建立长期的合作伙伴关系,共同实现成功。全体员工将不懈努力,继续为科研人员提供优良的产品和服务,致力成为全球细胞培养领域的参与者。
企业愿景
致力于成为国内细胞培养基产业的佼佼者,生物医药领域上游原材料的优良提供商。
企业使命
成长为专业细胞系及原代细胞培养供应商、专业细胞培养基及培养试剂生产商。
企业荣誉


风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验
DOI=10.1007/BF02618370
Stulberg C.S., Coriell L.L., Kniazeff A.J., Shannon J.E.
The animal cell culture collection.
In Vitro 5:1-16(1970)
PubMed=4991454; DOI=10.1016/0014-4827(79)90504-4
Adams R.A., Pothier L., Flowers A., Lazarus H., Farber S., Foley G.E.
The question of stemlines in human acute leukemia. Comparison of cells isolated in vitro and in vivo from a patient with acute lymphoblastic leukemia.
Exp. Cell Res. 62:5-10(1970)
PubMed=4363409; DOI=10.1084/jem.139.5.1070
Kaplan J., Shope T.C., Peterson W.D. Jr.
Epstein-Barr virus-negative human malignant T-cell lines.
J. Exp. Med. 139:1070-1076(1974)
PubMed=4523807; DOI=10.1007/BF02616012
Lazarus H., Barell E.F., Oppenheim S.O., Krishan A.
Divergent properties of two human lymphocytic cell lines isolated from a single specimen of peripheral blood.
In Vitro 9:303-310(1974)
PubMed=62390; DOI=10.1111/j.1365-3083.1976.tb03029.x
Yount W.J., Utsinger P.D., Hutt L.M., Buchanan P.D., Korn J.H., Fuller C.R., Logue M., Pagano J.S.
Subpopulations of human lymphoblastoid cell lines. Correlation with the expression of surface receptors and content of Epstein-Barr virus genome.
Scand. J. Immunol. 5:795-810(1976)
PubMed=1086134
Kaplan J., Peterson W.D. Jr.
Detection of T-cell lymphoma-associated antigens on cord blood lymphocytes and phytohemagglutinin-stimulated blasts.
Cancer Res. 36:3471-3475(1976)
PubMed=3335022
Alley M.C., Scudiero D.A., Monks A., Hursey M.L., Czerwinski M.J., Fine D.L., Abbott B.J., Mayo J.G., Shoemaker R.H., Boyd M.R.
Feasibility of drug screening with panels of human tumor cell lines using a microculture tetrazolium assay.
Cancer Res. 48:589-601(1988)
CLPUB00447
Mulivor R.A., Suchy S.F.
1992/1993 catalog of cell lines. NIGMS human genetic mutant cell repository. 16th edition. October 1992.
(In) Institute for Medical Research (Camden, N.J.) NIH 92-2011; pp.1-918; National Institutes of Health; Bethesda (1992)
PubMed=8316623; DOI=10.2307/3578190
Evans H.H., Ricanati M., Horng M.-F., Jiang Q.-Y., Mencl J., Olive P.L.
DNA double-strand break rejoining deficiency in TK6 and other human B-lymphoblast cell lines.
Radiat. Res. 134:307-315(1993)
DOI=10.1016/B978-0-12-221970-2.50457-5
Drexler H.G.
The leukemia-lymphoma cell line factsbook.
(In) ISBN 9780122219702; pp.1-733; Academic Press; London (2001)
PubMed=20215515; DOI=10.1158/0008-5472.CAN-09-3458
Rothenberg S.M., Mohapatra G., Rivera M.N., Winokur D., Greninger P., Nitta M., Sadow P.M., Sooriyakumar G., Brannigan B.W., Ulman M.J., Perera R.M., Wang R., Tam A., Ma X.-J., Erlander M., Sgroi D.C., Rocco J.W., Lingen M.W., Cohen E.E.W., Louis D.N., Settleman J., Haber D.A.
A genome-wide screen for microdeletions reveals disruption of polarity complex genes in diverse human cancers.
Cancer Res. 70:2158-2164(2010)
PubMed=25485619; DOI=10.1038/nbt.3080
Klijn C., Durinck S., Stawiski E.W., Haverty P.M., Jiang Z.-S., Liu H.-B., Degenhardt J., Mayba O., Gnad F., Liu J.-F., Pau G., Reeder J., Cao Y., Mukhyala K., Selvaraj S.K., Yu M.-M., Zynda G.J., Brauer M.J., Wu T.D., Gentleman R.C., Manning G., Yauch R.L., Bourgon R., Stokoe D., Modrusan Z., Neve R.M., de Sauvage F.J., Settleman J., Seshagiri S., Zhang Z.-M.
A comprehensive transcriptional portrait of human cancer cell lines.
Nat. Biotechnol. 33:306-312(2015)
PubMed=25877200; DOI=10.1038/nature14397
Yu M., Selvaraj S.K., Liang-Chu M.M.Y., Aghajani S., Busse M., Yuan J., Lee G., Peale F.V., Klijn C., Bourgon R., Kaminker J.S., Neve R.M.
A resource for cell line authentication, annotation and quality control.
Nature 520:307-311(2015)
PubMed=26589293; DOI=10.1186/s13073-015-0240-5
Scholtalbers J., Boegel S., Bukur T., Byl M., Goerges S., Sorn P., Loewer M., Sahin U., Castle J.C.
TCLP: an online cancer cell line catalogue integrating HLA type, predicted neo-epitopes, virus and gene expression.
Genome Med. 7:118.1-118.7(2015)
PubMed=29892436; DOI=10.1098/rsos.172472
Shioda S., Kasai F., Watanabe K., Kawakami K., Ohtani A., Iemura M., Ozawa M., Arakawa A., Hirayama N., Kawaguchi E., Tano T., Miyata S., Satoh M., Shimizu N., Kohara A.
Screening for 15 pathogenic viruses in human cell lines registered at the JCRB Cell Bank: characterization of in vitro human cells by viral infection.
R. Soc. Open Sci. 5:172472-172472(2018)
PubMed=35124168; DOI=10.1016/j.jsbmb.2022.106068
Tamai M., Kasai S., Akahane K., Thu T.N., Kagami K., Komatsu C., Abe M., Watanabe A., Goi K., Miyake K., Inaba T., Takita J., Goto H., Minegishi M., Iwamoto S., Sugita K., Inukai T.
Glucocorticoid receptor gene mutations confer glucocorticoid resistance in B-cell precursor acute lymphoblastic leukemia.
J. Steroid Biochem. Mol. Biol. 218:106068.1-106068.12(2022)
PubMed=35354797; DOI=10.1038/s41467-022-29224-5
Leo I.R., Aswad L., Stahl M., Kunold E., Post F., Erkers T., Struyf N., Mermelekas G., Joshi R.N., Gracia-Villacampa E., Ostling P., Kallioniemi O.-P., Pokrovskaja Tamm K., Siavelis I., Lehtio J., Vesterlund M., Jafari R.
Integrative multi-omics and drug response profiling of childhood acute lymphoblastic leukemia cell lines.
Nat. Commun. 13:1691.1-1691.19(2022)
 技术资料
技术资料暂无技术资料 索取技术资料