相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 库存:
6T
- 英文名:
Co-Immunoprecipitation (Co-IP)Kit For Plant
- 保质期:
参照shuomingshu
- 供应商:
武汉金开瑞生物工程有限公司
- 保存条件:
参照shuomingshu
Co-Immunoprecipitation (Co-IP)Kit For Plant
货号:JKR23001P
实验原理
免疫共沉淀(Co-Immunoprecipitation)是利⽤抗原与抗体之间的专⼀性作⽤为基础,从 ⽽⽤于研究蛋⽩质与蛋⽩质之间相互作⽤的⼀种⽅法。抗体与细胞裂解液或表达上清 中相应的蛋⽩结合后,再与ProteinA/G偶联的Sepharose或MagneticBeads孵育,通 过离⼼或者借助磁⼒架获得ProteinA/G珠⼦-抗体-⽬的蛋⽩复合物,在⾼温及还原剂的 作⽤下,抗原与抗体解离,收集上清,上清中包括抗体、⽬的蛋⽩和少量的杂蛋⽩。
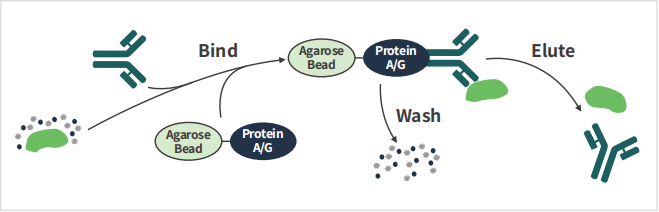
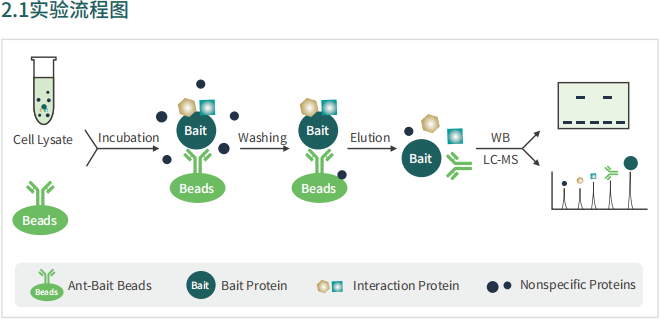
实验流程

试剂盒组分、操作步骤等更多细节请查看zuixinban说明书
CO-IP实验的应用
- 蛋白质相互作用研究:CO-IP实验的核心应用在于检测蛋白质之间的相互作用。通过识别并富集与目标蛋白质特异性结合的抗体,该技术可以进一步分析目标蛋白质与其互作伴侣的身份和相互作用模式。这对于理解细胞内的信号转导途径、细胞周期调控等生物过程至关重要。
- 互作位点分析:利用CO-IP实验,科学家可以确定蛋白质相互作用的具体位点,这有助于理解蛋白质复合物如何形成和发挥作用,进而为药物设计或治疗策略提供指导。
- 疾病机制研究:CO-IP实验可用于研究疾病发生发展过程中蛋白质相互作用的变化。通过比较正常细胞和疾病细胞中蛋白质相互作用模式的差异,可以揭示疾病的发生机制,为疾病的诊断和治疗提供新的思路。
- 药物靶点筛选:在药物研发过程中,CO-IP实验可以用于筛选潜在的药物靶点。通过干扰或增强特定蛋白质相互作用,可以评估药物对细胞功能的影响,从而筛选出具有治疗潜力的药物候选物。
CO-IP实验的共同验证
除了CO-IP(免疫共沉淀)实验外,还有以下几种实验方法可以在植物样本中验证蛋白互作:
- 双分子荧光互补(BiFC):这是一种蛋白质片段互补技术,将荧光蛋白多肽链切开并形成不发荧光的N-和C-末端两个多肽片段,然后将两个蛋白的基因分别连在具有荧光蛋白N端和C端的载体上,形成融合蛋白。当两个蛋白互作时,它们可以形成完整的荧光蛋白,并在特定光下激发荧光,从而判断蛋白是否互作。
- 酵母双杂(Y2H):将要验证互作的蛋白对应基因分别连在具有转录激活域和转录结合域的AD BD载体上,共转酵母。如果两个蛋白互作,它们能够形成完整的GAL4结构域,激活下游报告基因,从而通过酵母在对应缺陷培养基上的生长情况来判断是否互作。
- Pull-down:这种方法通常使用GST融合蛋白作为诱饵蛋白,将其与谷胱甘肽标记的珠子结合,然后从目标蛋白溶液中捕获与之相互作用的蛋白。洗脱结合物后,通过电泳分析可以证实两种蛋白间的相互作用。
- 荧光素酶互补实验(LCA):这是一种将萤光素酶蛋白拆分为N端和C端两个功能片段的实验方法。将待检测的两个目标蛋白分别与这两个片段融合,如果两个目标蛋白相互作用,则萤光素酶的N端和C端片段可以在空间上足够靠近并正确组装,从而发挥萤光素酶活性并产生荧光。
这些方法各有特点,可以根据具体的研究目的和实验条件选择适合的方法。
常见问题
Q1:通过Co-IP后WB验证发现,虽然可见目的条带,但是背景很高:
多方面原因造成:
1.由于非特异蛋白结合导致背景高,若要避色非特异性蛋白结合,则需要在无血清溶液中裂解细胞,且在免疫沉淀前用protein(A/G)珠子预洗,在免疫沉淀后增加漂洗次数和盐碱度(高盐或去垢剂)。
2.实验仪器或试剂被污染,使用洁净的仪器及试剂。
3.转移膜上的非特异吸附导致背景高,实验操作过程中戴手套,使用镊子来取,不要接触膜转移面。
4.制备样品中可能有不完全溶解的大的蛋白复合体,则在制备样品后进行短暂超声处理(3次,每次5秒钟 ),然后离心,取上清后进行后续试验。
5.洗涤不彻底,则需要多次洗涤,并增加洗涤液中的NaCl和去垢剂浓度。
6.可能有非特异性蛋白吸附于珠子上,则须进行Preclearing以排非特异性吸附。
7.抗体本⾝待异性不好可能导致背景高,则须选择合适的抗体,可以考虑单抗。
8.使用了过多的细胞或组织进行裂解导致背景高,则须减少样本量,推荐100- 500μg细胞裂解液。
9.蛋白降解也可能出现高背景的情况,尽量使用新鲜制备的样品。
Q2:通过Co-IP后WB验证发现,没有想要的目的条带?
1.有可能是样品被蛋白酶降解,对应的策略是需要添加蛋白酶抑制剂,所有操作保持4℃以下冰上操作并防止冻融。
2.有可能是抗体浓度太低导致条带较浅,则需要调整IP或WB抗体浓度,必要时设立浓度梯度,摸索最佳浓度。
3.抗体亲和力太低,选用适合于IP或者WB的抗体。
4.有的IP抗体未与磁珠结合,这种情况需选用适合IP的磁珠。
5.若Tag未暴露在融合蛋白构象的表面,则需改变Tag融合表达部位。
6.裂解液盐碱度太高,需用低盐碱度的裂解液。
7.抗体选择不当,更换抗体。
Q3:在进行CO-IP实验时,如何选择抗体?
解析:抗体的选择对于CO-IP实验的成功至关重要。首先,应确保抗体具有较高的特异性和亲和力。其次,为了避免假阳性结果,最好选择两个不同种源的抗体进行实验。这样可以排除因抗体与珠子或检测试剂的非特异性结合而导致的干扰。
Q4:CO-IP实验中,为什么有时无法检测到预期的蛋白质互作?
解析:这可能是由于胞内蛋白互作水平较低或没有互作。此时,可以尝试增加蛋白裂解物或进行诱导处理以提高互作水平。同时,也可能是由于细胞裂解液使用不当或目的蛋白未被有效洗脱。确保使用合适的裂解液和洗脱液,并优化洗脱条件,可以提高蛋白质的互作检测效率。
Q5:CO-IP实验结果不稳定,如何处理?
解析:实验结果的不稳定性可能由多种因素引起,如样品处理、抗体质量、实验操作等。为了提高实验结果的稳定性,可以优化样品处理过程,确保蛋白质的稳定性和活性;同时,选择高质量的抗体并严格按照操作说明进行实验;此外,多次重复实验并统计分析结果也是提高稳定性的有效方法。
Q6:如何避免CO-IP实验中的假阳性结果?
解析:为了避免假阳性结果,可以采取多种措施。例如,设置阴性对照实验,利用抗体对应的不含靶标蛋白的蛋白进行处理,以排除抗体抗原对实验的影响。此外,优化实验条件,如减少洗涤次数、降低洗涤强度等,也可以减少非特异性结合的可能性。
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验 技术资料
技术资料










