大多数蛋白质都是利用重组表达技术进行制备的,在克隆的过程中,一些肽类和蛋白质被广泛的用于生产重组蛋白,它们与目的蛋白融合表达,以便于目的蛋白的表达、检测、示踪和纯化。这类多肽或蛋白,被称为标签蛋白(Protein Tag),标签蛋白的种类有很多,如:His、GST、MBP、Strep-Ⅱ、Flag标签等,其中由于His-tag的分子量较小、免疫原性低、洗脱条件温和、可构建双标签系统等优点被广泛应用。
01、Ni亲和原理
金属螯合亲和技术作为一种蛋白质分离纯化的高效方法,它基于各种蛋白质分子的组氨酸、半胱氨酸、色氨酸等的残基与许多过渡金属离子发生不同程度的配位结合的特性,利用螯合剂将金属离子固定在基质上,常用的螯合剂有亚氨基二乙酸(IDA)、次氮基三乙酸(NTA)、N,N,N-三(羧甲基)-(TED)等。三种螯合剂的比较如下表:
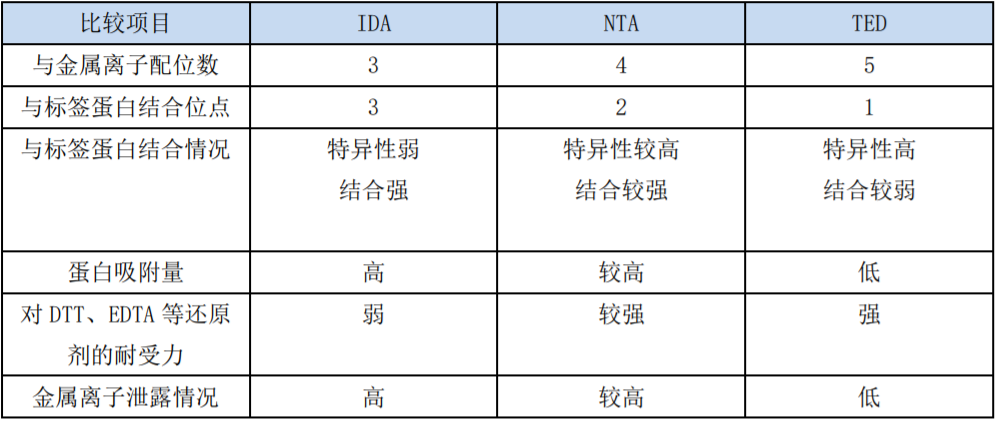
常用到的固定金属离子有Cu2+、Co2+、Ni2+、Zn2+等,其相对亲和性和特异性见下图:
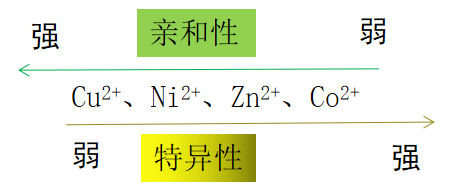
图1、过渡金属离子的亲和性和特异性比较
以IDA螯合剂为例,组氨酸(His)的残基上带有一个咪唑基团,可以和Ni2+,Co2+等固定金属离子形成配位键而选择性的结合在金属离子上,因此带有组氨酸标签的蛋白在经过键合了金属离子的层析介质时可以选择性的结合在介质上,而其他的杂质蛋白则不能结合或者仅能微弱结合。结合在介质上的HIS标签蛋白可以通过提高缓冲液中的咪唑浓度进行竞争性洗脱,从而得到较高纯度的HIS标签蛋白,同理半胱氨酸(Cys)残基上的巯基、色氨酸(Trp)残基上的吲哚基也可以Ni2+,Co2+等过渡金属离子形成配位键而选择性的结合在金属螯合介质上,his-tag的吸附、洗脱过程示意图如下:


图2、金属螯合层析的分离原理
针对His标签蛋白的纯化,纳微提供多种解决方案:包括预螯合金属离子的NW Rose®Ni FF、NW Rose®TED FF、Uni®IDA-80Ni、Uni®NTA-80Ni和Uni®TED-80Ni,也包括可用于金属离子螯合的NW Rose®IMAC FF、Uni®IDA-80L、Uni®NTA-80L和Uni®TED-80L等多种填料。
02、纳微层析预装柱
纳微科技也可提供多种规格层析预装柱,包括NmTRAP系列、NmSCREEN系列、NmPREP系列、NmVALID系列、NmVALID Pro系列、NmLOAD系列以及中压动态轴向压缩玻璃柱EZPacking 50/500等,产品可覆盖生物医药领域不同层析阶段,包括填料筛选、工艺优化与验证、小规模工艺放大与样品制备,预装柱性能优良,柱床稳定,可直接将预装柱连接到各种层析系统中使用,避免了装柱的繁琐步骤,提高工作效率。

图3、纳微全系列预装柱展示图
03、案例分享
实验条件:


图4、NmTRAP 1mL,NW Rose®Ni FF亲和捕获层析图
收集馏分进行电泳分析:

经灰度分析目的蛋白纯度可达83.0%,回收率90%。
04、His-tag融合蛋白纯化中的常见问题
①.标签蛋白与层析介质不结合,可能原因和解决方法:
a:样品前处理不到位,如:大肠杆菌表达的His-tag蛋白可能为:包涵体、胞内可溶。不同的表达方式样品处理的方法不同,可通过SDS-PAGE电泳确定样品或采用其他方式破碎细胞。
b:样品或平衡缓冲液不合适,要确保缓冲液中螯合剂、还原剂和咪唑的浓度不能太高,否则目的样品不能结合到层析介质上。
c:样品的粘度以及核酸的含量的影响,过滤、稀释样品或使用超声、核酸酶来减少核酸的影响。
d:可能蛋白的表达His-tag没有完全暴露,重新构建His标签。
②.His标签蛋白结合在层析介质上很难洗脱下来
a:洗脱条件太温和,增加洗脱缓冲液中咪唑的浓度。
b上样量太大,导致蛋白沉积在层析介质上,减少上样量或降低样品浓度。
③.层析介质变白、变黑、变黄
a:预螯合金属离子的层析介质变白说明 Ni 离子脱落,需要 Ni 离子再生;
b:层析介质变黑,一般是没有脱Ni 的情况下使用还原剂或NaOH,会导致层析介质损坏,无法继续使用。
c:层析介质变黄,一般是介质污染严重,需要再生清洗。
05、订货信息

