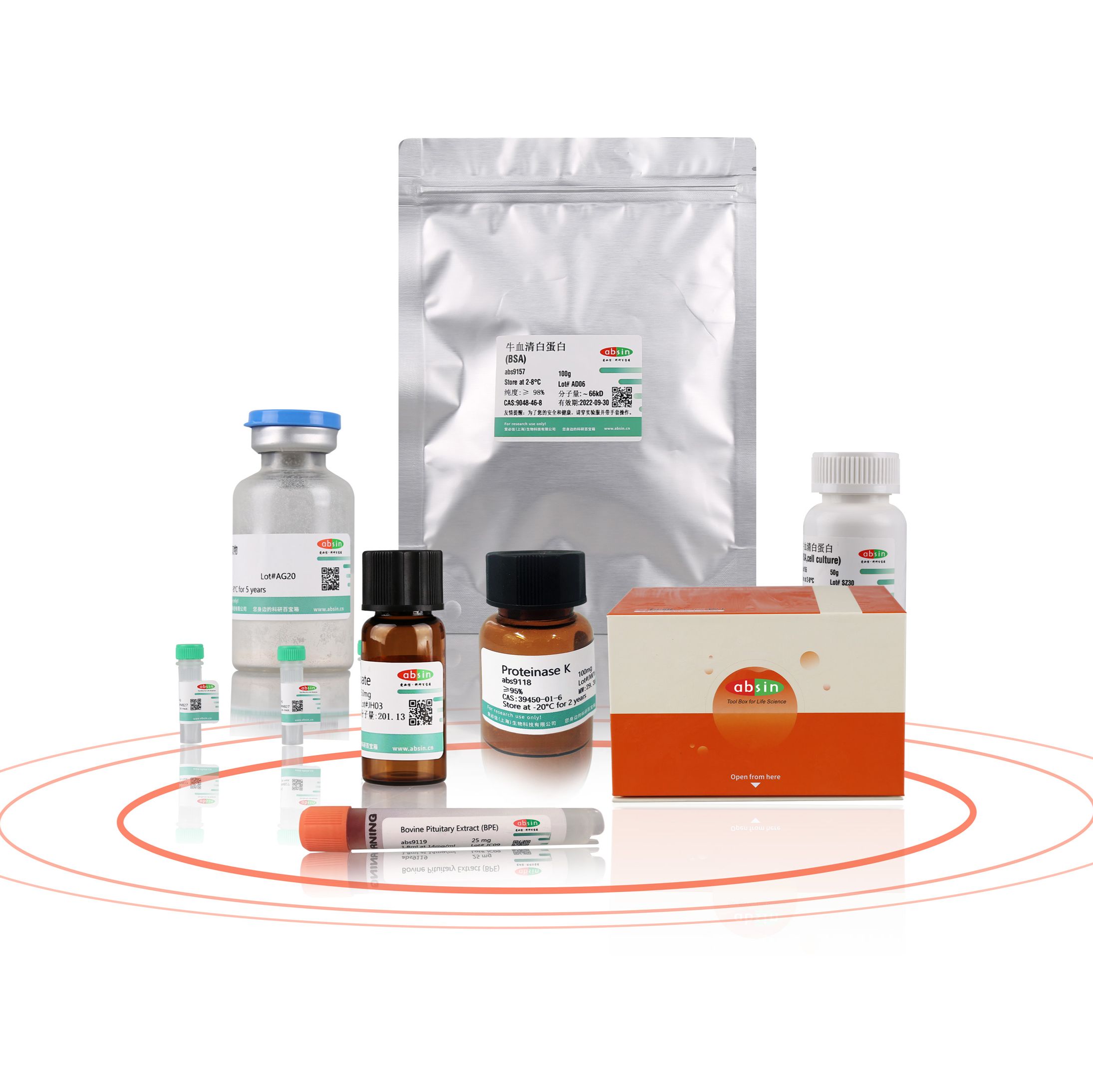
相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 保存条件:
-
- 保质期:
-
- 英文名:
-
- 库存:
现货
- 供应商:
爱必信(上海)生物科技有限公司
- CAS号:
-
- 规格:
10ml
| 公告提醒:爱必信所有产品和服务仅用于科学研究,不用于临床应用及其他用途提供产品和服务(也不为任何个人提供产品和服务)!
产品描述: 产品名称:Protein A抗体纯化琼脂糖磁珠 描述: 【产品介绍】Protein A琼脂糖磁珠以交联琼脂糖为基质,Protein A被在磁性微球表面。与同类产品相比,Protein A琼脂糖磁珠表面具有更多的抗体结合 位点。在IP实验中,只需使用更少的磁珠量,非特异性结合低,使用简便有效,具有大面积特异的表面区域,从而大大缩短抗体吸附和抗原结合的时间,可以在 30 分钟内完成 完整的IP实验。此产品适用的范围广泛,例如细胞裂解液、细胞分泌液上清、血清、动物腹水。 【产品规格】
【产品特点】抗体结合位点丰富;非特异性吸附低。 【作用对象】适用于细胞裂解液、细胞分泌液上清、血清、动物腹水以及其它的免疫抗原等。 【注意事项】 1. 进行免疫沉淀操作之前,请务必认真阅读本操作说明书;2. 本产品须与磁性分离器配套使用; 3. 磁珠应保存在储存溶液中,防止干燥; 4. 请勿将磁珠冷冻或离心,以免引起不可逆聚集; 5. 为保证最佳的实验结果,请选择特异性较强的抗体进行免疫沉淀反应; 6. 操作者可根据实际需求,利用抗体结合反应步骤以及抗原结合反应步骤中收集的上清 液检测抗体、抗原和磁珠的结合情况; 7. 对于IP实验,不同类型的抗体与抗原结合的亲和性是有区别的,抗体与抗原结合还会 受到结合缓冲液和洗涤缓冲液的影响,因此,如果操作者使用本试剂盒提供的缓冲体系 不能获得很好的实验结果,可自行筛选及配制缓冲液进行实验; 8. 本磁珠表面包被的重组蛋白Protein A在极端条件下(如低 pH、加热处理)存在极低 的蛋白脱落情况; 9. 不建议操作者用于分子量约130 kD 目标蛋白的免疫沉淀实验; 10. 本产品仅供研究使用。
使用方法: 【操作流程 】 推荐缓冲液
【抗原样品制备】 本操作说明书提供以下四种样品处理方法,建议您根据不同来源的抗原样品选择适当的方式进行预处理,使待检测抗原释放至样品溶液中。 血清样品处理:若目标蛋白丰度较高,建议用 Binding Buffer 稀释血清样品至目标蛋白终浓度为 10~100 µg/mL,置于冰上备用(或置于-20℃长期保存)。 悬浮细胞样品处理:离心收集细胞(4℃,500 g,10 min),弃上清后称重,按 1.0ˣ10^5个细胞20~30 µL的比例加入 PBS 洗涤2次;按1.0ˣ10^5个细胞20~30µL的比例加入NP40 Cell Lysis Buffer,同时加入蛋白酶抑制剂(如终浓度为1mM的PMSF),混匀后置于冰上处理10min;离心收集上清液(4℃,14000 g,10 min),置于冰上备用(或置于-20℃长期保存)。 贴壁细胞样品处理:移去培养基,用 PBS 洗涤两次;用胰酶消化或者细胞刮刀,收 集至 1.5 mL 离心管内,按 1.0ˣ10^5个细胞 20~30 µL 的比例加入PBS 洗涤 2 次;按 1.0ˣ105个细胞20~30 µL的比例加入NP40 Cell Lysis Buffer,同时加入蛋白酶抑制剂(如终浓 度为1 mM的PMSF),混匀后置于冰上处理 10min;离心收集上清液(4℃, 14000 g, 10 min),置于冰上备用(或置于-20℃长期保存)。 大肠杆菌样品处理:离心收集大肠杆菌(4℃, 12000 g, 2 min),弃上清后称重,按 每克(湿重)菌体10 mL 的比例用 PBS 洗涤 2 次;按每克(湿重)菌体 5~10 mL 的比 例加入Binding Buffer,同时加入蛋白酶抑制剂(如终浓度为 1 mM 的 PMSF),重悬菌体,超声裂解细胞,离心收集上清(4℃, 17000 g, 10 min)。
【磁珠预处理】 1. 移液器吹打或漩涡振荡器混匀磁珠,取 50µL 磁珠悬浮液(10%,v/v)至离心管中,5mL磁力架磁性分离去除保存液;注:客户可根据实际需要适当增减;2. 加入100 µL PBS 混匀磁珠(颠倒 30 秒或者旋涡振荡器混匀),磁性分离去除上清液(重复 2 次); 【抗体结合】 1. 用100µLPBST 稀释 2~20µg 抗体样品(如样品体积大于100ul则不需要稀释),稀释后加入到装有磁珠的离心管中;注:实际抗体使用量需根据实验摸索,可参看磁珠对应不同抗体亚型的亲和力表;2. 将上述混合物放入摇床或旋转混合仪室温或 37℃颠倒混匀或者涡旋混匀 10~15 分钟; 3. 将装有磁珠和抗体的离心管放入磁力架,待磁珠完全贴壁后,去除上清液; 4. 用100µLPBST 洗涤磁珠-抗体复合物 3 次。 【抗体交联反应】(备选) 如操作者需要将抗体和目标抗原复合物共同洗脱,请忽略本步骤,直接进行下一步骤;本步骤适用于操作者需要单独洗脱目标抗原的试验,推荐使用BS3(Thermo Scientific, Cat. #21580)作为交联剂,相关实验请参照该试剂的操作说明。 【抗原沉淀反应】 1. 抗原吸附:向上一步装有磁珠-抗体复合物的离心管中加入制备好的细胞裂解液100~1000µL,用移液枪吹打混匀;2. 37℃颠倒混匀或者低速涡旋混匀15~20 分钟,使抗原和结合抗体的磁珠结合;注:为使集合更充分,孵育时间和稳定可根据实际需求进行调整; 3. 将上一步的离心管和混合物放入磁力架,吸取上清(上清可丢弃也可保存做后续分析); 4. 取 200µL PBS 洗涤磁珠-抗体-抗原复合物 3 次; 5. 洗涤完成后用100µLPBS重悬磁珠,用于下一步操作。 注:抗原洗脱前务必将磁珠转移新的离心管,避免将管壁上原有的非特异性吸附蛋白一起洗脱 【抗原洗脱】 本操作说明书提供以下两种抗原洗脱方案,操作者可根据后期检测的需要选择不同的抗原洗脱方法。 变性洗脱法: 1. 将沉淀抗原第5步骤中的磁珠放入磁力架,磁性分离去除上清液; 2. 向离心管中加入约30µL的Elution Buffer,用移液器轻轻混匀避免气泡产生,颠倒混匀 或者低速涡旋混匀2~5分钟; 3. 将磁珠放入磁力架,磁性分离收集上清(注:上清液中含有抗原勿丢弃); 4. 中和:上述步骤收集上清中抗原,若需做功能验证需加入Neutralization Buffer中和洗脱液(例入100µLElution Buffer加入10 µL Neutralization Buffer即可)。 【磁珠后处理】 使用后的磁珠用Elution buffer洗涤2次,磁性分离,弃上清液;接着用Binding/Washing buffer洗涤3次,磁性分离,弃上清液,加入200 μL Storage buffer重悬磁珠 ,置于2~8℃保存。 【磁珠再生】 1. 磁珠多次使用后会有沉淀蛋白、强疏水性蛋白、脂蛋白等杂质非特异性吸附到磁珠上,为了保证磁珠的使用效率,建议持续使用5次后进行磁珠再生处理。 按约每1 mL 10%(v/v)磁珠加入1 mL 1%(v/v)Triron X-100 磁珠再生缓冲液, 振荡均匀,在室温下置于翻转混合仪或者手工轻轻翻转混合,10 min 后进行磁性分离, 弃上清液。 2. 立即加入1 mL Binding/Washing buffer 进行重悬,然后磁性分离,弃上清液,重复该 操作 3 次。 3. 加入 1 mL Storage buffer 重悬磁珠 ,置于 2~8℃保存。 absin,您身边的科研百宝箱 |
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验- LAR Downregulation Protects the Astrocytic U251 and Cocultured SH-SY5Y Cells in a Rotenone-Induced Parkinson’s Disease Cell Model
Wei Zheng,Xiao Han,Bing Han,Gang Li,Jing Gan,Tian Wang,Bo Xu,Jie He,Wenxiao Du,Xiaolin Cao,Zhenhua Wang
INTERNATIONAL JOURNAL OF MOLECULAR SCIENCES. 2023 Jul 05 .
影响因子: 5.6
character. The N- and C- terminal and T-groups of the polypeptide can be ionized, contributing to the overall charge. The protein's net electric charge is the sum of the electric charges found on the surface of the molecule as a function of the environment
Protein Purification and Analysis
Levels of Structure in Protein Primary: A description of all covalent bonds. The sequence of AA residues Secondary: particularly stable arrangements of AA giving rise to recurring structural
 技术资料
技术资料暂无技术资料 索取技术资料