
插入式细胞培养小室和嵌套式培养板
接近天然状态的细胞生长
从1950年代开始,默克密理博的高品质膜
就被科学家创新地应用于细胞培养实验并
发表了众多高水平的研究报告。经过几十
年的实践和优化,Millicell
®
系列产品已经
成为细胞相关研究的基本工具。
Millicell
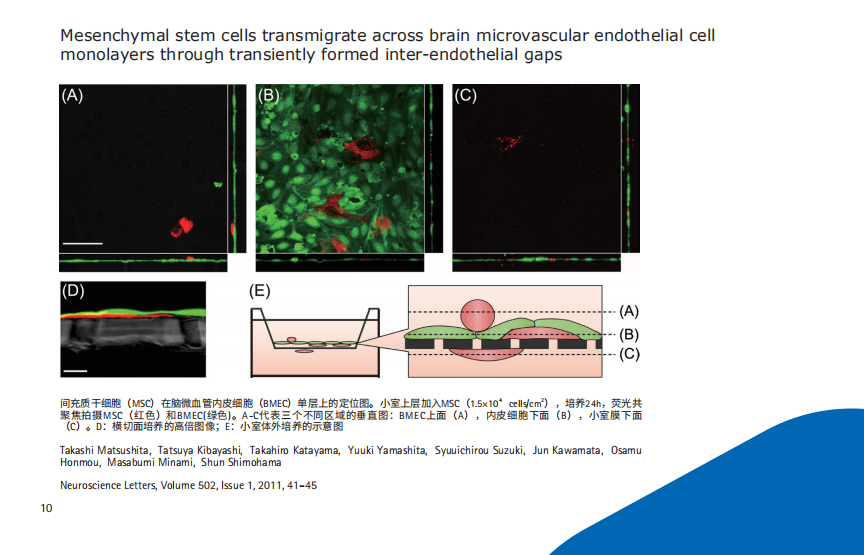
®
插入式细胞培养小室和培养板底面为
膜材质,使生长的细胞上下两侧都易于被接
触。因此细胞处于3D生长状态,比塑料表面更
能模拟细胞在生物体内的情况。而且,
Millicell
®
插入式细胞培养小室使细胞共培养及
单层细胞的上下两面进行研究变得非常方便。
品种齐全,方便选择
既提供悬挂式和站立式的单孔插入式细胞培养小
室,也有24孔或96孔的插入式细胞培养板及套
件,还有经组织培养处理的接收板;以上每种产
品又包括不同膜材质和膜孔径的多种选择。此外默
克密理博还全面提供细胞培养中必需的纯水制备系
统、无菌过滤装置、细胞计数器、培养基及各种添
加剂、抗生素、细胞迁移研究等完整试剂盒。关于
细胞培养与检测的各类技术问题,默克密理博富有
经验的专家团队也随时给予您专业的帮助。
插入式培养小室为单个无菌包装形式,
方便好用,减少浪费





















产品优点
改善细胞形态结构
更完善的细胞分化
更多的细胞器
更高的细胞密度
塑料表面
膜材质
加有胞外基质的膜
比较Setroli细胞在不同材质表面的生长情况。这篇文献指明在默克密理博再
生基底膜(RBM)上生长的细胞形态为卵圆形或锥形细胞核的高圆柱形单层,
非常接近这种细胞在体内的正常形态和功能。
Byers SW, Hadley MA, Djakiew D, Dym M. Growth and characterization of polarized
monolayers of epididymal epithelial cells and Sertoli cells in dual environment
culture chambers. J Androl. 1986 Jan
-
Feb;7(1):59
-
68.
Millicell
®
微孔膜材质的细胞培养
(产品应用指南)膜的类型及其特点
Biopore
™
亲水PTFE 膜
(聚四氟乙烯),CM
透氧透光性好,3D组织培养和观察
MF
-
Millipore
™
MCE 膜
(混合纤维素酯),HA
文献引用率高,用于毒理和极化等研究
Isopore
™
PCF 膜
(聚碳酸酯)
规格齐全,特别适合转运/渗透性等研究
PET 膜
(聚乙烯对苯二酸酯)
功能全面,是悬挂式Millicell
®
唯
一
采用的膜材质
Millicell® 悬挂式
细胞培养小室
Millicell® 站立式
细胞培养小室
Millicell® 器官培养型
站立式培养小室
• 用于细胞共培养、渗透性试验及频
繁的独立操作
• 独特的设计使上下两侧操作都非常
方便,减少对细胞的损害和污染
• 全部为PET膜材质,有5种膜孔径和
3种膜面积(适合不同多孔板)的产
品供选择;其中1μm孔径的是透明
的,特别推荐用于光学观察
• 细胞生长状态好,多种选择使
各种细胞学研究极为方便
• 膜材质包括Biopore
™
(PTFE)膜,
MF
-
Millipore
™
(混合纤维素酯)
膜,聚碳酸酯膜等,有5种膜孔径、
2种膜面积供选择(适合6孔板和
24孔板)
• 获得活性更高的培养细胞和组织,
特别推荐用于体外移植物的立体培
养和长期组织结构研究
• 较薄且更低的侧壁,使其更好地适
合标准培养皿尺寸,操作也更方便
• Biopore
™
(PTFE)膜透氧性及透光
性也非常出色,有助于提高细胞的
存活力,最长超过40天
膜厚50μm,仅0.4μm
一
种规格,需包被ECM。透
明性很好,荧光背景低,蛋白吸附低,适合细胞显微
观察。透氧性好,最适合用于组织器官的长时间培养
和观察。有站立式和器官培养型Millicell
®
产品形式。
10μm薄膜,膜孔径齐全。已经组织培养预处理,不
需包被ECM。低荧光背景,低蛋白吸附,仅有站立
式Millicell
®
产品形式。
120μm厚不含Triton
®
的混合纤维素酯膜,仅0.45μm
一
种规格,不需包被ECM。用于细胞表面受体、体外
毒理学、微生物吸附和极化吸收分析。与塑料培养皿
相比,细胞在此膜上生长密度可提高2到3倍,而且具
有更好的细胞形态。仅有站立式Millicell
®
产品形式。
10μm超薄蚀刻膜,其中孔径为1μm规格的透明性极
,可用于直接观察。低荧光背景,低蛋白吸附,孔
径齐全,不需要ECM细胞即能生长良好。
单个无菌包装,即拆即用,减少污染风险并避免不必要的浪费。适用于SEM和TEM可视技术,并与荧光染色兼容。
特别
推荐
脑片培养实验应用介绍
文件供免费索取
23
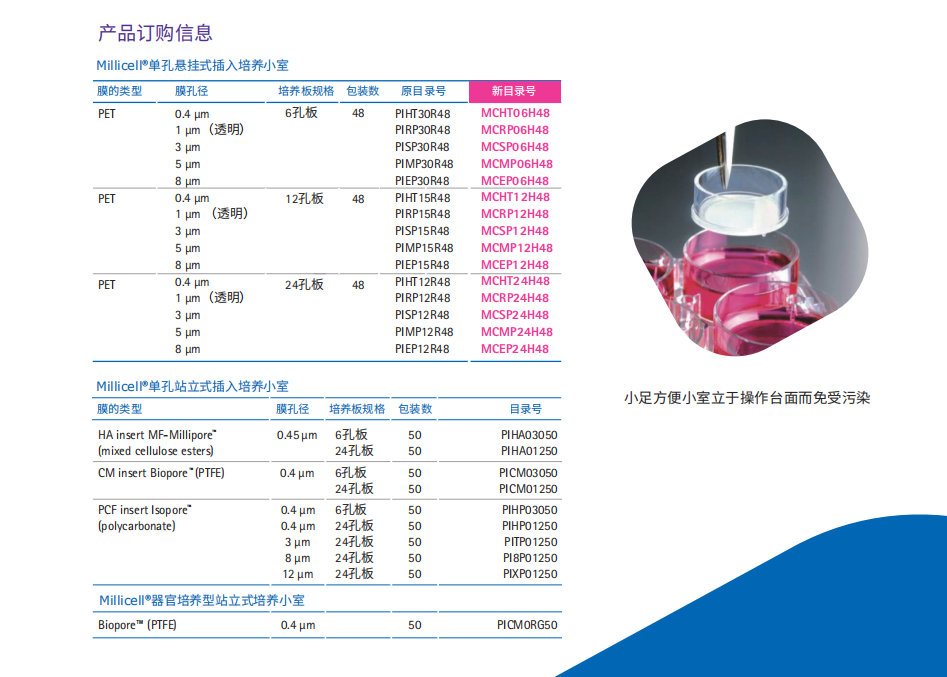
产品订购信息
Millicell
®
器官培养型站立式培养小室
HA insert MF
-
Millipore
™
(mixed cellulose esters)
0.45 µm 6孔板
24孔板
50
50
PIHA03050
PIHA01250
CM insert Biopore
™
™
(PTFE) 0.4 µm 6孔板
24孔板
50
50
PICM03050
PICM01250
PCF insert Isopore
Biopore
™
(PTFE)
(polycarbonate)
0.4 µm
0.4 µm
0.4 µm
3 µm
8 µm
12 µm
6孔板
24孔板
24孔板
24孔板
24孔板
50
50
50
50
50
50
PIHP03050
PIHP01250
PITP01250
PI8P01250
PIXP01250
PICM0RG50
Millicell
®
单孔悬挂式插入培养小室
Millicell
®
单孔站立式插入培养小室
PET 0.4 μm
1 μm(透明)
3 μm
5 μm
8 μm
0.4 μm
1 μm (透明)
3 μm
5 μm
8 μm
0.4 μm
1 μm(透明)
3 μm
5 μm
8 μm
PIHT30R48
PIRP30R48
PISP30R48
PIMP30R48
PIEP30R48
PIHT15R48
PIRP15R48
PISP15R48
PIMP15R48
PIEP15R48
PIHT12R48
PIRP12R48
PISP12R48
PIMP12R48
PIEP12R48
MCHT06H48
MCRP06H48
MCSP06H48
MCMP06H48
MCEP06H48
MCHT12H48
MCRP12H48
MCSP12H48
MCMP12H48
MCEP12H48
MCHT24H48
MCRP24H48
MCSP24H48
MCMP24H48
MCEP24H48
6孔板 48
PET 12孔板 48
PET 24孔板 48
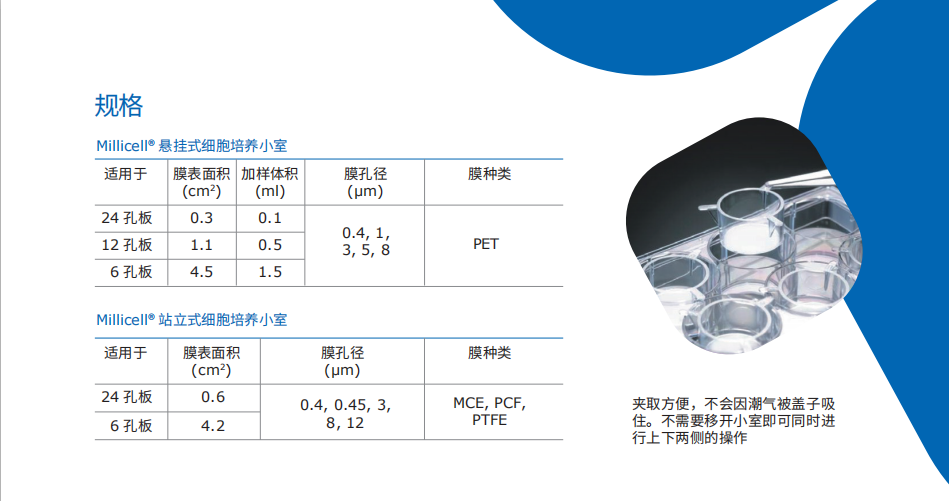
规格
Millicell
®
站立式细胞培养小室
适用于
24 孔板
6 孔板
0.6
4.2
0.4, 0.45, 3,
8, 12
MCE, PCF,
PTFE
膜表面积
(cm
2
)
膜孔径
(µm)
膜种类
Millicell
®
悬挂式细胞培养小室
适用于
24 孔板
12 孔板
6 孔板
0.3
1.1
4.5
0.1
0.5
1.5
0.4, 1,
3, 5, 8 PET
膜表面积
(cm
2
)
膜孔径
(µm)
加样体积 膜种类
(ml)
膜的类型 膜孔径 培养板规格 包装数 原目录号 新目录号
膜的类型 膜孔径 培养板规格 包装数 目录号
夹取方便,不会因潮气被盖子吸
住。不需要移开小室即可同时进
行上下两侧的操作
小足方便小室立于操作台面而免受污染Millicoat Collagen I 6
-
well plate
Millicoat Collagen I 24
-
well plate
Millicoat Poly
-
D
-
Lysine 6
-
well plate
Millicoat Poly
-
D
-
Lysine 24
-
well plate
Millicoat Fibronectin 6
-
well plate
Millicoat Fibronectin 24
-
well plate
PICL06P05
PICL24P05
PIDL06P05
PIDL24P05
PIFB06P05
PIFB24P05
产品描述 包装数 目录号
5
5
5
5
5
5
产品订购信息
产品描述 膜材质 膜孔径 包装数 目录号
Millicell
®
24 孔嵌套式细胞培养板
Millicell
®
96 孔嵌套式细胞培养板
24
-
well cell culture plate,
single
-
well feeder tray,
24
-
well receiver tray, and lid
PCF
PET
PCF
PCF
PCF
0.4 µm
1 µm
3 µm
5 µm
8 µm
1 经干细胞 PSHT010R1
培养验证
经干细胞
培养验证
PSRP010R1
PSST010R1
PSMT010R1
PSET010R1
24
-
well cell culture plate,
24
-
well receiver tray, and lid
PCF
PCF
PCF
3 µm
5 µm
8 µm
5 PSST010R5
PSMT010R5
PSET010R5
24
-
well cell culture plate,
24
-
well receiver tray, and lid
single
-
well feeder tray, and lid
PCF
PET
0.4 µm
1 µm
5
5
PSHT010R5
PSRP010R5
PSMW010R5
96
-
well cell culture plate,
single
-
well feeder tray, 96
-
well
receiver tray, and lid
PCF
PET
0.4 µm
1 µm
1 PSHT004R1
PSRP004R1
96
-
well cell culture plate, 96
-
well
receiver tray, and lid
PCF 0.4 µm 5 PSHT004S5
96
-
well cell culture plate,
single
-
well feeder tray, and lid
PCF
PET
0.4 µm
1 µm
5 PSHT004R5
PSRP004R5
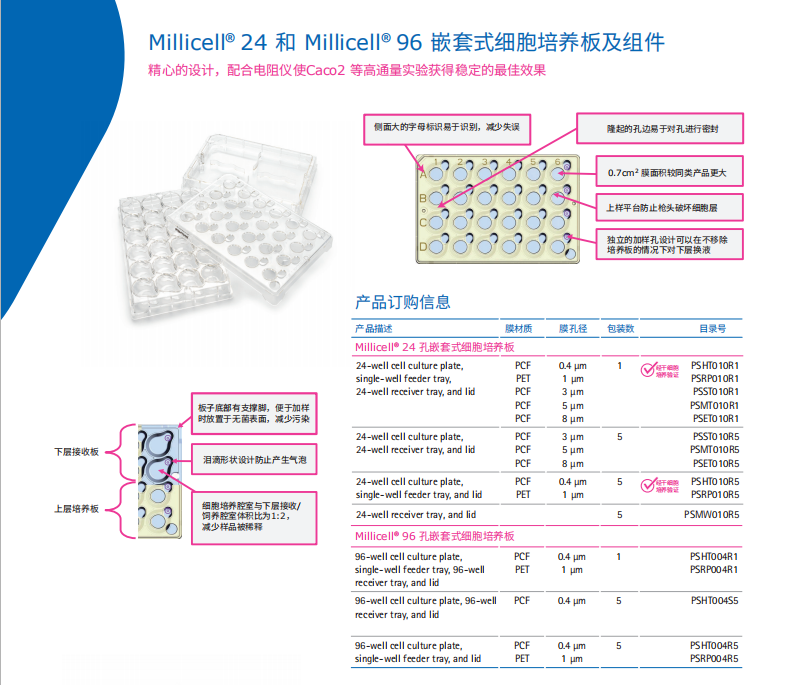
Millicell
®
24 和 Millicell
®
96 嵌套式细胞培养板及组件
预包被ECM的培养板
•
•
•
•
提供最适合贴壁细胞贴附和生长的表面
用于包被的包括collagen, fibronectin以及poly
-
D
-
lysine
提供6
-
,24
-
孔板形式的产品
品质优异,使细胞培养更方便,数据更稳定
0.7cm
2
膜面积较同类产品更大
侧面大的字母标识易于识别,减少失误 隆起的孔边易于对孔进行密封
上样平台防止枪头破坏细胞层
独立的加样孔设计可以在不移除
培养板的情况下对下层换液
泪滴形状设计防止产生气泡
板子底部有支撑脚,便于加样
时放置于无菌表面,减少污染
细胞培养腔室与下层接收/
饲养腔室体积比为1:2,
减少样品被稀释
下层接收板
上层培养板
精心的设计,配合电阻仪使Caco2 等高通量实验获得稳定的最佳效果
4应用 站立式(膜孔径µm) 悬挂式(膜孔径µm) 24孔板(膜孔径µm) 96孔板(膜孔径µm)
细胞表面受体 PCF (0.4)
HA (0.45)
CM (0.4)
PET (0.4, 1) PCF (0.4)
PET (1)
PCF (0.4)
PET (1)
趋化性/趋触性 PCF (3, 8) PET (3, 5, 8) PCF (3, 5, 8) MultiScreen® MIC
Plate (3, 5, 8)
上皮细胞生长/
药物吸收
PCF (0.4)
HA (0.45)
PET (0.4, 1) PCF (0.4)
PET (1)
PCF (0.4)
PET (1)
饲养层 PCF (0.4, 3, 8) PET (所有孔径) PCF (所有孔径)
PET (1)
PCF (0.4)
PET (1)
体外受精 CM (0.4) PET (1) PET (1) PET (1)
体外毒理学 PCF (0.4)
CM (0.4)
HA (0.45)
PET (0.4, 1) PCF (0.4)
PET (1)
PCF (0.4)
PET (1)
微生物附属物 PCF (0.4)
CM (0.4)
HA (0.45)
PET (0.4, 1) PCF (0.4)
PET (1)
PCF (0.4)
PET (1)
组织/器官培养 Organotypic (0.4)
相差显微镜检查 CM (0.4) PET (1) PET (1) PET (1)
极化蛋白质分泌物 PCF (0.4)
CM (1)
PET (0.4, 1) PCF (0.4)
PET (1)
PCF (0.4)
PET (1)
极化摄取 PCF (0.4)
CM (0.4)
HA (0.45)
PET (0.4, 1) PCF (0.4)
PET (1)
PCF (0.4)
PET (1)
转运/渗透性 PCF (0.4) PET (0.4, 1) PCF (0.4)
PET (1)
PCF (0.4)
PET (1)
肿瘤细胞转移和侵袭 PCF (8,12) PET (5, 8) PCF (5, 8) MultiScreen® MIC
Plate (5, 8)
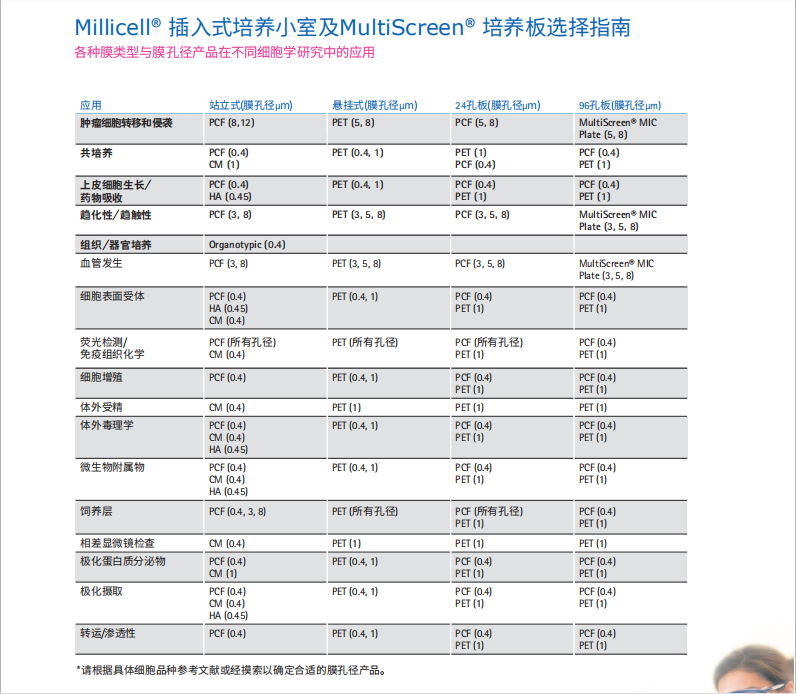
Millicell
®
插入式培养小室及MultiScreen
®
培养板选择指南
各种膜类型与膜孔径产品在不同细胞学研究中的应用
代码 膜种类 膜材料
膜材质代码
CM
HA
PCF
PET
Biopore
™
MF
-
Millipore
™
Isopore
™
PET
亲水性 PTFE
混合纤维素酯类
聚碳酸酯
聚酯
*
请根据具体细胞品种参考文献或经摸索以确定合适的膜孔径产品。
血管发生 PCF (3, 8) PET (3, 5, 8) PCF (3, 5, 8) MultiScreen® MIC
Plate (3, 5, 8)
共培养 PCF (0.4)
CM (1)
PET (0.4, 1) PET (1)
PCF (0.4)
PCF (0.4)
PET (1)
细胞增殖 PCF (0.4) PET (0.4, 1) PCF (0.4)
PET (1)
PCF (0.4)
PET (1)
荧光检测/
免疫组织化学
PCF (所有孔径)
CM (0.4)
PET (所有孔径) PCF (所有孔径)
PET (1)
PCF (0.4)
PET (1)
5肿瘤侵袭实验
肿瘤细胞侵袭能力检测在肿瘤学(迁移、侵袭)和免疫学(迁
移、趋化)中是常规实验。
侵袭是细胞迁移的
一
种。细胞迁移分三种类型:趋触、趋化
和侵袭。趋触是指细胞定向向
一
些整联蛋白或粘附蛋白受体
迁移的能力,例如上皮细胞和成纤维细胞;趋化指细胞趋向
于
一
些化学分子的特性,例如免疫细胞;侵袭通常指肿瘤细
胞分泌因子降解并穿透基质胶的能力。
肿瘤细胞的侵袭性是肿瘤相关信号通路、药物治疗、靶向治疗、
致癌 / 抑癌基因等肿瘤学研究的
一
个重要指标。
免疫细胞具有趋化性,例如粒细胞、巨噬细胞、单核细胞对
CCL、CXCL 类因子的趋化性,免疫细胞异常(如过度趋化)
通常会引起
一
些炎症类疾病如风湿、关节炎、牛皮藓、动脉
粥样化等。
复苏代数靠前的肿瘤细胞,在含有10%FBS的培养基中预先培
养2
-
3代,待细胞汇合达到80%左右,饥饿处理18
-
24小时。
准备铺胶:
a) 4
°
C融EMC胶过夜。
b) 将细胞小室、培养板和枪头等于4
°
C 预冷。
c ) 用无血清的冷培养基稀释ECM 胶至20ug/mL ,以
5
-
10ug/cm2的密度加入到细胞小室的上层(按照ECM产品说明
书的推荐比例和体积),轻轻摇晃使胶均匀铺在膜上。以上操
作在冰上进行。
d)立即将铺好ECM胶的细胞小室置于培养板中,于37
°
C孵育1
小时,ECM胶可由液体凝成固体,吸走多余的或者未凝的胶。
细胞用PBS清洗
一
次,EDTA或者0.05%胰酶消化,然后用包含
5%BSA的无血清培养基中和,1500rpm离心5
-
10min。
用无血清培养基重悬细胞,调整细胞密度至0.5
-
2.0x10
6
cell/ml。
肿瘤细胞最好经过饥饿处理,并且小室上下培养
基的FBS有浓度差,以保证细胞可以穿透基质胶。
铺细胞要均匀,滤膜底部不能产生气泡,否则会
导致细胞染色不均匀,或者局部细胞无法穿透。
根据细胞类型选择合适的膜孔径和膜类型。PET
膜兼容广泛,适合绝大多数种类的细胞。
侵袭实验的细胞密度比较大,
一
般在 1 0 6
cells/cm2左右,不同肿瘤细胞的接种密度、培养
时间不同,需要参考文献和实验摸索。细胞太
少,迁移不过去;细胞太多,可能导致正常组和
实验组无差异。
做实验需要用正常的细胞摸索合适的细胞密
度和培养时间,确定之后再加实验组,同时如果
条件允许,设置
一
组已知高迁移性的细胞作阳性
对照。
注意细胞小室内外培养基的比例,不要使小室外
培养基超过小室内培养基液面。
观察细胞时
一
定要擦去小室内部贴在膜上的细胞。
实验目的:研究肿瘤细胞侵袭能力
本实验技术要点:
实验简介:
具体操作:
以配合24孔板的8μM PET膜Millicell
®
悬挂式细胞培养小室
(cat#MCEP24H48)为例,
实验周期:3
-
5天
常见检测细胞:
肿 瘤 细 胞(MDA
-
MB
-
231, MCF
-
7, HT1080, B16F10)等,
用孔径为 8μM 的培养小室
巨噬细胞、单核细胞 PMN:用孔径为 5μM 的培养小室
内 皮 细 胞(HUVEC)、白 血 病 细 胞 K562、骨 髓 瘤 细 胞
HB124:用孔径为 3μM 或 5μM 的培养小室
6
Millicell
®
细胞培养小室/
培养板的经典应用
1.
2.
3.
4.
1.
2.
3.
取上述200μL细胞液加入小室,下室(培养板)
加入900L含有10% FBS的培养基。不同规格的
小室和培养板所加的体积不同,具体参考
Millicell®产品说明书。
37
°
C孵育24至72小时,依据肿瘤细胞类型而定。
孵育结束,小心取出细胞小室,吸掉小室上层培
养液,PBS清洗
一
遍,70%酒精或者4%多聚
醛固定5min,0.5%结晶紫(2%乙醇或PBS溶
解)染色20min,然后进行第8步或者第9步。
PBS清洗两次以去除多余的染料,立即用棉签擦
去滤膜上层的细胞,自然静置风干。显微镜下观
察滤膜下层的细胞,随机选取不同的视野计数并
算平均值。
结晶紫溶解滤膜下层细胞,然后用33%醋酸脱
色,将结晶紫完全洗脱下来,洗脱液可在酶标仪
上570nm读取OD值。这种方法可以避免视野下
细胞穿透不均匀带来的误差。
5.
6.
7.
8.
9.
1.
2.
3.
4.
5.
6.
7.默克提供的相关产品:
1. N Yang, Y Tang, F Wang, H Zhang, D Xu, Y Shen, Blockade of
store
-
operated Ca 2+ entry inhibits hepatocarcinoma cell
migration and invasion by regulating focal adhesion
turnover, Cancer letters, 2013,4: 330
-
2, 163
–
169 (HCC
-
LM3
cells: 8μM)
2. Q Ma, Q Jiang, Q Pu, X Zhang, MicroRNA
-
143 inhibits
migration and invasion of human non
-
small
-
cell lung cancer
and its relative mechanism, Int J Biol Sci. 2013; 9(7):
680
–
692. (NSCLC cell )
3. Ota D, Ikesue M, Matsui Y, et al. The cell to cell interaction
of breast cancer cells regulates cancer invasion via adam15
[J]
. American Journal of Immunology, 2012, 8(4): 123.
1. Kong L M, Liao C G, Zhang Y, et al. A regulatory loop involving miR
-
22,
Sp1, and c
-
Myc Modulates CD147 expression in breast cancer invasion and
metastasis [J]
. Cancer research, 2014, 74(14): 3764
-
3778.
2. Zhang J J, Zhu Y, Xie K L, et al. Yin Yang
-
1 suppresses invasion and
metastasis of pancreatic ductal adenocarcinoma by downregulating
MMP10 in a MUC4/ErbB2/p38/MEF2C
-
dependent mechanism[J]
. Molecular
cancer, 2014, 13(1): 130.
3. Kong L M, Liao C G, Zhang Y, et al. A regulatory loop involving miR
-
22,
Sp1, and c
-
Myc Modulates CD147 expression in breast cancer invasion and
metastasis[J]
. Cancer research, 2014, 74(14): 3764
-
3778.
4. Chen Y J, Lee L Y, Chao Y K, et al. DSG3 facilitates cancer cell growth and
invasion through the DSG3
-
plakoglobin
-
TCF/LEF
-
Myc/cyclin D1/MMP
signaling pathway [J]
. PloS one, 2013, 8(5): e64088.
5. Yu H, Pan C, Zhao S, et al. Resveratrol inhibits tumor necrosis
factor
-
α
-
mediated matrix metalloproteinase
-
9 expression and invasion of
human hepatocellular carcinoma cells[J]
. Biomedicine & Pharmacotherapy,
2008, 62(6): 366
-
372. (HepG2 cell: 8μM)
6. Chiu C C, Lin C Y, Lee L Y, et al. Glucose
-
regulated protein 78
regulates multiple malignant phenotypes in head and neck
cancer and may serve as a molecular target of
therapeutic intervention[J]
. Molecular cancer
therapeutics, 2008, 7(9): 2788
-
2797.
(Nasopharyngeal cancers)
参考文献:
中国科学家发表的高水平文章:
• 目录号 MCEP24H48(原目录号PIEP12R48):
PET膜,膜孔径8 µM, 适合24孔板
• 目录号 MCEP12H48(原目录号PIEP15R48):
PET膜,膜孔径8 µM,适合12孔板
• 目录号 MCEP06H48(原目录号PIEP30R48):
PET膜,膜孔径8 µM, 适合6孔板
• 目录号 PI8P01250:
PCF膜,膜孔径8 µM,适合24孔板
基质胶:
• 目录号08
-
110:ECMatrix,
• 目录号CC050:CollagenⅠ等等
成套试剂盒:
• 目录号 ECM551:QCM
™
Collagen Cell Invasion
Assay, 24
-
well (8 µm), Colorimetric
• 目录号 ECM552:QCM
™
Collagen Cell Invasion
Assay, 24
-
well (8 µm), Fluorometric
• 目录号 ECM550:QCM
™
ECMatrix Cell Invasion
Assay, 24
-
well (8 µm), Colorimetric
• 目录号 ECM555:QCM
™
ECMatrix Cell Invasion
Assay, 96
-
well (8 µm), uorimetric
自行配置试剂盒:推荐组合
• Cat#MCEP24H48 + Cat#08
-
110,即ECM550
• Cat#MCEP24H48 + Cat#CC050,即ECM551
Millicell
®
细胞培养小室:
PET膜悬挂式或PCF膜站立式,膜孔径为
5 μM或8 μM
1. 细胞伤口划痕实验 scratch motility (wound
healing) :在铺满细胞的板中间划
一
道伤口,两边的细
胞会迁移到中间从而覆盖伤口,通过计算伤口愈合速率
来判断细胞迁移能力。该方法比较早,不能定量计算迁
移的细胞数量,而且有可能受到增殖的影响,所以
一
般
适合初筛,然后还是要用到小室实验来证明。默克密理
博提供 Cell Comb
™
Scratch Assay
-
(Cell Comb
™
Scratch Assay),目录号 17
-
10191。
2. 明胶酶谱:收集肿瘤细胞培养上清,在含有 0.1% 明胶
的 SDS
-
PAGE 中电泳,再经过复性、孵育和染色,检查
透明条带。这是检测活性基质金属蛋白酶 MMP
-
2 和
MMP
-
9 的经典方法,以此辅助证明肿瘤细胞侵袭能力。
3. 体内荷瘤实验:包括实验性肿瘤转移模型和原位肿瘤转移
模型,前者是尾静脉注射肿瘤细胞,后者是在皮下荷瘤,
最终都是检测其他脏器的肿瘤转移情况。体内实验更有
说服力,但是实验周期也比较长,因此通常是在细胞水
平验证之后再开展。
知道更多
肿瘤细胞侵袭实验常用的其他方法
Cat# ECM551, Merck Millipore
HT
-
1080 与 NIH3T3 的侵袭比较。分别在不含 FBS 的小室中培养
HT
-
1080 和 NIH3T3 cells(+/
-
25 μM MMP 抑制剂 GM6001),25 万
个细胞 / 孔,下室培养基含有 10%FBS,培养 24h,擦去膜上层
细胞,染色,拍照。
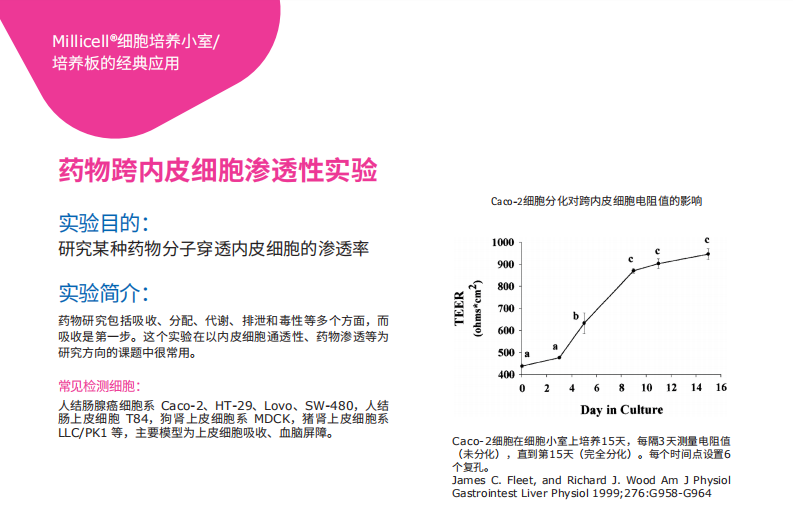
7药物跨内皮细胞渗透性实验
药物研究包括吸收、分配、代谢、排泄和毒性等多个方面,而
吸收是第
一
步。这个实验在以内皮细胞通透性、药物渗透等为
研究方向的课题中很常用。
常见检测细胞:
人结肠腺癌细胞系 Caco
-
2、HT
-
29、Lovo、SW
-
480,人结
肠上皮细胞 T84,狗肾上皮细胞系 MDCK,猪肾上皮细胞系
LLC/PK1 等,主要模型为上皮细胞吸收、血脑屏障。
实验目的:
研究某种药物分子穿透内皮细胞的渗透率
实验简介:
上皮细胞生长到细胞汇合度达80
-
90%时开始实验,不要超
过90%,否则会影响到后续细胞单层的形成。
将细胞均匀接种在小室膜上。对于24孔板和96孔板的接种密
度见本文图示。
每隔2天用电阻仪测量细胞跨膜电阻值,直到达到平台,提
示细胞已经形成致密单层;或者通过检测荧光染料荧光黄的
通过率,以判断细胞刚好完全汇合。电阻仪测量因不伤害细
胞,可以继续培养而比荧光黄法更为普遍地被采用。
细胞单层汇合后,用DPBS清洗
一
次细胞,加入含有不同浓
度药物(
一
般10
-
200μM)的缓冲液。如果要测药物从上至
下的运输效果,则上层小室中加药物,下层培养板孔里只加
缓冲液;反之则相反。
将培养板在37℃条件下培养(60rpm震荡或者不震荡)
1
-
2h,到达时间之后,分别从细胞小室和培养孔里取出
一
定
体积缓冲液(
一
般50μL )转移至新的转运分析板进行
LC/MC分析。对于放射性标记药物,分别取出20μL缓冲液
加入100μL闪烁液,通过多孔闪烁读板仪读值。
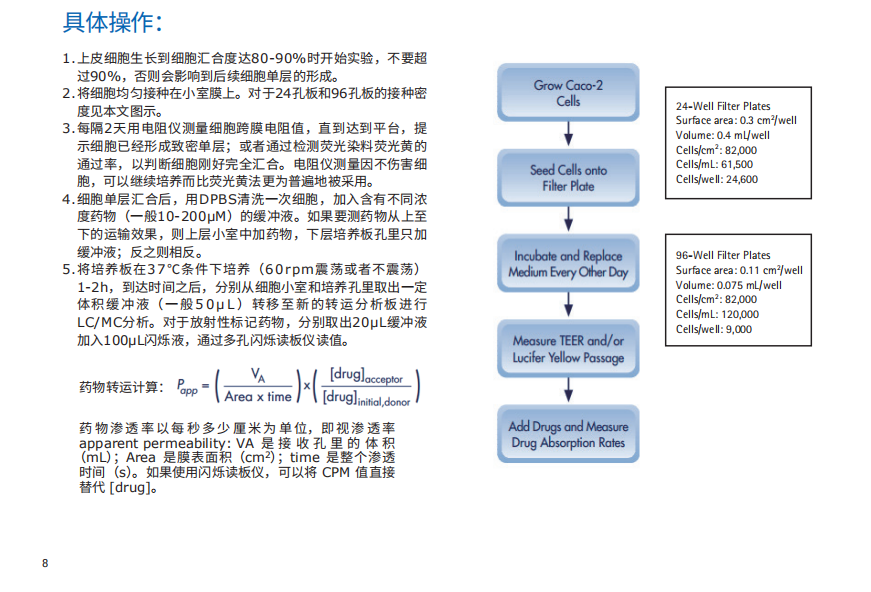
具体操作:
24
-
Well Filter Plates
Surface area: 0.3 cm
2
/well
Volume: 0.4 mL/well
Cells/cm
2
: 82,000
Cells/mL: 61,500
Cells/well: 24,600
96
-
Well Filter Plates
Surface area: 0.11 cm
2
/well
Volume: 0.075 mL/well
Cells/cm
2
: 82,000
Cells/mL: 120,000
Cells/well: 9,000
Caco
-
2细胞分化对跨内皮细胞电阻值的影响
Caco
-
2细胞在细胞小室上培养15天,每隔3天测量电阻值
(未分化),直到第15天(完全分化)。每个时间点设置6
个复孔。
James C. Fleet, and Richard J. Wood Am J Physiol
Gastrointest Liver Physiol 1999;276:G958
-
G964
8
Millicell
®
细胞培养小室/
培养板的经典应用
药物转运计算:
药 物 渗 透 率 以 每 秒 多 少 厘 米 为 单 位,即 视 渗 透 率
apparent permeability: VA 是接收孔里的体积
(mL);Area 是膜表面积(cm
2
);time 是整个渗透
时间(s)。如果使用闪烁读板仪,可以将 CPM 值直接
替代 [drug]。
1.
2.
3.
4.
5.细胞密度对于 Caco
-
2 细胞的生长和分化很重要,
最初实验时可以设置几个梯度以确定最佳细胞密度,
例 如:10
-
day Caco
-
2 Cell Seeding Density 可
以设置为 10,000 至 35,000 细胞 / 孔;21
-
day
Caco
-
2 Cell Seeding Density 从 6,000 至
12,500 细胞 / 孔。
换液时不要碰到或者吹散细胞,尽可能避免破坏细
本实验技术要点:
Calcein
-
AM Efflux
MDCK
-
MDR1
3 DAY
MDCK
3 DAY
Caco
-
2
21 DAY
No
Inhibitor
Inhibitor
Drug Transport
96 Well
–
PCF Membrane
24 Well
–
PCF Membrane
24 Well
–
PET Membrane
Efflux Ratios
Mannitol n Testosterone n Digoxin n Mannitol Digoxin
3 Day MDCK
0.9 ± 0.5 17 17.4 ± 4 14 0.8 ± 0.4 27 1.0 9.2
3 Day MDCK
-
MDR1 1.4 ± 0.4 16 20.0 ± 4 12 0.6 ± 0.3 25 1.2 21.9
21 Day CACO 2.2 ± 0.6 20 34.9 ± 8.4 30 1 ± 0.3 30 1.1 27.8
Mannitol n Testosterone n Digoxin n Mannitol Digoxin
3 Day MDCK 1.1 ± 0.1 10 24.8 ± 3.4 10 1.5 ± 0.4 10 1.2 3.9
3 Day MDCK
-
MDR1 1.4 ± 0.05 10 20.0 ± 0.2 10 0.7 ± 0.01 10 1.2 28.0
21 Day CACO 1.4 ± 0.02 6 21.7 ± 1.2 6 0.7 ± 0.04 6 0.9 12.5
Mannitol n Testosterone n Digoxin n Mannitol Digoxin
3 Day MDCK 1.2 ± 0.4 10 27.4 ± 3.0 10 2.1 ± 0.4 10 1.2 3.7
3 Day MDCK
-
MDR1 1.6 ± 0.05 10 22 ± 2.6 10 0.4 ± 0.08 10 1.0 22.0
21 Day CACO 1.9 ± 0.07 6 24 ± 2.8 6 1.1 ± 0.2 6 1.0 12.4
Andrew A. Arena, Sara Gutierrez, Steven D. Sheridan, and Matthew J. Wilgo
3 versus 21 day assays
采用 Millicell
®
24 孔板和 96 孔板建立经 MDR1 转染的 MDCK 细胞高通量药物渗透试验模型。
Caco
-
2 完全分化后会分泌 P
-
糖蛋白,将
一
些被动运输到细胞内的小分子泵出,例如钙黄绿素 Calcein,使得细胞内
Calcein
-
AM 荧光信号下降。通过检测 Calcein 的溢出率,可以判断 Caco
-
2 细胞的分化程度。图中转染了 MDR1 的细胞
系 MDCK
-
MDR1,可以在 3 天时完成分化,达到和 Caco
-
2 细胞 21 天
一
样的效果。
Drug Transport results: Caco
-
2 & MDCK
1. Intestinal Absorption and First
-
Pass Metabolism of
Polyphenol Compounds in Rat and Their Transport Dynamics
in Caco
-
2 Cells, Zenghui Teng , Chengjun Yuan , et al,
PlOSOne, 2012 (1): DOI: 10.1371/journal.
pone.0029647
2. Identication of permeability
-
related hurdles in oral delivery
of curcumin using the Caco
-
2 cell model, Banrida Wahlang,
Yogesh B. Pawar, Arvind K. Bansal, European Journal of
Pharmaceutics and Biopharmaceutics, 2011(2): 77
-
2,
275
–
282
3. Insulin
-
Loaded Nanoparticles Based on N
-
Trimethyl
Chitosan: In Vitro (Caco
-
2 Model) and Ex Vivo (Excised Rat
Jejunum, Duodenum, and Ileum) Evaluation of Penetration
Enhancement Properties, Giuseppina Sandri, Maria Cristina
Bonferoni, Franca Ferrari, Cinzia Boselli, Carla Caramella,
AAPS PharmSciTech, 2010(3):11
-
1, 362
-
371
4. A modied fast (4 day) 96
-
well plate Caco
-
2 permeability
assay, Masashi Uchida, Tominaga Fukazawa, et al, Journal of
Pharmacological and Toxicological Methods, 2009(2):59
-
1,
page 39
–
43
参考文献: 默克提供的相关产品:
• 目录号 PSRP004R1:
PET膜,膜孔径1.0 µM, 96孔膜板及套件
• 目录号 MCHT24H48(原目录号PIHT12R48):
PET<


































 文献和实验
文献和实验





