相关产品推荐更多 >
万千商家帮你免费找货
0 人在求购买到急需产品
- 详细信息
- 文献和实验
- 技术资料
- 库存:
999
- 保质期:
12个月
- 供应商:
上海博尔森生物科技有限公司
- 保存条件:
-20℃
- 规格:
48T
产品说明
致病微生物检测系列基于独特的恒温荧光检测技术,可针对食品、动物产品等样品中致病微生物的特异核酸片段进行扩增,通过实时扩增曲线判定结果。本产品用于对肠出血性大肠杆菌 O104 的检测,检出限为 10³ CFU/ml。
产品组成(48 测试)
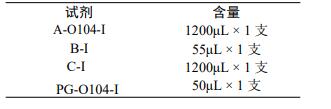
适用仪器
Dhelix-Q5、ESE Tube Scanner、Genie II、Deaou-308C 等恒温荧光检测仪,ABI 7500,ABI StepOne,LightCycler480,CFX 96 等荧光 PCR 仪。
自备耗材和仪器
①灭菌 1.5mL 或 2.0mL 离心管;②灭菌 0.2mL PCR 管或八联管;③冰盒;④移液器(0.5-10μL,10-100μL,
100-1000μL)及配套灭菌吸头;⑤离心机;⑥涡旋混匀器;⑦金属浴
注意事项
1. 本试剂检测灵敏度高。为了防止污染,实验要分区操作。
1) 第一区:试剂准备区。
2) 第二区:样本制备区。
3) 第三区:扩增及产物分析区。
分区之间最好进行物理性隔离,避免人为因素造成的污染。
2. 实验过程中穿戴工作服和乳胶手套,不同区域独立使用工具,需更换手套和实验服。
3. 严格按照操作步骤操作,试剂配制和加样等步骤请严格按照说明书要求在冰盒上操作。
4. 反应液中的成分对光敏感,应避光保存。试剂使用前要完全解冻,但应避免反复冻融,推荐使用前离心30秒,并按检测频次将反应液以适当体积分管保存。
5. 反应结束后,扩增管请置于密封袋内丢弃,当日清理,开盖易造成气溶胶污染,禁止开盖。
6. 不同批号试剂请勿混合使用,在有效期内使用。
7. 检出限为 10³ CFU/ml是以 1 ml 10³ CFU/ml增菌液离心后收集菌体再提取的细菌基因组 DNA作为模板。
样品处理
参照 《SN/T 3994-2014 动物产品中肠出血性大肠杆菌 O104:H4 检疫技术规范》中的 5.2 处理样品,对样品进行前增菌,制备的菌液保存待用。详细步骤请按照标准操作。
样品采集后应尽快检验,若不能及时检验,可在 2℃~4℃保存 18h。以无菌操作取检样 25g(ml)加入到含有225ml BPW 的无菌均质袋中,在拍击式均质器上连续均质 1min~2min;或放入盛有 225ml BPW 的无菌均质杯中,8000 rpm/min~10000 rpm/min 均质 1min~2min。无菌操作将样品转至 500mL 锥形瓶中,如使用均质袋,可直接进行培养,于 36℃±1℃培养 18h~24h。
实验操作
将试剂完全解冻,各组分离心30s。
1. 试剂配制(试剂准备区,放置于冰盒中进行):
若有N 个待检样品,则参照下表,按照 N+2 个数量计算各组分用量(N 个待检样品+1 个阴性对照+1 个阳性对),将反应液置于0.6ml 或者1.5ml 离心管中,涡旋混匀,离心30 秒,分装于0.2ml PCR 管中,并向每管加入1滴C-I(约 20μl)。
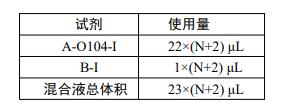
2. 模板制备(样本制备区)
建议使用试剂配套细菌组 DNA 提取系列产品,具体过程详见产品说明书。
3. 添加模板(样本制备区,放置于冰盒中进行)
向步骤 1 中已含有混合液的 PCR 管中分别加入 2 μL 模板,顺序为待测样品模板、阳性对照 PG- O104-I(阴性对照管无需额外加入模板),离心 30 秒,立即进行扩增反应。
4. 扩增反应(扩增及产物分析区)
①恒温仪器 63℃条件下反应 45 min。待仪器升温至 63℃后,新建程序,设置实验名称及反应时间,将步骤3中离心后的 PCR 反应管放入恒温荧光分子检测仪,点击开始检测。 ②若使用荧光定量 PCR 仪,则荧光基团选择 AM,淬灭基团选择 None,将 63℃ 15 s,63℃ 45 s 作为一个循环,于 63℃ 45 s 处收集荧光信号,45 个循环。
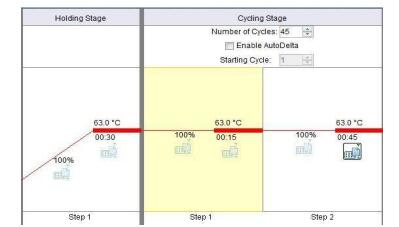
其他仪器请参照仪器说明书进行设置。
结果判定
①仪器自动判定结果,若显示示“阳性”或“+”,则样品中含有肠出血性大肠杆菌 O104;若显示“阴性” 或“-”, 且没有出现 S 型扩增曲线,则样品中不含有对肠出血性大肠杆菌 O104 或含量低于检出限。
②在荧光定量 PCR 仪上,根据有无“S”型扩增曲线判定结果。若有“S”型扩增曲线,则样品中含有肠出血性大肠杆菌 O104;若无“S”型扩增曲线,则样品中不含有肠出血性大肠杆菌 O104 或含量低于检测限。
NG 反应管结果显示“阴性”,PG 反应管结果显示“阳性”,此次检测结果有效,否则无效。如重复检测结果仍为无效,请与技术支持人员联系。
特别提示:本公司的所有产品仅可用于科研实验,严禁用于临床医疗及其他非科研用途!
风险提示:丁香通仅作为第三方平台,为商家信息发布提供平台空间。用户咨询产品时请注意保护个人信息及财产安全,合理判断,谨慎选购商品,商家和用户对交易行为负责。对于医疗器械类产品,请先查证核实企业经营资质和医疗器械产品注册证情况。
 文献和实验
文献和实验的作用——他们通过将引发此次疫情的O104:H4型肠出血性大肠杆菌 与2001年采集自一名溶血性尿毒症(HUS)体内的O104:H4型肠出血性大肠杆菌进行基因对比后,发现,两种菌株并非同源,引起此次德国EHEC暴发的O104:H4菌株来自一种肠聚集性大肠杆菌EAEC O104:H4 55989菌株的变异,其中还掺杂了一种目前未知的由志贺毒素产生的O104:H4菌株。 在这一场“战役”中,Harmsen教授主要采用的就是新一代测序 技术,他说,“至今,新一代测序技术已经遍布全球上百
的CaCl2 低渗溶液中,使细胞膨胀,同时Ca2 使细胞膜磷脂层形成液晶结构,使得位于外膜与内膜间隙中的部分核酸酶离开所在区域,这就构成了大肠杆菌人工诱导的感受态;2)此时加入DNA,Ca 2 又与DNA结合形成抗脱氧核糖核酸酶(DNase)的羟基-磷酸钙复合物,并粘附在细菌细胞膜的外表面上;3)经短暂的42℃热脉冲处理后,细菌细胞膜的液晶结构发生剧烈扰动,随之出现许多间隙,致使通透性增加,DNA分子便趁机进入细胞内。此外在上述转化过程中,Mg 2 的存在对DNA的稳定性起很大的作用,MgCl
能够吸收l噬菌体DNA,此后不久,Cohen等人用此法实现了质粒 DNA转化 大肠杆菌 的感受态细胞,其整个操作程序为:1)将处于对数生长期的细菌 置入0℃的CaCl2 低渗溶液中,使细胞膨胀,同时Ca2 使细胞膜 磷脂层形成液晶结构,使得位于外膜与内膜间隙中的部分核酸酶离开所在区域,这就构成了大肠杆菌人工诱导的感受态;2)此时加入DNA,Ca 2 又与DNA结合形成抗脱氧核糖核酸酶 (DNase)的羟基-磷酸钙复合物,并粘附在细菌 细胞膜 的外表面上;3)经短暂的42℃热脉冲处理
 技术资料
技术资料暂无技术资料 索取技术资料










