Olink Proteomics品牌商
1 年
手机商铺
- NaN
- 0
- 1
- 2
- 1
推荐产品
公司新闻/正文
Olink蛋白组学助力绘制脑内炎症蛋白地图,锁定AD关键标志物
94 人阅读发布时间:2025-10-09 10:59
研究背景
阿尔茨海默病(AD)是一种进行性神经退行性疾病,其特征是β淀粉样蛋白(Aβ)和tau蛋白的异常积累,最终导致神经元损伤和认知功能下降。
近年来,神经炎症被认为是AD进展的重要推动因素。研究表明,小胶质细胞(大脑中的免疫细胞)的异常激活可能加速Aβ斑块沉积和tau蛋白的扩散。然而,关于炎症生物标志物的研究结果缺乏一致性,对体液生物标志物的开发也面临重大挑战。

瑞典哥德堡大学的研究团队通过Olink技术分析脑脊液(CSF)和血浆中的炎症相关蛋白,以识别与TSPO(转运蛋白) PET信号相关的潜在生物标志物,更好地理解神经炎症在阿尔茨海默病中的作用。
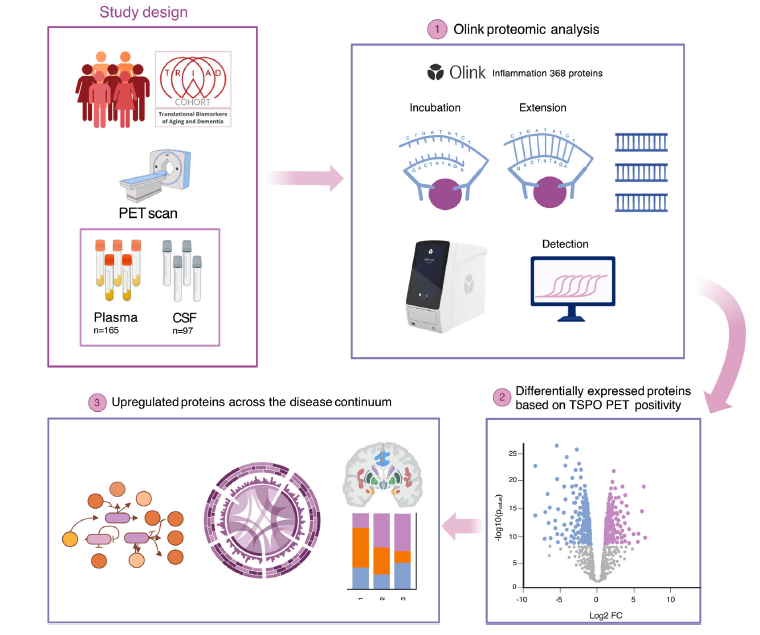
试验设计
亮点结果
这些差异表达的蛋白包括CD160、ANGPT1、EPCAM、CCL25和GAL等。功能富集分析显示,这些蛋白参与了多个与AD病理生理相关的关键过程,包括MAPK和ERK级联,细胞因子和白细胞迁移等。
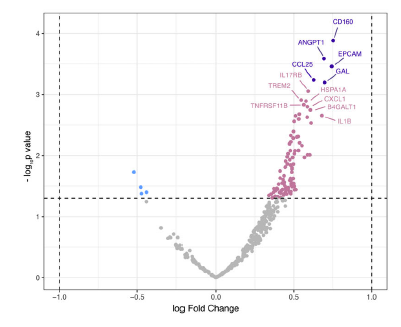
差异蛋白火山图
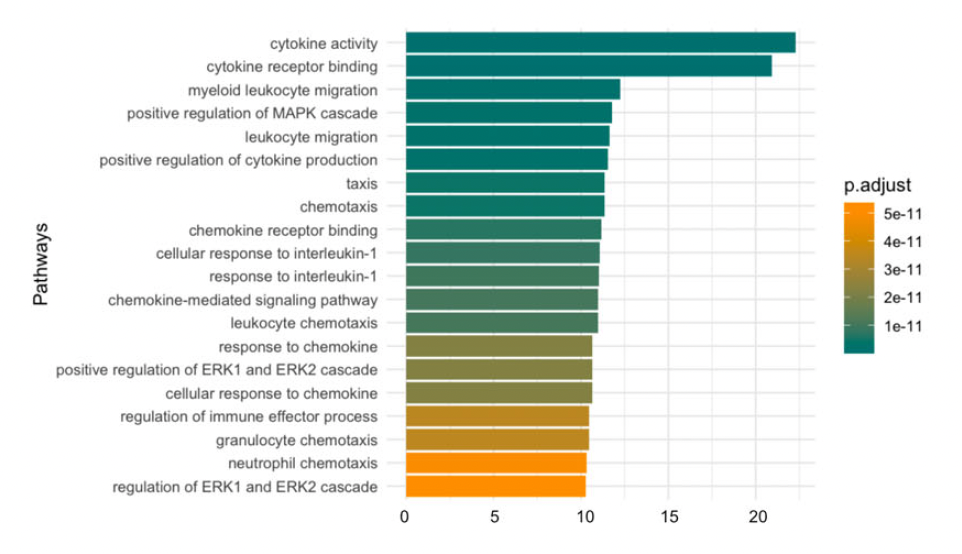
GO分析
在所有差异表达的蛋白中,CXCL1和TNFRSF11B两种蛋白表现出了与TSPO PET信号最显著的相关性。
Spearman相关性分析显示,炎症蛋白和AD影像生物标志物之间存在显著相关性。CXCL1和TNFRSF11B等10个蛋白与TSPO PET显著相关,并且随着TSPO PET信号从低到高,这些蛋白质的表达呈阶梯式增加。
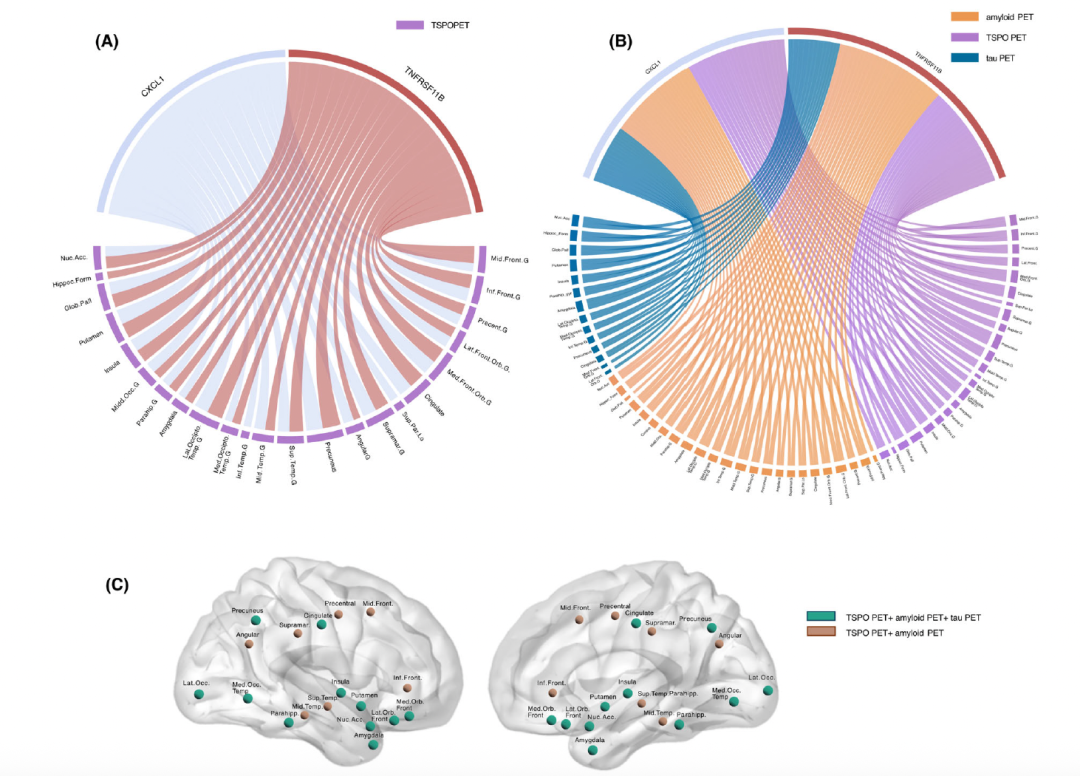
研究发现,选定的两种脑脊液(CSF)蛋白,CXCL1与TNFRSF11B,与TSPO PET信号摄取在23个解剖脑区中呈现显著正相关。值得注意的是,这些脑区具有明确的细胞与病理特征:富含小胶质细胞和星形胶质细胞(两类主导神经炎症反应的关键细胞类型),同时包含对维持髓鞘结构完整性至关重要的少突胶质细胞。
这种“空间分布一致性”(即炎症蛋白高表达区域与TSPO PET高摄取区域、特定胶质细胞富集区域高度重叠)强烈提示:CXCL1与TNFRSF11B所代表的神经炎症过程,与AD的核心病理变化(如小胶质细胞激活、髓鞘损伤)可能在相同脑区协同作用,进而共同推动疾病进展。
更进一步的分析发现,这些与TSPO PET显著相关的脑区,在不同PET模式(淀粉样蛋白PET、tau蛋白PET及TSPO PET)中均属于与AD病理密切关联的关键区域。其中,与淀粉样蛋白PET和TSPO PET相关的脑区比例显著高于tau PET相关脑区——这一现象暗示了AD病理演进的潜在时间顺序:神经炎症(表现为TSPO PET与炎症蛋白信号升高)可能发生于疾病早期,早于tau蛋白的显著沉积;而tau病理的明显进展可能出现在炎症反应之后。
写在最后
这项研究的发现具有重要的临床意义。首先,识别了与神经炎症相关的CSF蛋白,为AD的早期诊断提供了新的生物标志物。
其次,这些蛋白可以作为治疗监测的工具,评估抗炎药物在临床试验中的效果。针对神经炎症的治疗策略是AD药物开发的新兴领域,这些生物标志物将大大促进这一领域的进展。
此外,研究结果表明神经炎症可能在AD的早期阶段就发挥作用,这强调了早期干预的重要性。针对神经炎症的预防性措施可能会延缓或阻止疾病进展。
未来,我们也期待能够有更大规模和纵向研究进一步证明炎症蛋白在AD发生发展不同阶段的作用,并发现监测疾病进展和对抗神经退行性疾病的新路径。相信人类对抗阿尔茨海默病的战役,正在因这些微观世界的发现而迎来转机。
1. Pola I, Ashton NJ, Antônio De Bastiani M, Brum WS, Rahmouni N, Tan K, Machado LS, Servaes S, Stevenson J, Tissot C, Therriault J, Pascoal TA, Blennow K, Zetterberg H, Zimmer ER, Rosa-Neto P, Benedet AL. Exploring inflammation-related protein expression and its relationship with TSPO PET in Alzheimer's disease. Alzheimers Dement. 2025 Apr;21(4):e70171. doi: 10.1002/alz.70171. PMID: 40289873; PMCID: PMC12035552.