上海昂朴生物科技有限公司
2 年
手机商铺
- NaN
- 0.7999999999999998
- 1.7999999999999998
- 0.7999999999999998
- 3.8
推荐产品
公司新闻/正文
Nature |APOE4/4基因与阿尔茨海默病:iPSC+单细胞转录组助力发现小胶质细胞中的脂滴之谜
325 人阅读发布时间:2025-04-25 16:21
在阿尔茨海默病(AD)的研究领域,APOE4/4基因一直是一个备受关注的焦点。近期,发表在《Nature》上的一项研究为我们揭示了APOE4/4基因与小胶质细胞中脂滴形成之间的神秘联系,为理解AD的病理机制提供了新的视角。通过对 AD 患者脑组织的单细胞核 RNA 测序,确定了一种由脂质滴相关酶 ACSL1 表达定义的小胶质细胞状态(LDAM),其在APOE4/4基因型的AD患者中最为丰富。在人类诱导多能干细胞(iPSC)衍生的小胶质细胞中,纤维状Aβ以APOE依赖的方式诱导ACSL1表达、甘油三酯合成和脂质滴积累,含脂质滴的小胶质细胞的条件培养基可导致 Tau 磷酸化和神经毒性。此外,研究还探索了 PI3K 抑制清除小胶质细胞脂质滴积累的策略,为 AD 治疗提供了潜在方向。

研究背景
阿尔茨海默病(AD)是一种常见的神经退行性疾病,其特征包括记忆丧失、认知功能下降以及行为改变。APOE4/4基因是AD的一个主要遗传风险因素,与早发性AD和疾病进展密切相关。然而,APOE4/4基因如何影响小胶质细胞的功能,以及这些细胞如何参与AD的病理过程,仍然是一个未解之谜。研究人员通过单核RNA测序分析了AD患者的脑组织,发现了一种特定的小胶质细胞状态,这些细胞以表达脂滴相关酶ACSL1为特征。进一步的实验中,研究人员利用诱导多能干细胞(hiPSCs)技术,从小胶质细胞中诱导出脂滴,并研究了这些脂滴在不同APOE基因型下的形成和功能。
主要内容
1. AD 中与脂质相关的 ACSL1+ 小胶质细胞为了研究人类AD死后脑组织的转录状态与APOE基因型的关系,研究人员对来自被诊断为APOE4/4基因型AD患者、APOE3/3基因型AD患者以及年龄和性别匹配的APOE3/3基因型对照患者的新鲜冷冻额叶皮层组织进行了单核RNA测序。研究发现,ACSL1是AD-APOE4/4 小胶质细胞中差异表达最显著的基因,其在AD脑组织的小胶质细胞中特异性上调,且在APOE4/4基因型中上调程度更大。ACSL1+小胶质细胞构成了一种不同于稳态和疾病相关小胶质细胞的状态,称为 LDAM。AD-APOE4/4脑组织中LDAM的比例最高,其次是AD-APOE3/3,对照脑组织中最少。
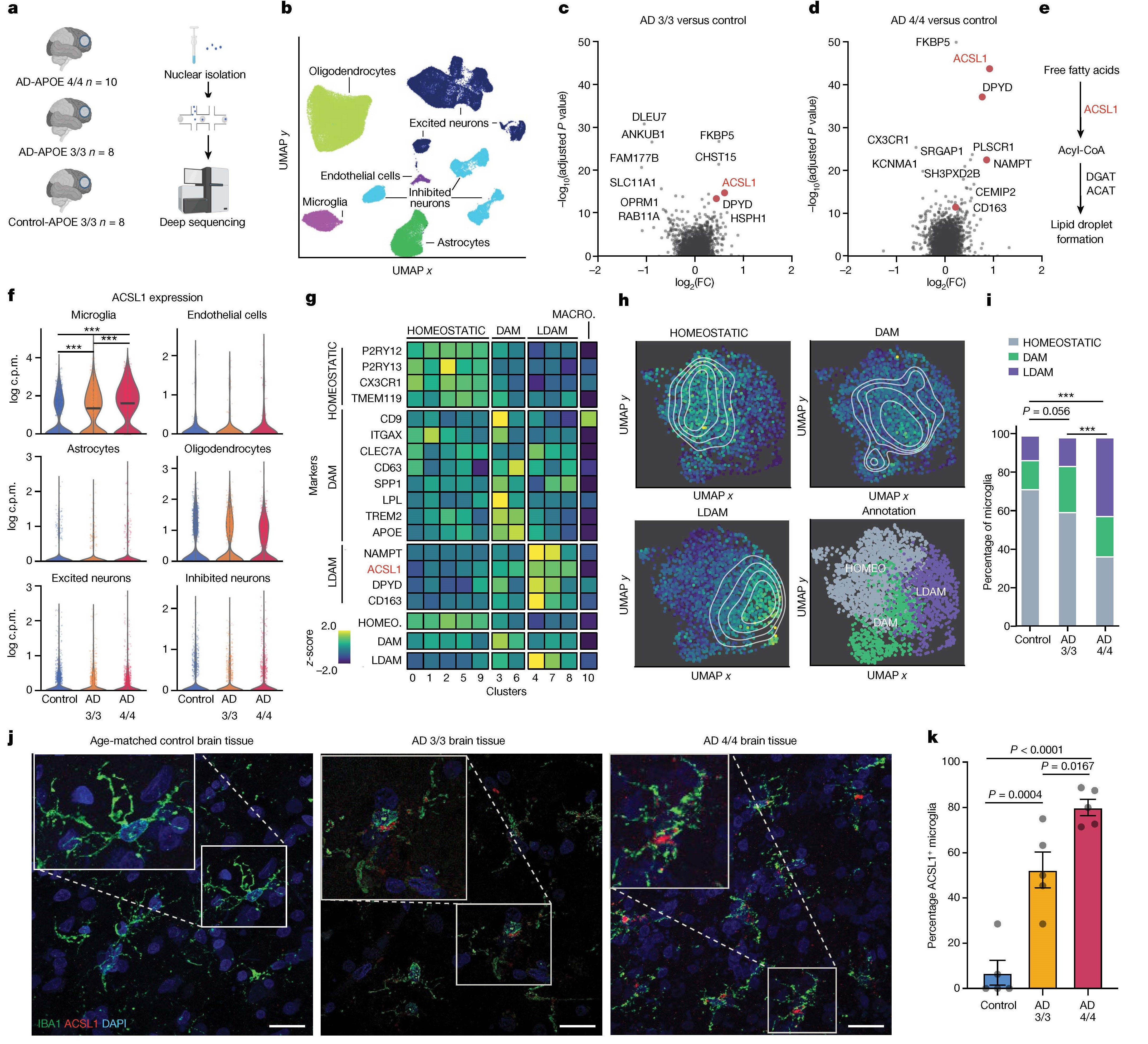
图1 AD小胶质细胞的脂质转录状态由ACSL1确定
2. 脂质积累与AD病理的关联 AD-APOE4/4患者大脑中存在大量类似脂质滴的核周油红O阳性脂质体,且脂质体数量与认知能力呈负相关,与Aβ斑块数量和Tau病理水平呈正相关。在 J20/APOE3和 J20/APOE4 AD小鼠模型中,与年龄匹配的野生型小鼠相比,有更多的 LD+小胶质细胞。
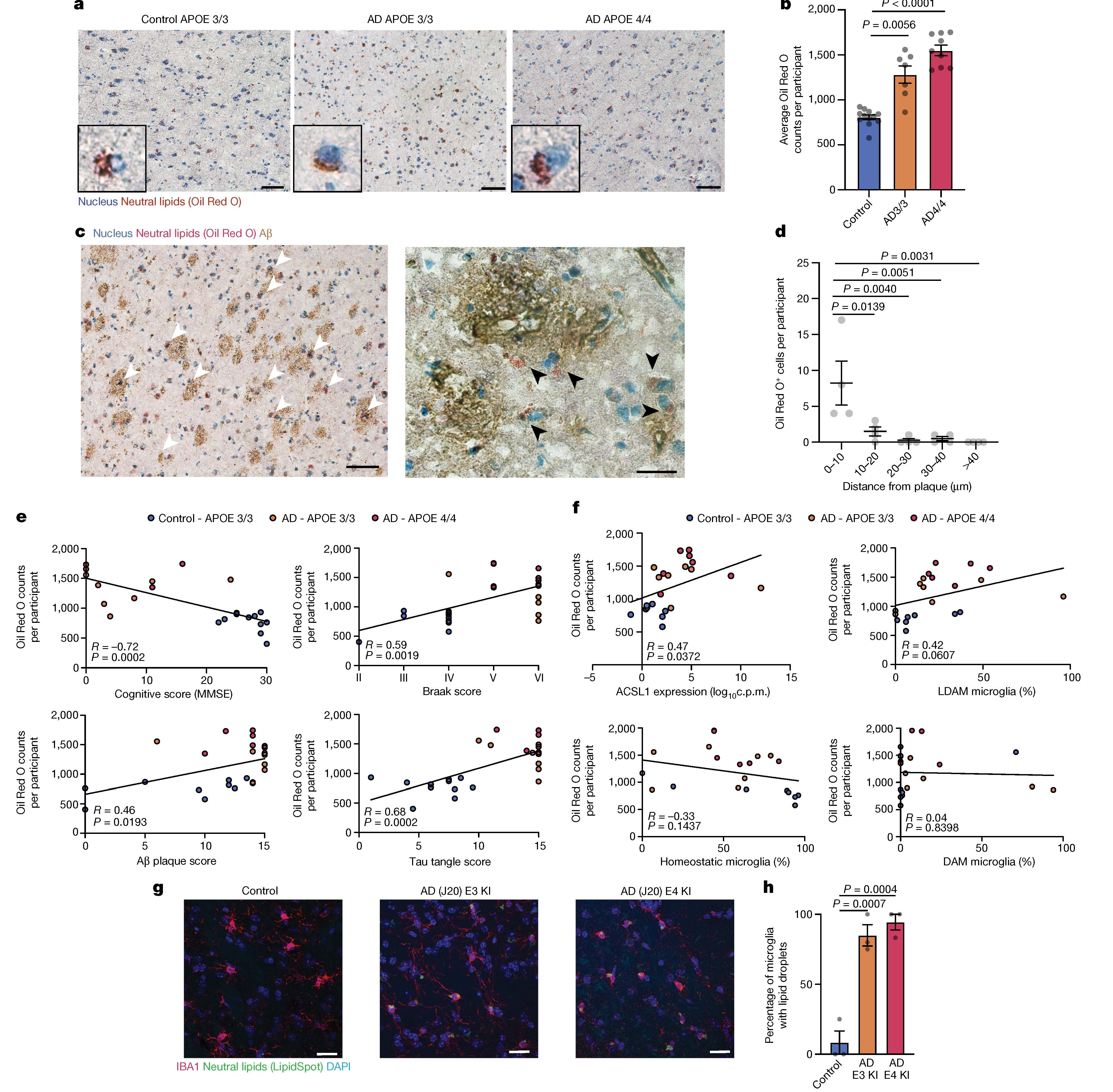
图2 脂质积累与注意力缺失症病理有关
3. fAβ刺激后ACSL1和甘油三酯增加 将APOE4/4和同基因APOE3/3的iPSC分化为小胶质细胞(iMG),用纤维状 Aβ(fAβ)处理,检测脂质滴积累、基因表达等。结果发现,APOE4/4 iMG 中脂质滴积累增加,且这种增加在APOE4/4背景下更为明显。fAβ 刺激还导致 LD 相关基因PLIN2和ACSL1的表达上调。通过 CRISPR-KO筛选确定了甘油三酯代谢调节因子是脂质滴积累所需的关键基因类别,ACSL1是脂质滴形成的重要基因之一。抑制 PI3K可减少APOE4/4 iMG中脂质滴的形成,并改善小胶质细胞的功能。
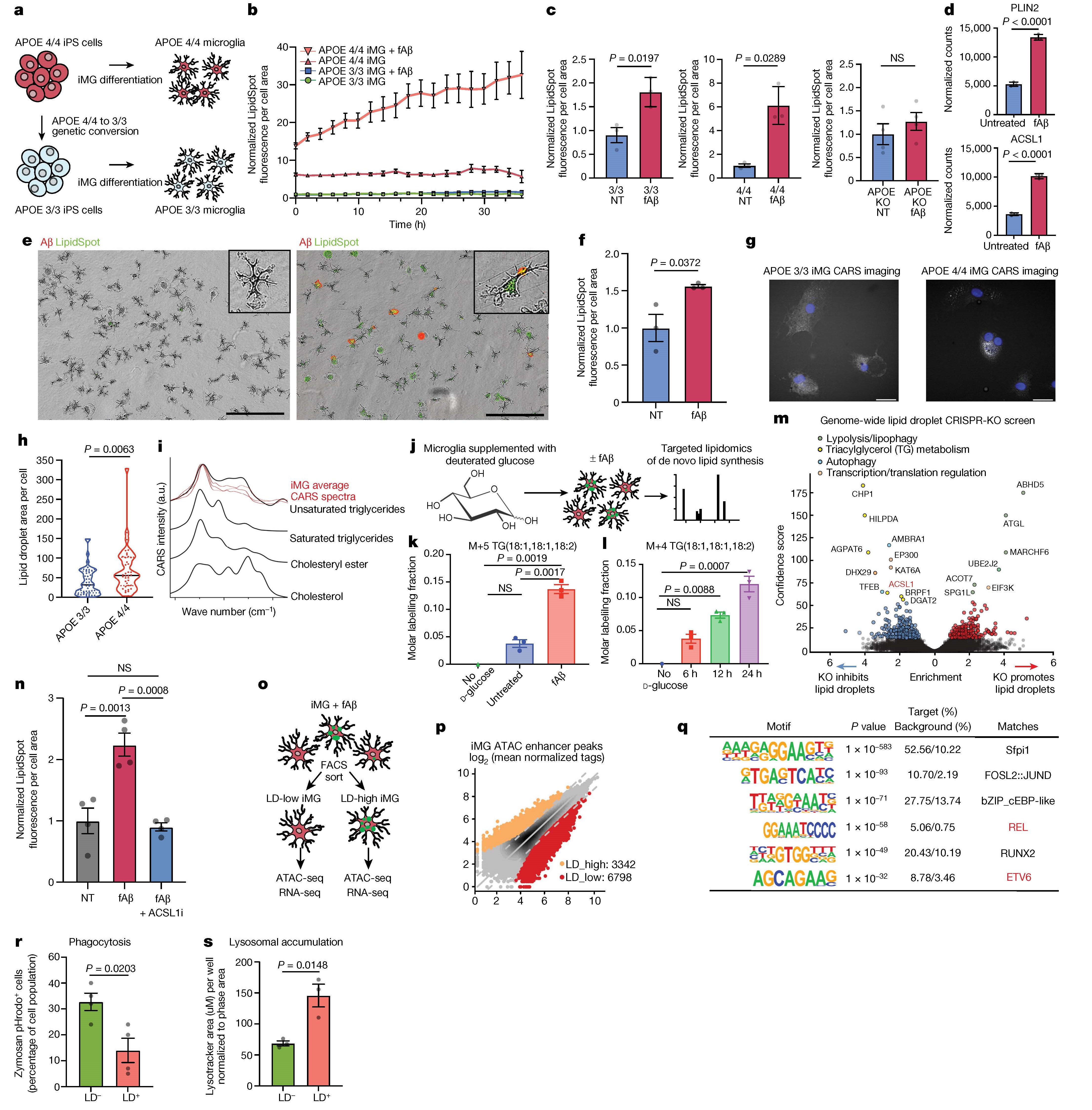
图3 fAβ 刺激后 iMG增加ACSL1和三酸酯脂质合成
4. LD+ iMG诱导神经元中的pTau和细胞凋亡 用 LD-high APOE4/4 iMG条件培养基处理人iPS细胞衍生的神经元,可诱导高浓度的 pTau和细胞凋亡,而 LD-low条件培养基的作用与未处理条件相似。神经元在 LD-high 条件培养基处理后,脂质滴染色增加,且积累的甘油三酯与iMG中积累的种类相同。
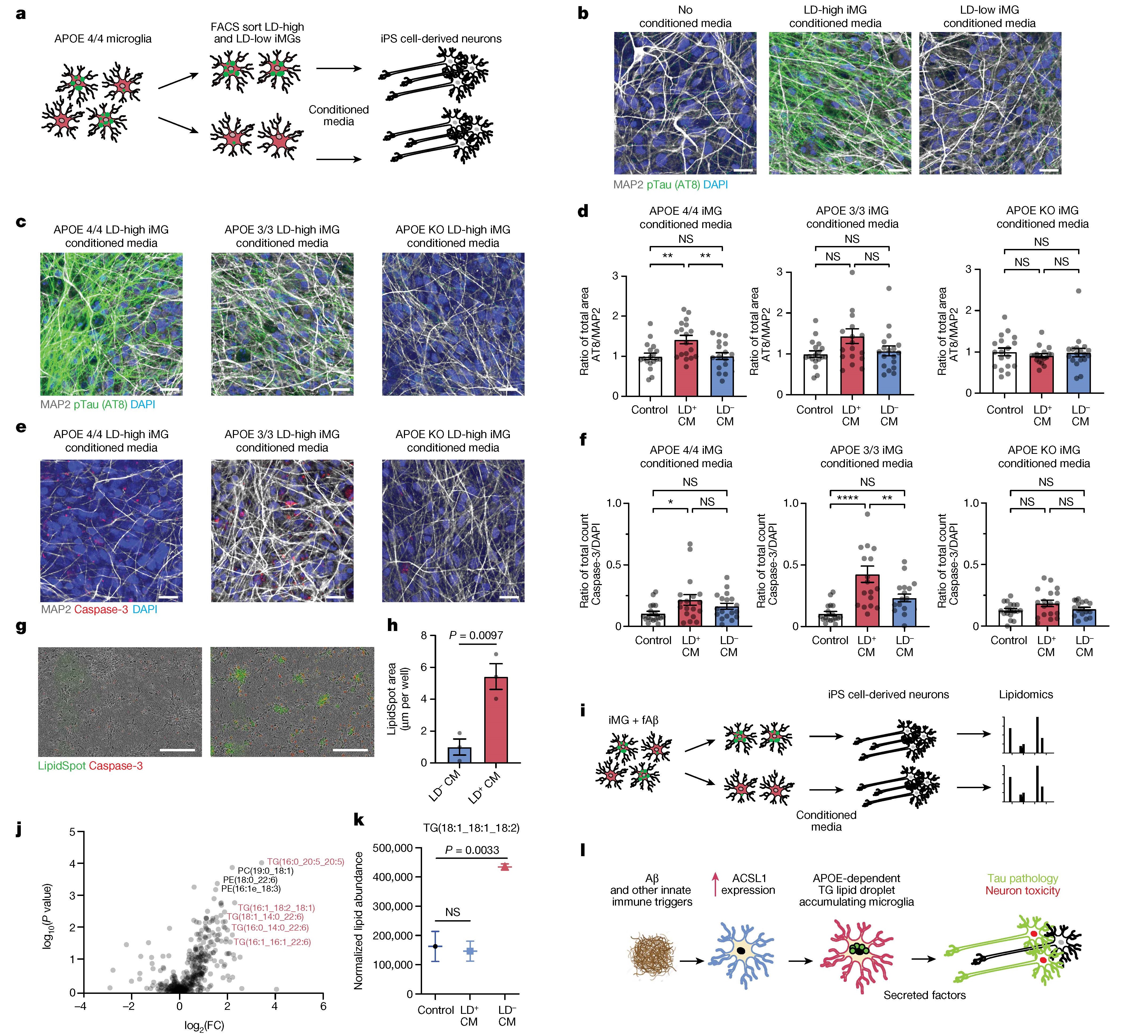
图4 LD+小胶质细胞诱导神经元Tau磷酸化和细胞死亡
小结
本研究发现了一种在人类大脑中存在的小胶质细胞状态,其特征为脂质积累和脂质合成相关基因的上调,且这种状态在 AD 大脑中更为普遍,在APOE4/4基因型个体中更为富集。研究还揭示了fAβ可诱导iMG中甘油三酯合成和脂质滴积累,且 LD-high 小胶质细胞的条件培养基可诱导神经元出现AD病理特征。PI3K抑制可能是清除小胶质细胞脂质滴积累的一种策略,但需要进一步研究其对脂质自噬通量的影响。通过结合iPSC技术和多组学方法,研究人员能够从多个维度深入研究阿尔茨海默病的病理机制,揭示脂滴形成和小胶质细胞功能异常的关键分子机制,并为开发新的治疗方法提供了强有力的工具。这种方法不仅提高了研究的效率和准确性,还为个性化医学的发展提供了新的可能性。



