北京基尔比生物科技有限公司
3 年
手机商铺
- NaN
- 0
- 1
- 0
- 3
推荐产品
技术资料/正文
细胞类器官培养简史: From Harrison to Kirkstall Quasi Vivo Organs-on-a-Chip
141 人阅读发布时间:2025-07-09 10:25
北 京 基 尔 比 生物科技公司主营产品:
Kilby 全自动3D细胞类器官培养仪,
Kilby Gravity 微重力三维细胞培养系统,
Kilby Bio类器官芯片摇摆灌注仪,动态3D细胞培养系统
Kirkstall Quasi Vivo®类器官3D仿生动态共培养系统
一、关键词
细胞培养、二维细胞培养、三维细胞培养、类器官、球体、器官芯片
二、摘要
概述了细胞培养领域的历史里程碑,从19世纪80年代Wilhelm Roux的开创性实验,到Ross Granville Harrison在20世纪初的奠基工作,再到Alexis Carrel的永生化细胞研究。
后续Johannes Holtfreter、Aron Moscona、Joseph Leighton等推动了三维细胞培养发展,2006年Takahashi和Yamanaka诱导多能干细胞(iPSCs)的发现具有革命性意义。近年来,球体、类器官和器官芯片技术成为研究热点,文章还探讨了从二维到三维细胞培养的转变及未来方向。

三、细胞培养历史概述
1. 早期起源(19世纪末-20世纪初)
- Robert Koch(19世纪80年代):改进微生物培养技术,使用明胶固化培养基,提出“科赫法则”,强调灭菌的重要性,与Richard Petri合作改进培养皿(Petri dish)。
- Wilhelm Roux(19世纪80年代):通过鸡胚细胞实验,证明细胞可在盐溶液中在体外存活。
- Leo Loeb:在华盛顿大学开展细胞培养、移植和激素研究,为实验病理学奠定基础。
- Ross Granville Harrison(1906年):在试管中培养蛙神经纤维组织,使用血块、盐溶液和琼脂作为培养基,开发“悬滴技术”,通过无菌操作(如灭菌手术器械)将细胞培养延长至5周,其著作《Observations on the Development of Living Nerve Fibers》具有重要意义。
2. 技术发展与突破(20世纪初-中期)
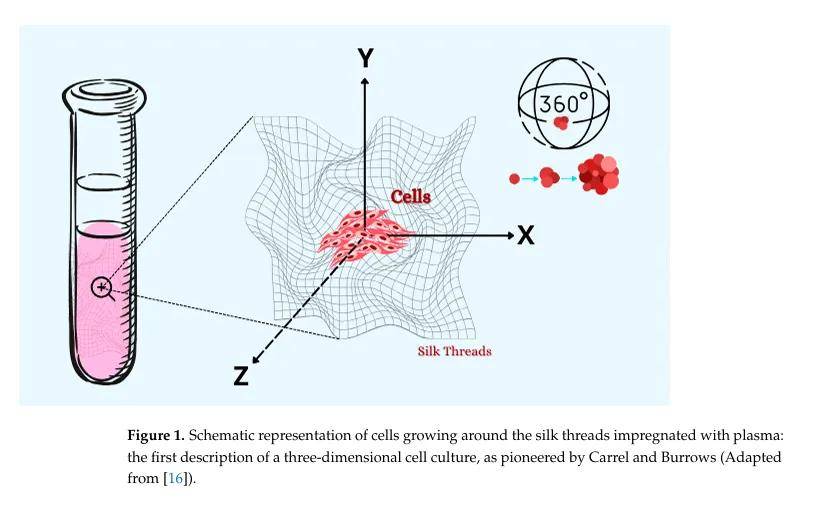
- Alexis Carrel:1912年诺贝尔生理学或医学奖得主,改进悬滴培养法,设计“卡雷尔培养瓶”,首次详细描述三维细胞培养(利用丝绸线培养组织碎片),与Charles Lindbergh合作,后者开发血清分离方法并引入耐高压的“Pyrex玻璃”器皿,成功培养出首个永生化鸡胚心肌细胞系。
- HeLa细胞系(1951年):源于Henrietta Lacks的宫颈腺癌组织,由George Gay实验室培养成功,具有强增殖能力,至今仍广泛应用于研究。
- 三维培养技术先驱:
- Johannes Holtfreter:开发球形细胞聚集体培养方法,通过搅拌培养瓶促进细胞接触和营养扩散。
- Aron Arthur Moscona:利用锥形瓶持续搅拌培养细胞,防止细胞贴壁,促进三维细胞聚集体形成,开展细胞嵌合体研究。
- Joseph Leighton(20世纪50年代):使用纤维素海绵三维基质培养细胞,证明三维培养更能模拟体内细胞行为。
3. 干细胞研究与突破(20世纪60年代-21世纪初)
- 骨髓干细胞研究:Ernst McCulloch和James Till(20世纪60年代初)通过骨髓细胞移植实验,提出“脾集落”概念,为骨髓干细胞定义奠定基础。
- 间充质干细胞研究:Alexander Friedenstein(20世纪60年代起)从骨髓中分离出“成纤维细胞集落形成细胞(FCFCs)”,即间充质干细胞的前身,证明其多向分化潜能。
- 胚胎干细胞:1981年,Martin Evans和Matthew Kaufman建立小鼠囊胚细胞系,Gail R. Martin首次使用“胚胎干细胞”术语。
- 人类胚胎干细胞:1998年,James Thomson团队从人类囊胚内细胞团培养出人类胚胎干细胞。
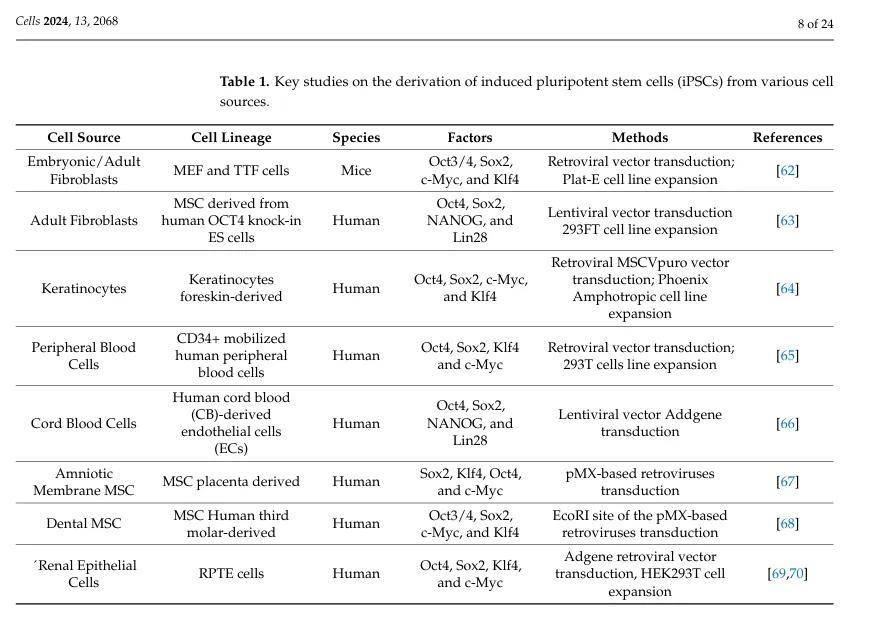
- 诱导多能干细胞(iPSCs):2006年,Kazutoshi Takahashi和Shinya Yamanaka通过Oct3/4、Sox2、Klf4、c-Myc四因子将成纤维细胞重编程为iPSCs;2007年,James Thomson团队使用Oct4、Sox2、NANOG、Lin28四因子获得人类iPSCs。
四、二维与三维细胞培养技术
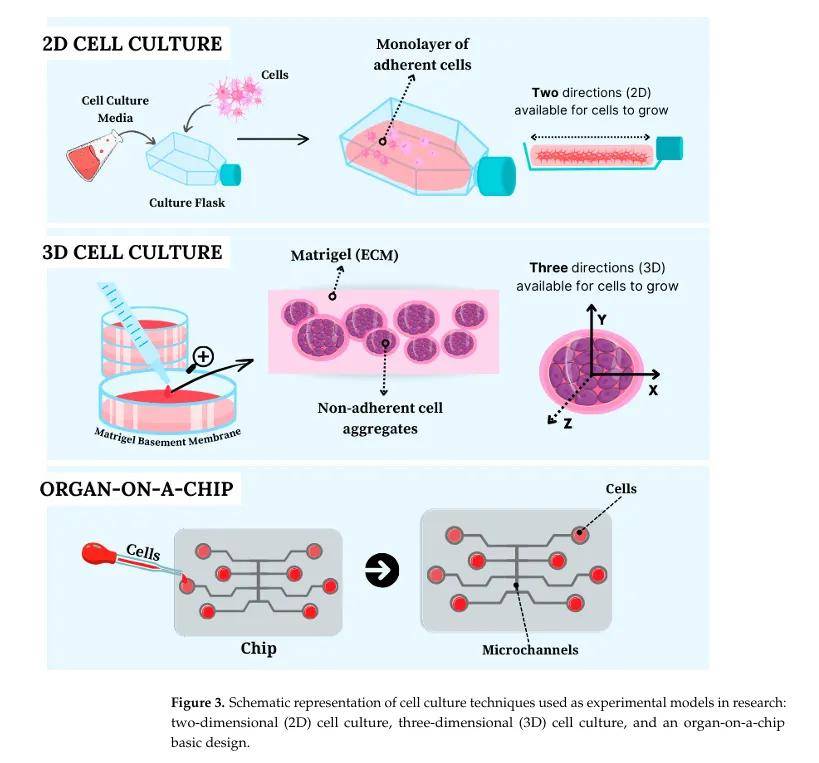
1. 二维(2D)细胞培养
- 原理:细胞在平面贴壁表面(如培养皿、培养瓶)生长,通过特定涂层(如多聚赖氨酸、Matrigel、纤连蛋白)促进非贴壁细胞黏附。
-应用:用于研究细胞分化、迁移、生长等生理机制,广泛应用于癌症研究、毒性测试(如药物候选物评估),符合“3Rs”原则(减少、优化、替代动物实验)。
- 局限性:缺乏细胞与细胞外基质的接触,难以模拟体内细胞结构和生理特性,部分细胞系(如肝细胞)难以在二维环境中稳定培养。
2. 三维(3D)细胞培养
- 球体(Spheroids):由细胞自组织形成的球形聚集体,无需预定义基质,可通过悬滴法、磁悬浮等方法制备,存在营养、氧气等梯度,核心易形成坏死区,适用于癌症模型研究。
- 类器官(Organoids):比球体更复杂,由干细胞或分化细胞形成,具有自组织、多细胞性和功能性,可模拟器官发生和功能,应用于遗传疾病、肿瘤、药物研发等领域(如脑类器官研究小头畸形,肝类器官研究囊性纤维化)。
- 发展里程碑:1970年Robert Sutherland开发多细胞球体;1972年Tom Elsdale和Jonathan Bard使用胶原蛋白凝胶作为三维支架;1977年Matrigel被引入作为细胞外基质提取物。
- 局限性:缺乏功能性血管化,导致营养分布不均和坏死;结构组织与体内器官存在差异;操作复杂、成本高。
五、器官芯片(Organ-on-a-Chip)
- 原理:基于微流控系统,将三维细胞培养集成在芯片中,通过微通道实现细胞间相互作用,可模拟血管化、机械刺激和组织灌注。 例如英国Kirkstall Quasi Vivo多功能细胞类器官芯片
- 典型模型:
- 肺芯片(2010年):由多孔膜分隔的两个微通道组成,分别培养肺泡上皮细胞和肺微血管内皮细胞,可模拟呼吸运动和肺部感染。
- 心脏芯片:基于人类iPSCs分化的心肌细胞,可模拟心脏收缩(频率55~80 bpm),用于药物评估。
- 脑芯片:模拟神经祖细胞迁移,用于神经发育和肿瘤研究。
- 肝芯片、肾芯片、胰腺芯片:分别用于评估肝毒性、肾毒性和研究囊性纤维化相关胰腺功能障碍。
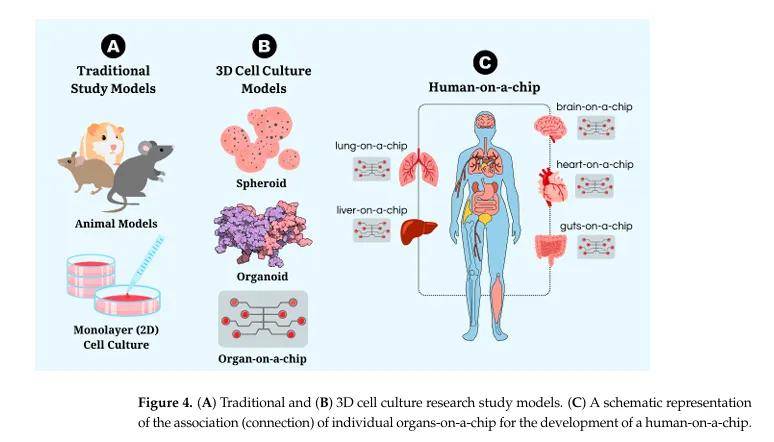
六、细胞培养的新展望
- 人体芯片(Human-on-a-Chip):整合多个器官芯片,通过微通道模拟全身生理相互作用,有望替代动物实验,用于系统生物学研究和药物测试。
- 挑战:缺乏通用细胞培养基;血管化技术尚未成熟;微通道设计需模拟体内血管特性。
- 应用前景:推动个性化 medicine 发展,加速药物研发,深入解析疾病机制。

七、结论
二维细胞培养为生物医学研究奠定了基础,但存在局限性;三维细胞培养(球体、类器官)和器官芯片技术通过模拟体内微环境,在临床前研究、药物筛选和再生医学中显示出巨大潜力,未来将进一步缩小基础研究与临床应用的差距。
北 京 基 尔 比 生物科技公司主营产品:
Kilby 全自动3D细胞类器官培养仪,
Kilby Gravity 微重力三维细胞培养系统,
Kilby Bio类器官芯片摇摆灌注仪,动态3D细胞培养系统
Kirkstall Quasi Vivo®类器官3D仿生动态共培养系统
请联系我们,了解更多产品详情!