上海生物芯片有限公司
3 年
手机商铺
- NaN
- 0.7000000000000002
- 0.7000000000000002
- 1.7000000000000002
- 0.7000000000000002
推荐产品
公司新闻/正文
单细胞空间多组学揭示肛周克罗恩病瘘管新机制
169 人阅读发布时间:2025-05-14 10:52
单细胞空间多组学技术掀起了生命科学研究的革命。这些技术不仅能够揭示细胞异质性,还能展示细胞在组织中的空间分布,为理解疾病的病理机制提供了全新视角。利用这些先进技术,研究人员首次全面解析了肛周克罗恩病瘘管(PCD)的复杂微环境。揭示了致病性Th17细胞和髓系细胞的关键贡献,并为抗TNF治疗的效果提供了全新解释。这项研究不仅深化了对PCD病理机制的理解,还展示了单细胞空间多组学技术在临床研究中的巨大潜力。
1 研究背景
肛周瘘管是克罗恩病(CD)患者常见的并发症,严重影响生活质量。尽管抗TNF药物(如英夫利昔单抗)在临床上取得了一定疗效,但其具体机制尚不明确。为了深入理解肛周克罗恩病瘘管(PCD)的病理机制和细胞异质性,研究人员采用了单细胞RNA测序(scRNA-seq)、质谱流式细胞术(CyTOF)和空间转录组学等先进技术,分析PCD和非克罗恩病肛周瘘管(IPF)的细胞组成、免疫反应及治疗效果。研究揭示了IFN-γ和TNF-α信号通路的作用,解析了致病性Th17细胞和髓系细胞的贡献,并评估了抗TNF治疗对瘘管愈合的影响。此外,通过空间转录组学,研究人员揭示了PCD和IPF中的共有和独特微环境,为开发更有效的治疗策略提供了新见解。
2 文章详情
文章题目:Single-Cell and Spatial Multi-omics Reveal Interferon Signaling in the Pathogenesis of Perianal Fistulizing Crohn’s Disease
中文题目:单细胞和空间多组学揭示肛周瘘管型克罗恩病中的干扰素信号通路
发表时间:2024.11
期刊名称:bioRxiv
影响因子:无
实验平台:10x Genomics单细胞转录组测序+10x visium空间转录组测序+质谱流式细胞术
DOI:10.1101/2024.11.08.620717
3 研究结果
1.单细胞转录组学解析肛周瘘管中的细胞异质性
为了理解肛周瘘管的细胞组成,研究人员利用单细胞RNA测序分析了9名PCD和6名IPF患者的活检样本。通过严格质量控制,保留了 56,560个高质量细胞,并根据经典基因标志物解析了主要细胞类型及其亚群,包括T细胞、先天淋巴样细胞(ILCs)、B细胞、浆细胞、髓系细胞、基质细胞和内皮细胞。这些结果揭示了肛周瘘管中复杂的细胞异质性,为后续病理机制研究提供了基础。
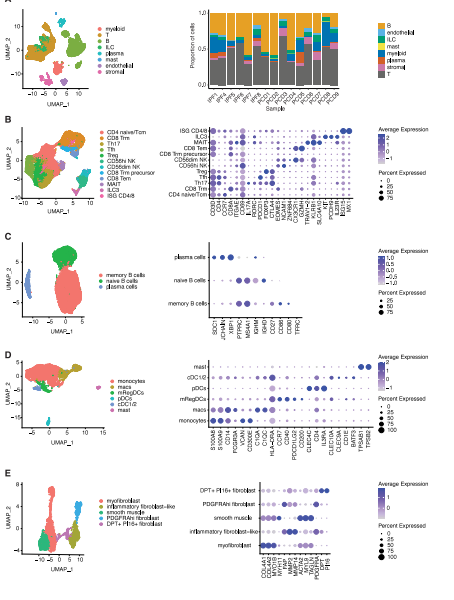
Fig1. 单细胞RNA测序揭示瘘管管道的细胞异质性
2.PCD特征为增强的IFN-γ和TNF-α反应
研究人员探讨了PCD中IFN-γ和TNF-α信号通路的作用,发现多个配体-受体对(如IFNG-IFNGR2、GZMB-PGRMC1、IL2-IL2RG等)在PCD中富集。TNF-α和IL22、IL13的表达上调进一步验证了这些细胞因子的重要性。此部分揭示了PCD中IFN-γ和TNF-α信号通路的增强及其对EMT基因表达的影响。
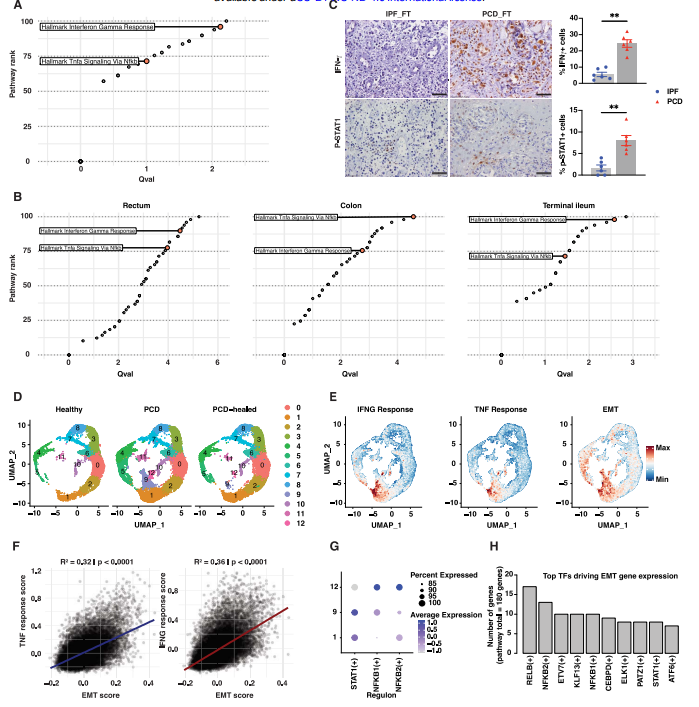
Fig2. IFN-γ信号是PCD的一个显著特征
3.致病性Th17细胞和髓系细胞在PCD中贡献IFN-γ信号
通过分析IFNG通路,研究人员发现IFN-γ主要由致病性Th17细胞和调节性T细胞(Tregs)产生。髓系细胞表达了更多的NLRP3、AREG和IFN-γ反应性趋化因子CXCL9和CXCL10。这些数据表明,pTh17和髓系细胞是PCD中IFN-γ信号增强的基础,突显了它们在疾病发展中的作用。
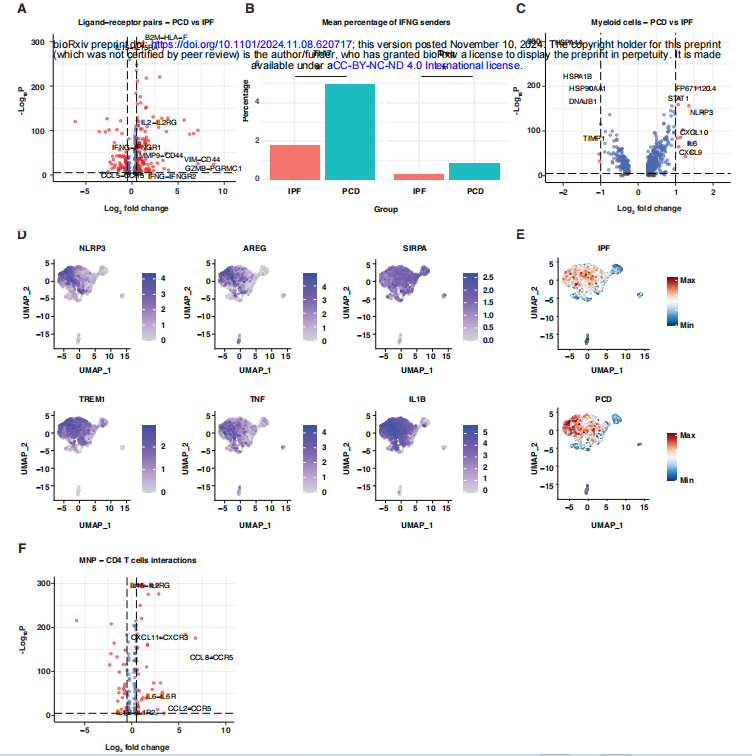
Fig3. 病理性的髓系细胞-Th17细胞相互作用是PCD瘘管中IFN-γ反应的基础
4.CyTOF揭示PCD瘘管通道及周围组织中的致病性免疫反应
使用质谱流式细胞术(CyTOF),研究人员分析了PCD、NPCD和IPF患者的黏膜免疫细胞群。结果显示,瘘管通道中CD4 T细胞表达激活标志物CD137和CD56显著增加,循环 Th17细胞也显著增加。此外,PCD瘘管通道中 CD172a/b+ TREM1+ CD14+单核吞噬细胞增加,且T细胞耗竭标志物CD39增加而CD127 减少。CyTOF数据佐证了转录组学发现,强调了致病性免疫反应的重要性。
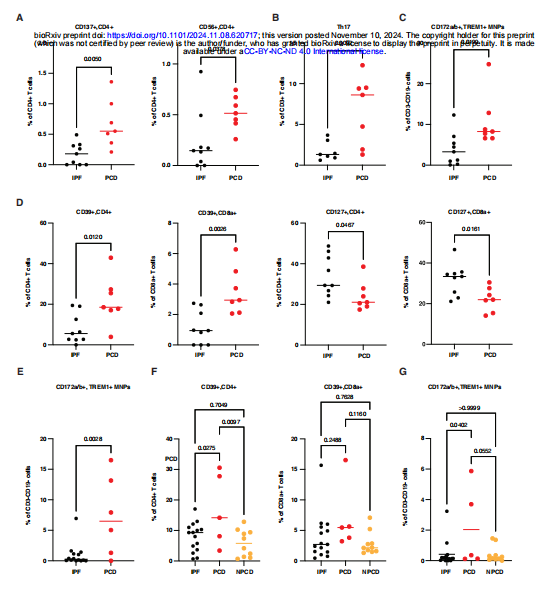
Fig4.CyTOF揭示了瘘管管道与周围组织之间的免疫学关系
5.抗TNF治疗对PCD瘘管的转录组影响
通过加权基因共表达网络分析(WGCNA),研究人员识别了与抗TNF治疗相关的基因模块。“lightpink1”模块下调,包含T细胞、髓系细胞和干扰素反应相关基因;“royalblue2”模块上调,涉及结构蛋白、细胞代谢和DNA复制等基因。这些数据表明,抗TNF治疗通过抑制致病性T细胞和髓系细胞特征,同时促进细胞增殖和黏膜屏障完整性,从而促进瘘管愈合。
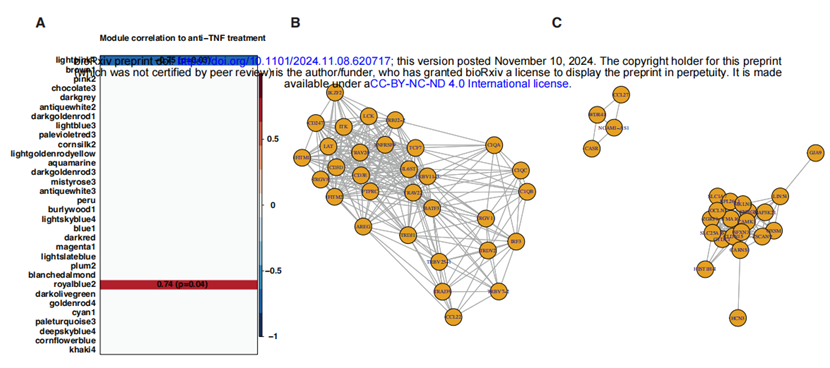
Fig5. PCD瘘管管道中的基因表达模块与抗TNF治疗相关
6.空间转录组学解析IPF和PCD瘘管的共有和独特微环境
研究人员使用10x Visium对IPF和PCD瘘管通道进行了空间转录组学分析,识别出六个空间相关簇,揭示了共有转录组生态位。通过细胞类型解卷积和配体-受体相互作用分析,发现了成纤维细胞、上皮细胞和免疫细胞的分布特征及特异性信号对。最后,研究人员发现pTh17和NLRP3+ AREG+ MNPs在PCD样本中广泛存在,伴随IFNG信号增强,强调了这些细胞在维持炎性微环境中的关键作用。
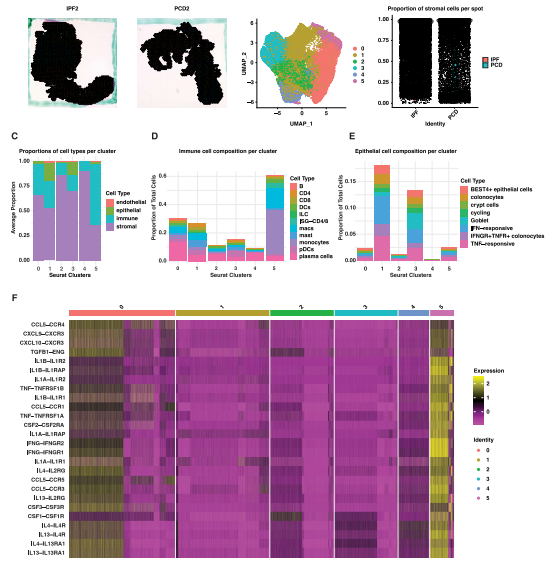
Fig6. 空间转录组识别了瘘管管道之间共享的转录组微环境
4 主要结论
本研究利用单细胞转录组、空间转录组和质谱流式技术揭示了PCD和IPF瘘管通道中的免疫和非免疫细胞组成。PCD瘘管显示了包括干扰素γ(IFNG)反应和TNF信号通路在内的过度激活的致病途径,主要发生在髓系和间质细胞中。PCD患者的肠道细胞表达了更高水平的IFNG反应基因和上皮-间质转化(EMT)相关基因。此外,PCD患者的瘘管通道和回肠黏膜中发现了扩展的IFNG+致病性Th17细胞,这些细胞表达了升高的炎症介质。CyTOF还识别出PCD患者在瘘管通道、瘘口和直肠中存在偏斜的免疫细胞表型,包括扩展的Th17细胞、增加的致病性髓系细胞和改变的T细胞耗竭标志物。进一步分析还揭示了与抗TNF治疗相关的细胞模块。多组学分析描绘了PCD中免疫、间质和上皮细胞的图谱,突显了过度激活的IFNG信号在瘘管通道和腔内黏膜中的致病作用,并确定IFNG为PCD的潜在治疗靶点。
> 参考文献:
Cao, Siyan et al. “Single-Cell and Spatial Multi-omics Reveal Interferon Signaling in the Pathogenesis of Perianal Fistulizing Crohn's Disease.” bioRxiv : the preprint server for biology 2024.11.08.620717. 10 Nov. 2024.