产品分类
联系方式
- 公司地址
-
上海市浦东新区蔡伦路150号
邮编:200120
- 联系电话
- 021-****6258登录查看商家电话
- 传真号码
- 电子邮箱
- service@****io.net登录查看商家邮箱
- 公司网址
- http://www.kesci.net
公司新闻
体内基因转染—我与小动物的相爱相杀
发布时间:2021-11-19 10:57 | 点击次数:
说起生物医药科研界的让人撕心裂肺的实验,动物实验肯定是其中一大块。裸鼠成瘤,各种疾病造(zuo)模(nie),让我们饱尝与鼠小弟的相爱相杀。
既然有牺牲,还得有价值。如何让鼠小弟们的牺牲换来高逼格的实验数据?自然少不了时下最火爆的动物体内基因转染技术。
所谓基因转染,通俗一点说,主要指基因上调或下调(即 Gain of function OR loss of function)。动物体内基因的上下调,其实现方法主要包括:基因工程小鼠及病毒载体介导动物体内基因转染。
基因工程小鼠
最经典传统的动物体内基因干预,当属基因工程小鼠了。基因工程小鼠包括转基因小鼠,(TG mouse,transgenetic mouse),敲除小鼠(KO mouse,Konckout mouse),敲入小鼠 (KI mouse,Knockin mouse)。在引入 Cre-loxP 系统后,又发展了组织特异性 TG 和 KO 小鼠。
基因工程小鼠对生物医药研究与研发发挥了巨大的作用,但也存在不少的限制因素:
- 从受精卵开始的基因干预,经过发育的长时间复杂代偿,所表现出来的功能表型和实际的基因功能表型可能存在巨大的偏差。(2015 年 nature 杂志发表了 Didier Stainier 研究小组发现受精卵敲除 egfl7 基因和成年后用 RNA 干扰阻断 egf17 的表达,模式生物所得到的表型完全不一样。)
- 基因工程小鼠周期长,成本相对高。是否还记得,在动物房里伺候老鼠的那些日子,一把屎一把尿拉扯它长大,给它找对象,还得帮它养孩子……
病毒载体介导的动物体内基因转染
目前最主流的病毒载体工具有三种:腺病毒(adenovirus),慢病毒(lentivirus),腺相关病毒(AAV,adenovirus associated virus)。相比较基因工程小鼠的局限性,病毒载体工具有如下优势:
1)对成年的动物直接进行急性的基因干预,避免了发育代偿的问题;
2)病毒载体相对与基因工程小鼠来说,周期、成本要小得多;
3)病毒载体介导的基因干预可以在动物造模后进行,作为一个基因治疗干预手段,与临床更加接近,而不仅仅是完成基因功能研究。
动物活体基因转导工具比较:
| 慢病毒 | 腺病毒 | 腺相关病毒(AAV) | |
| 特点 | 整合基因组,稳定表达,被广泛应用于建立稳赚细胞系 | 可插入片段大;瞬时表达能力强,体内注射72小时即开始强烈表达 | 安全性极高;免疫原性低,长效表达(稳定表达3-6个月);病毒颗粒小,感染均一性强;注射方式多样;是体内基因转导最优方式 |
| 体内应用局限 | 滴度底,应用于动物活体(in vivo)水平劣势明显;随机插入基因组,有致瘤风险 | 免疫原性高,可能引发强烈的免疫反应,导致动物死亡或者腺病毒被免疫;表达周期短,大约2周时间;注射方式多为原位定点,操作复杂 | 表达到高峰所需的时间长 |
在体感染小鼠海马组织对比:
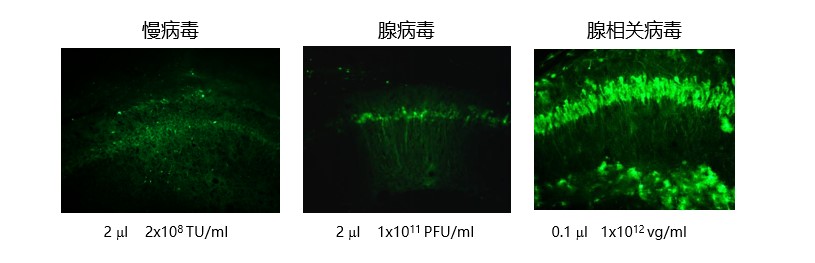
所以,AAV 是优秀安全的动物体内基因转染工具,并且 AAV 有多种血清型,每种血清型的靶器官亲和性各不相同,这一点决定了 AAV 与其他病毒载体相比,是更有器官选择性的载体,并且注射方式多样,详见下表:
| 注射部位 | 汉恒推荐 的血清型 |
注射方式 | 动物 | 注射体积( μl) | 备注 |
| 心脏 | AAV9,汉恒AAV-heart | 原位多点注射(局部) | 大鼠 | 10-15/点,5 个点 | 心肌主要有系统性给药、 原位给药和冠脉给药法,最常用的是前两种,冠脉法技术难度大,较少用。 **如需提高心肌特异性,您可配合使用心肌特异性启动子。汉恒生物AAV-heart是对AAV9进行了升级改造,只需尾静脉注射即可,特异高效。 |
| 小鼠 | 10-15/点,3-5 个点 | ||||
| 尾静脉注射(系统性) | 大鼠 | 250(200g 体重) | |||
| 小鼠 | 100 | ||||
| 肝脏 | AAV8 | 尾静脉注射 | 大鼠 | 200(200g 体重) | 大多数病毒都有嗜肝性,因此肝脏也是所有脏器中最好感染的。肝脏也可以用门静脉注射,感染效果更好。 但门静脉注射需行动物手术,技术复杂且易造成创伤。 **如需提高肝脏特异性,您可配合使用汉恒筛选的肝脏特异性启动子。 |
| AAV9 | 小鼠 | 100 | |||
| 全脑 | AAV-BBB | 尾静脉注射 | 大鼠 | 250-300 | 特殊血清型,可跨血脑屏障,感染全脑。 但经过汉恒验证,目前该血清型只适合大小鼠,在猴子上不成功。 **如需提高神经细胞特异性,您可配合使用汉恒筛选的神经特异性启动。汉恒AAV-BBB2.0升级版,效率更高,尾静脉注射轻松感染全脑。 |
| 小鼠 | 100 | ||||
| 大脑(局部) | AAV9,AAV2,AAV5 | 立体定位注射 | 大鼠 | 1-5 | 经汉恒验证,AAV9型感染扩散范围广, AAV2次之,AAV5扩散范围最小最集中 **如需提高神经细胞特异性,您可配合使用汉恒筛选的神经特异性启动子,如pSyn,pCamKII,pGFAP等。 |
| 小鼠 | 0.2-2 | ||||
| 脊髓 | AAV5,AAV1,AAV9 | 鞘内注射 | 大鼠 | 5-10 | 针头要足够细,找准椎骨之间空隙入针,避免损伤神经。 注射一定要缓慢,且控制好注射体积。 |
| 小鼠 | |||||
| 脂肪 | 汉恒脂肪特异性血清型 | 腹内脂肪-腹腔注射 | 大鼠 | 300 | 汉恒实验室自验证的脂肪特异性血清型 |
| 小鼠 | 150-200 | ||||
| 皮下脂肪-原位注射 | 大鼠 | 10-15/点,5-8个点 | |||
| 小鼠 | 10-15/点,5-8个点 | ||||
| 骨骼肌 | AAV9 | 原位多点注射 | 大鼠 | 10-15/点,3-5个点 | 下针缓慢,注意深度, |
| 小鼠 | 10-15/点,3-5个点 | ||||
| 眼睛 | 汉恒AAV视网膜专用型 | 玻璃体腔注射 | 大鼠 | 3~5 | 汉恒实验室自验证的视网膜特异性血清型 |
| 小鼠 | 1-2 | ||||
| AAV-DJ | 视网膜下腔注射 | 大鼠 | 3~5 | ||
| 小鼠 | 1-2 | ||||
| 肺脏 | 汉恒肺脏特异血清型 | 无创气管注射 | 大鼠 | 100-200(200g体重) | 需呼吸机。汉恒也测试过滴鼻法,效果不如气管注射。 |
| 小鼠 | 50-75 | ||||
| 肾脏 | AAV2或AAV9 | 肾脏肾盂原位注射 | 小鼠 | 100 | 较为复杂,方法详见汉恒公众号实验视频 |
| 肠道 | AAV1或AAV5 | 灌肠 | 大鼠 | 1000(200g 体重) | 动物需要提前饥饿,排空肠道。病毒用量非常大。 |
| 小鼠 | 500 | ||||
| 血管 (内皮为主) |
AAV1或AAV5 | 腹主动脉局部感染 | 大鼠 | 50 | 局部感染30分钟,感染时需要clamped肾主动脉 |

汉恒生物多脏器 AAV 注射及基因转染策略

