上海华雅思创生物科技有限公司
1 年
手机商铺
- NaN
- 0.2999999999999998
- 1.2999999999999998
- 0.2999999999999998
- 3.3
推荐产品
技术资料/正文
ProteanFect®助力AI“酿”出新药方:单轮筛选,高效进化靶向RNA
56 人阅读发布时间:2026-03-16 15:36
01 革命性突破:
GRAPE-LM实现RNA适配体的单轮定向进化
在生物医学领域,RNA适配体(Aptamer)因其高特异性结合能力被视为“分子钥匙”,但传统筛选方法依赖耗时耗力的多轮SELEX(指数富集配体系统进化),限制了其在药物研发和疾病诊断中的应用。近日,中国科学院深圳先进院、深圳大学、天津大学等单位的研究团队合作在《Nature Biotechnology》发表重磅研究成果,开发出全新的生成式AI框架GRAPE-LM,实现RNA适配体的单轮定向进化。该框架整合了核酸语言模型和条件自编码器,利用单轮CRISPR-Cas介导的细胞内筛选数据,就能生成结合活性远超传统多轮人工筛选的RNA适配体,为RNA靶向药物、生物传感器的开发带来革命性突破。
研究团队针对人类T细胞受体CD3ε、SARS-CoV-2刺突蛋白RBD、人类致癌转录因子c-Myc三个完全不同的靶点验证了GRAPE-LM的有效性。


RNA适配体是通过与特定靶标结合而定义的RNA分子,为研究RNA的结合功能提供了理想模型。传统适配体筛选主要依赖指数富集的配体系统进化技术,这一过程高度手动且劳动密集型。
更为关键的是,传统筛选在溶液中进行,缺乏生物相关性。这些挑战凸显了开发能够在细胞环境中筛选具有功能和效力的适配体进化方法的迫切需求。
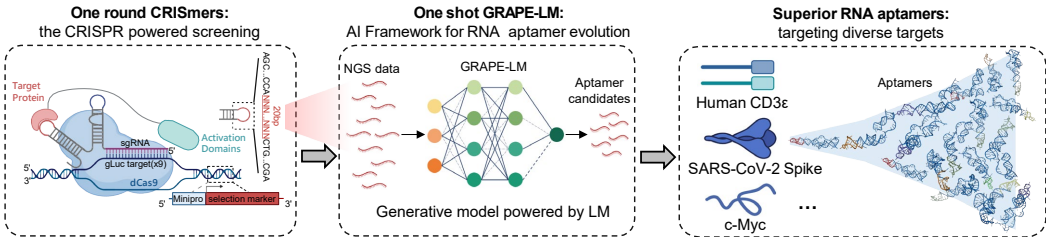
GRAPE-LM是一个生成式人工智能框架,集成了基于Transformer的条件自编码器与核酸语言模型,并利用基于CRISPR-Cas的细胞内适配体筛选数据作为指导。
该框架包含三个核心组件:基于语言模型的编码器,将RNA序列嵌入连续潜在语义空间;活性指导模块,约束潜在空间并根据伪活性水平组织RNA序列;基于Transformer的解码器,通过从潜在空间的高活性区域采样生成新型RNA适配体候选物(图2)。
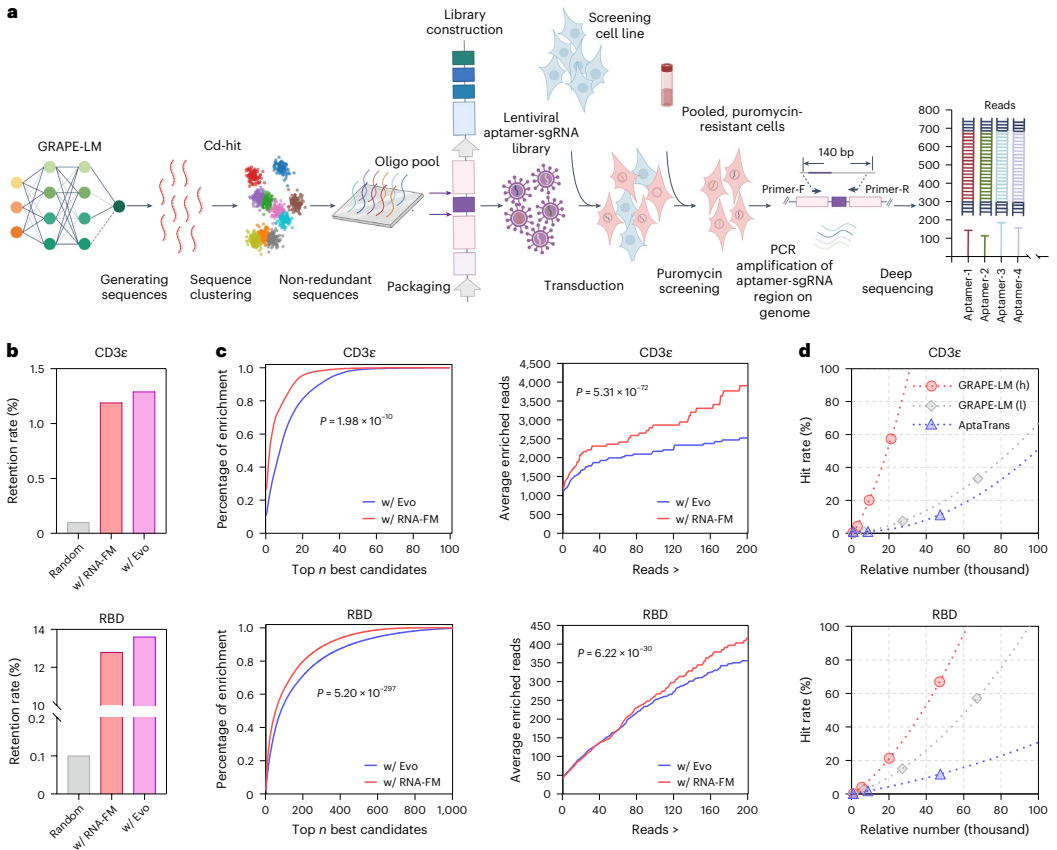
与传统的VAE、扩散或反向折叠框架不同,GRAPE-LM采用条件自编码器这一更直接有效的深度学习框架。研究团队通过对比实验证明,CAE在生成多样性方面优于VAE和掩码语言建模框架。
尽管扩散框架能有效生成多样化序列,但固有的去噪训练方案阻碍了活性指导模块的整合,这在Pearson相关系数表现不佳上得到体现。
研究团队在三个不同靶标上验证了GRAPE-LM的性能:人类T细胞受体CD3ε、SARS-CoV-2刺突蛋白受体结合域和人类致癌转录因子c-Myc。
令人瞩目的是,仅使用单轮CRISmers筛查信息的单次迭代,GRAPE-LM成功获得了比传统多轮人工筛选和优化方法产生的RNA适配体结合活性更高的RNA适配体。
在CD3ε靶向实验中,GRAPE-LM生成的适配体表现出高亲和力和特异性。顶级候选物CD3ε post-AI-34的解离常数达到53±12 nM(图3),优于预AI先导化合物以及之前报道的多轮SELEX衍生的CD3ε适配体。
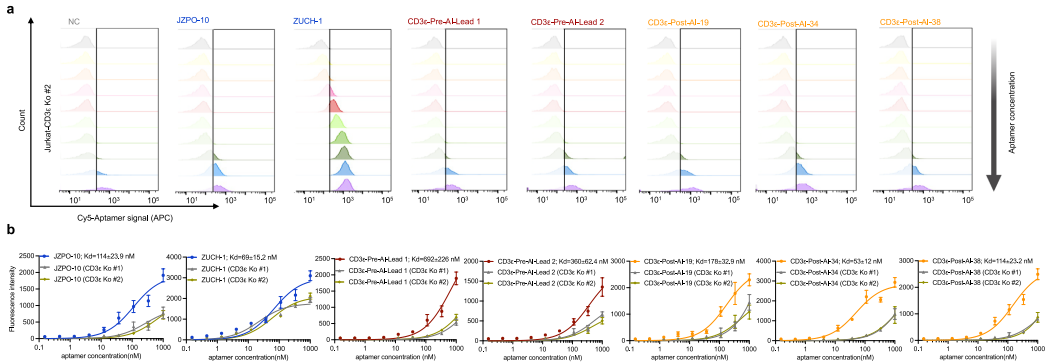
GRAPE-LM的成功关键在于其与高保真实验筛选系统的整合。CRISPR-Cas工具在此作为高保真数据生成器,能够捕获传统体外方法无法复制的细胞内生物过程。
尽管CRISmers的库容量受到实际限制,但GRAPE-LM通过从有限的起始库进行推断,探索更广泛的序列空间,从而弥补了这一不足。
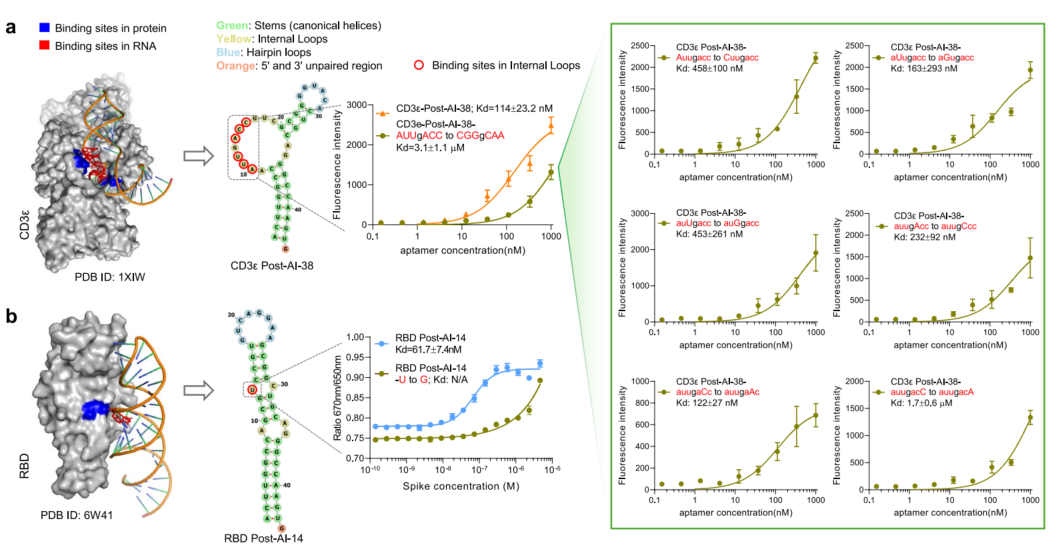
这项研究开发的CRISmers+GRAPE-LM管道包含两个进化阶段:细胞内的物理进化,随后通过语言模型进行数字优化。这种分叉方法从根本上不同于传统SELEX,为高效创建功能性适配体铺平了道路,消除了对人类努力进行劳动密集型和耗时轮次选择的需求。
GRAPE-LM的成功标志着人工智能在生物分子设计领域迈出了重要一步,为RNA治疗药物的开发和合成生物学应用开辟了新机遇。随着数据可用性和建模技术的不断进步,这一技术有望在更多领域发挥重要作用。
这项研究不仅展示了人工智能在生物技术领域的巨大潜力,更为未来生物医学研究提供了全新的技术路线和发展方向。