大家都在搜
| PD-1/PD-L1 肿瘤免疫治疗是近些年较为热门的研究领域,其中的免疫检查点 PD-1/PD-L1 更是备受关注,成为各大厂家研究的热门靶点。 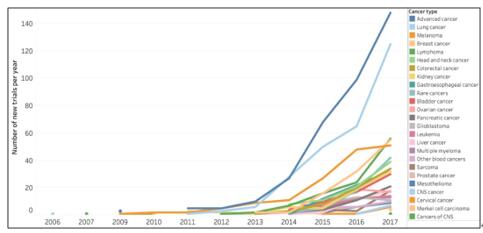
图 1. 2006-2017 年间 PD-1/PD-L1 疗法临床试验数量的变化趋势[1]
细胞程序性死亡蛋白-1(PD-1) 主要在活化的 T 细胞和 B 细胞中表达,PD-1 与细胞程序性死亡配体-1(PD-L1)结合介导免疫抑制信号,具有抑制 T 淋巴细胞活性、下调免疫应答的作用。由于 T 细胞或 B 细胞的过度激活会引发自身免疫病,故 PD-1/PD-L1 是免疫系统中的一种自稳机制。然而,肿瘤微环境会诱导浸润性 T 细胞中 PD-1 的表达水平增高,过度表达的 PD-1 与 PD-L1 的结合能够抑制T细胞的增殖与活化,使 T 细胞处于失活状态,最终导致免疫逃逸。免疫组化等方法已证实 PD-L1 在肺癌、肝癌与胃癌等多种实体肿瘤中均高度表达。PD-1/PD-L1 抑制剂均可阻断 PD-1 与 PD-L1 的结合,恢复 T 细胞对肿瘤细胞的识别与杀伤功能,通过人体自身的免疫功能实现抗肿瘤的目的[2]。 如何筛选适合使用 PD-1/PD-L1 抑制剂的患者? PD-1/PD-L1 抑制剂为治疗部分难治性肿瘤带来了新的方案,但 PD-1/PD-L1 抑制剂在患者中的总缓解率只有 20% 左右,这限制了其在临床实践中的应用[3]。如何筛选适合使用 PD-1/PD-L1 抑制剂的患者是 PD-1/PD-L1 抑制剂在临床应用中最主要的问题。目前,PD-1/PD-L1 抑制剂的预测指标主要有:PD-L1 的表达水平、微卫星不稳定(MSI)、肿瘤基因突变负荷(TMB)以及肿瘤浸润淋巴细胞(TIL)。 患者肿瘤组织中 PD-L1 的表达水平是应用最广泛的预测指标,PD-L1 的高表达与 PD-1/PD-L1 抑制剂治疗的应答率及患者的临床获益正相关[4]。例如,当非小细胞肺癌组织中 PD-L1 的表达率超过 50% 时,PD-1 抑制剂可以作为治疗方法。免疫组化技术(IHC)是最常用于 PD-L1 表达水平检测的方法。微卫星不稳定性(MSI)[6]、肿瘤突变负荷(TMB)[1] [7]、肿瘤浸润淋巴细胞 [8]和部分基因的突变等[9-10]也被文献报道影响 PD-1/PD-L1 抑制剂的有效率。 活动内容: 购买下列芯超组织芯片、免费随产品赠送 PD-L1IHC 数据  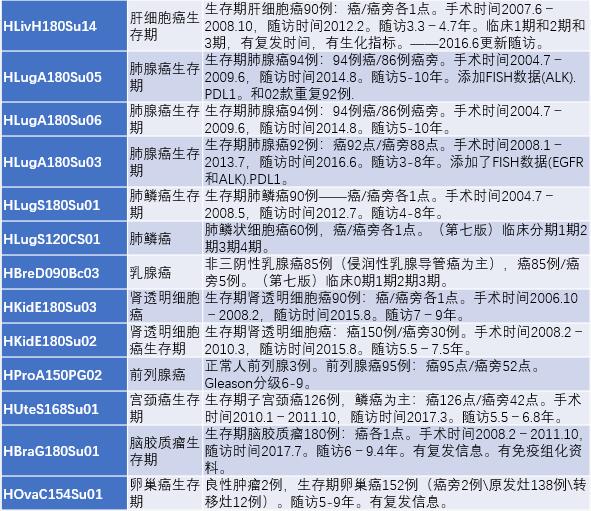
海量临床研究数据指标已上传至官网(http://www.superchip.com.cn/biology/tissue.html),随时等你来发掘! 参考文献: [1] Trial watch: The clinical trial landscape for PD1/PDL1 immune checkpoint inhibitors. [2] Alsaab H O , Samaresh S , Rami A , et al. PD-1 and PD-L1 Checkpoint Signaling Inhibition for Cancer Immunotherapy: Mechanism, Combinations, and Clinical Outcome[J]. Frontiers in Pharmacology, 2017, 8:561-. [3] Ming Y , Dechao J , Hanxiao X , et al. Biomarkers for predicting efficacy of PD-1/PD-L1 inhibitors[J]. Molecular Cancer, 2018, 17(1):129. [4] Ding W , Laplant B R , Call T G , et al. Pembrolizumab in patients with CLL and Richter transformation or with relapsed CLL[J]. Blood, 2017, 129(26):3419-3427. [5] Zeinalian M , Hashemzadehchaleshtori M , Salehi R , et al. Clinical Aspects of Microsatellite Instability Testing in Colorectal Cancer.[J]. Advanced Biomedical Research, 2018, 7(1):28. [6] Jin Z , Yoon H H . The promise of PD-1 inhibitors in gastro-esophageal cancers: microsatellite instability vs. PD-L1[J]. Journal of gastrointestinal oncology, 2016, 7(5):771-788. [7] Yarchoan M , Hopkins A , Jaffee E M . Tumor Mutational Burden and Response Rate to PD-1 Inhibition[J]. New England Journal of Medicine, 2017, 377(25):2500-2501. [8] Tomioka N , Azuma M , Ikarashi M , et al. The therapeutic candidate for immune checkpoint inhibitors elucidated by the status of tumor-infiltrating lymphocytes (TILs) and programmed death ligand 1 (PD-L1) expression in triple negative breast cancer (TNBC)[J]. Breast Cancer, 2017:1-9. [9] Mehnert, J.M., Panda, A., Zhong, H., Hirshfield, K., Damare, S., Lane, K., Sokol, L., Stein, [10] George, S., Miao, D., Demetri, G.D., Adeegbe, D., Rodig, S.J., Shukla, S., Lipschitz, M., Amin-Mansour, A., Raut, C.P., Carter, S.L., et al. (2017). Loss of PTEN Is Associated with Resistance to Anti-PD-1 Checkpoint Blockade Therapy in Metastatic Uterine Leiomyosarcoma. Immunity 46, 197-204. |