大家都在搜
| CRISPR基因编辑技术可以精确靶向目的基因进行敲除、敲入和点突变。目前科学家们通过CRISPR基因编辑技术来调节基因表达和纠正基因突变尝试治疗癌症,比如正在进展的1期临床试验表明经过CRISPR基因编辑的通用CAR-T细胞可用于治疗复发性B细胞白血病。除了在诊断治疗领域备受瞩目外,利用CRISPR基因编辑技术在基础研究的进展也层出不穷,近期凋亡机制的研究利用CRISPR技术就取得了一些新进展。 CRISPR KO助力SARS-CoV-2机制研究 新冠肺炎导致的死亡主要是由于SARS-CoV-2引发的肺细胞凋亡引起的肺泡毛细血管屏障破坏导致的肺水肿。然而,SARS-CoV-2促凋亡作用的分子机制尚不清楚。科学家们最近发现SARS-CoV-2病毒的膜(M)蛋白可以诱导肺上皮细胞线粒体凋亡。M蛋白能通过抑制BOK蛋白的泛素化及促进其转位到线粒体上来提高BOK的稳定性。M蛋白上具有与BOK相关作用必需的结构域。 通过CRISPR/Cas9基因编辑系统来敲除BOK基因后,科学家发现细胞抵抗M蛋白介导凋亡的能力增强。并且在不存在BAX和BAK的情况下,M蛋白就能够诱导BOK触发细胞凋亡。而BOK的BH2结构域是与M蛋白相互作用和促凋亡所必需的。体内实验表明,慢病毒介导M蛋白感染小鼠肺部,能诱导caspase相关的细胞凋亡并增加肺泡毛细血管通透性。CRISPR/Cas9敲除BOK基因能改善M蛋白慢病毒感染引起的肺水肿。因此小鼠体内实验表明,M蛋白通过激活BOK依赖的凋亡通路从而加剧了SARS-CoV-2 相关的肺损伤。这些发现揭示了M蛋白在SARS-CoV-2发病机制中的促凋亡作用,可能为新冠肺炎的治疗提供潜在的新靶点。 CRISPR助力肿瘤耐药基因筛选研究 免疫系统中的T细胞具有强大的清除肿瘤细胞的能力,利用T细胞的肿瘤免疫疗法在临床上也取得了显著的成功。然而肿瘤细胞对免疫疗法的抵抗是一个主要挑战,目前比较清楚的可以确定包括CD274(PD-L1)在内的一些基因,能够使肿瘤细胞逃避免疫系统。因此以PD-L1抑制剂一直是当前临床开发的重点。除了PD-L1,寻找其他免疫检测点抑制相关基因也是目前热门的研究。由于CRISPR文库筛选技术既可以用于Loss-of-Function (如CRISPR KO,CRISPRi),又可以用于Gain-of-Function(如CRISPRa)的筛选研究,因此被科学家们广泛应用于对未知靶点的筛选。 之前的研究使用了CRISPR KO文库在基因组层面进行大规模筛选,并鉴定出在抗原呈递,干扰素-γ(IFN-γ),肿瘤坏死因子(TNF)和自噬通路中,介导了肿瘤细胞对T细胞杀伤产生抗性的相关基因。近期的研究,科学家们又利用CRISPR技术在人黑色素瘤细胞中进行了基因组规模的CRISPR激活(CRISPRa)筛选,通过这种Gain-of-Function的CRISPRa文库筛选出4个候选基因(CD274(PD-L1)、MCL1、JUNB和B3GNT2),这些基因在上调后使人黑色素瘤细胞能够逃避T细胞杀伤。同时科学家发现MCL1和JUNB是通过调节线粒体凋亡途径来促进肿瘤细胞的免疫逃逸。其中JUNB编码的转录因子能够下调凋亡通路的FasL和TRAIL受体,上调MCL1相关的BCL2A1基因,并激活凋亡相关NF-κB通路。而B3GNT2编码的一种聚-N-乙酰氨基乳糖合酶,可以作用于多个配体和受体,以破坏肿瘤和T细胞之间的相互作用,减少T细胞活化。该研究结果不仅寻找到线粒体凋亡通路中对肿瘤逃逸免疫杀伤的相关基因,也显示了使用CRISPRa筛选和阐明耐药途径和确定治疗靶点的强大作用。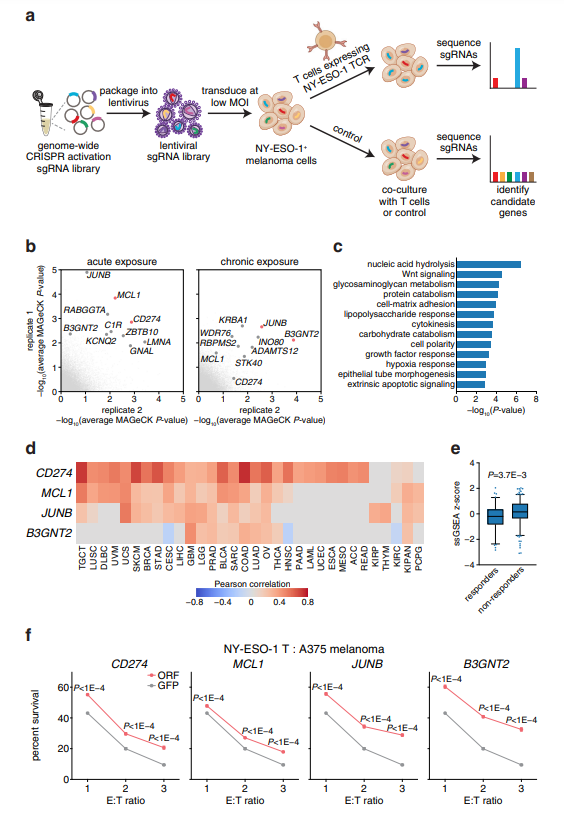
Scilia通过自主研发的高通量自动化平台,结合CRISPR技术敲除热门基因,本次推出上百种凋亡基因敲除的Hela细胞株,即定即发,为您的科学研究省时省力! Scilia 基因敲除细胞株&gRNA质粒 限时促销中! 活动时间:2023.3.14~4.14
|