
腺相关病毒AAV于20世纪中期在实验室中发现,随后科学家对其开展了广泛的研究和调查,由此AAV的生物学特性被渐渐揭晓。AAV属于微小病毒,无包膜,由单链DNA和蛋白衣壳组成,无法自主复制,且极少整合到宿主基因组上,对人没有致病性,通过改造野生型AAV后获得的重组腺相关病毒(rAAV)因其免疫原性低、靶向性强、多种血清型、感染宿主范围广、体内基因表达时间长等特点被视为重要的基因治疗工具。 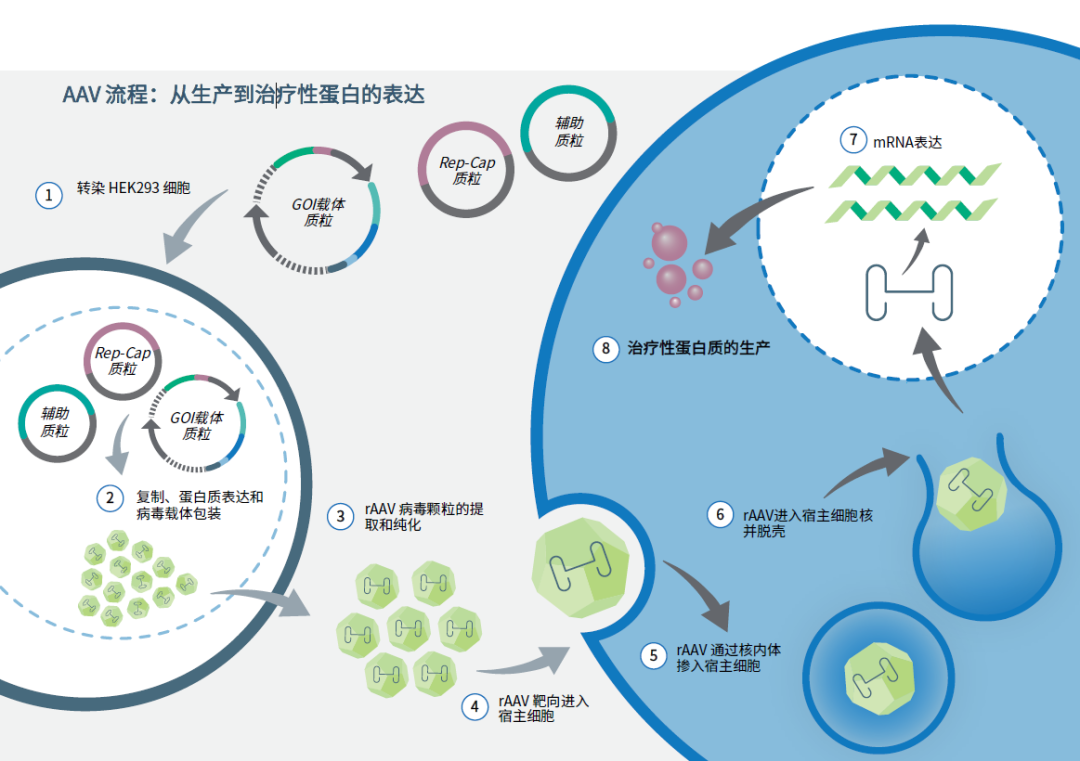
从发现到商业化,BalanCD HEK293 Viral Feed 简化了培养基制备并促进了无缝的工艺流程,帮助生物工艺组更快地实现目标。BalanCD HEK293 Viral Feed 可与从小规模到大规模的 HEK293 悬浮培养物一起用于多种血清型的 AAV 生产,以及多种基础生长培养基和转染方法。
• 化学成分限定的BalanCD HEK293Viral Feed, 经过优化以提高病毒载体的产量 • 在转染后补充至HEK293 悬浮培养体系中并支持高细胞密度 • 实现基因治疗应用病毒载体生产目标的完整解决方案 • 针对与 BalanCD HEK293 化学成分限定的培养基一起使用进行了优化,并与其他基础生长培养基兼容
满足您的高质量生产需求BalanCD HEK293 Viral Feed 在 cGMP 设施中生产使用来自可靠供应链的合格原材料,以确保 HEK293 特定应用的供应连续性和批次间可靠性。我们进行了严格的监督、分析和确认,使得BalanCD HEK293 Viral Feed符合全球和各个区域标准,同时满足每个制造批次文件的监管要求。 • 严格的原材料控制和采购计划 • 符合cGMP生产 • COA、COO、TSE/BSE 声明 • ISO13485, EN 13485:2016 认证 • 支持药物主文件 (DMF)* *根据要求提供 病毒滴度成倍增加BalanCD HEK293 Viral Feed 可提高 VG/capsid产量,并使滴度成倍增加,从而帮助制造商为其应用获得更多产出。 细胞生长:活细胞密度 (VCD) 和活率保持一致
图1. HEK293 悬浮细胞(细胞系 1)接种在 BalanCD HEK293 培养基(30 mL)中,24 小时后使用 PEIpro 方法以 1.8-1.9 X106 的细胞密度转染 1.5 μg DNA/mL(DNA 与 PEI 的比率为 1 :2). BalanCD HEK293 Viral Feed在转染后 24 小时以 12% v/v 添加。在收获时绘制活细胞密度 (A) 和活力 (B)。数据表明补料培养基对细胞生长和活率没有不利影响。
补料后 AAV2 滴度提高
图2. AAV2 病毒基因组滴度和衣壳滴度使用经过三个冻融循环的细胞提取物测量,然后在 qPCR 之前通过离心澄清和用 DNAse I 和裂解缓冲液处理(使用 AAVpro 滴定试剂盒,Takara Bio)和 ELISA(AAV2 滴定ELISA,Progen)。蓝色条表示病毒基因组 (VG) 和衣壳滴度在没有补料的情况下超过基础对照组。数据表明添加补料培养基使 AAV2 产量在 VG 方面提高了大约 10 倍,在衣壳滴度方面提高了 6 倍。整体结果,确定病毒包装提高了约 67%,从基础的 13% 提高到基础+补料的 21.81%(数据未显示)。
|