大家都在搜
 单纯疱疹病毒(Herpes simplex virus , HSV)是一种是人类常见的病原体,且人是其自然宿主。从结构上看,HSV 病毒呈球型,为多层同心结构。从外到内,完整的 HSV 颗粒由包膜蛋白、病毒包膜、被膜、衣壳以及 dsDNA 基因组构成。HSV 有两个血清型:HSV-1 和 HSV-2。其中 HSV-1 主要感染人的口唇、鼻部等黏膜部位,HSV-2 则感染主要引起生殖器疱疹及生殖器炎症。 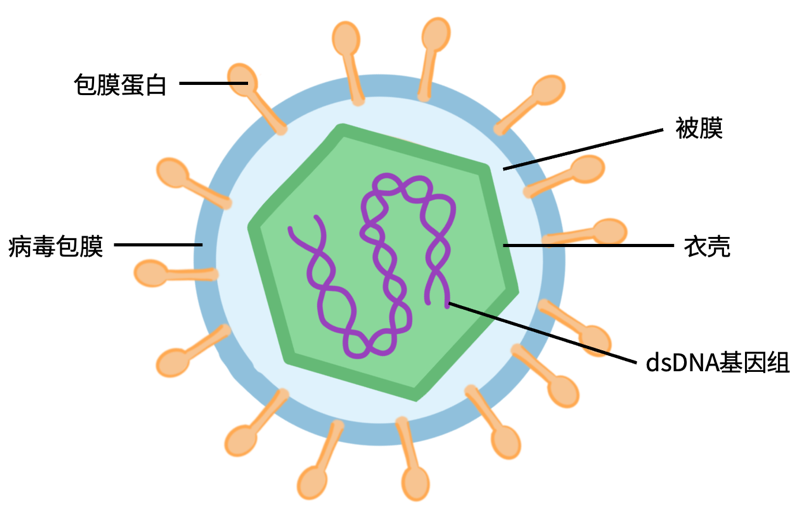
HSV 的基本结构
HSV 具有天然的神经嗜性,通常以上皮细胞作为首要的感染位点。HSV 在上皮细胞中进行复制后其生产的子代病毒颗粒可以进一步感染感觉神经元,然后沿轴突传递进入神经元细胞体。HSV 可以在神经元中长期潜伏,但是在一定条件下则被重新激活,然后从轴突回到上皮细胞触发再次感染。 虽然野生型 HSV 与疾病相关,但是当前利用重组 HSV 进行基因递送是基因治疗应用的前沿领域。重组 HSV 在神经系统基因递送、溶瘤基因转导和疫苗开发方面有着广泛的应用。重组HSV具备相当多的优点,如嗜神经嗜性、长潜伏期、病毒基因组以游离体形式存在于整个宿主细胞生命周期以及极大的载体容量,因此基因治疗研究中体内和体外基因转导实验的理想病毒载体。 HSV 作为溶瘤病毒 HSV-1 在溶瘤病毒疗法应用方面,由于以下几个因素而具有相当的潜力。首先 HSV-1 具有很强感染性,在 10 小时内即可完成其整个复制周期并释放数千个子代病毒颗粒,这比腺病毒等其它的常见病毒所需的时间要短得多。除了细胞外扩散外,HSV-1 病毒颗粒还可以通过细胞连接的方式从一个细胞传导到另一个细胞,这有利于病毒在实体瘤内高效传播。此外,HSV-1 已被证明可有效感染多种实验动物,因此非常适合体内临床前研究。经过专门设计的减毒HSV溶瘤病毒可以选择性地在肿瘤细胞中复制并将其杀死,但是不能在正常细胞中生长。这样的HSV可以通过删除正常细胞中病毒复制所必需但对肿瘤细胞不是必需的基因来产生。此外,这种HSV的肿瘤杀伤效果还可以通过携带抗癌基因或者激活化疗试剂的基因来进一步增强。 2015 年,FDA 批准了 HSV-1 溶瘤病毒药物 Talimogene Laherparepvec(TVEC),目前用于治疗黑色素瘤。TVEC 删除了病毒基因 ICP34.5 和 ICP47,使其在正常细胞中无法复制但是可以激活免疫系统。TVEC 的溶瘤潜力还因为其过表达人粒细胞巨噬细胞刺激因子 (GM-CSF)而得到额外增强。GM-CSF基因通过增强树突状细胞的迁移和成熟来进一步激活免疫系统。 除了减毒病毒载体,复制缺陷型的 HSV 也可以用于治疗多种癌症。该方法主要原理是利用复制缺陷型 HSV 来驱动细胞自杀基因(例如胸苷激酶(TK))或者其它治疗潜力的基因(例如 TNF-α)在肿瘤细胞内表达从而达到抑制肿瘤生长的目的。 HSV 作为疫苗 HSV 在用于抗病毒和抗细菌疫苗研制方面拥有以下几个优势:1、可以通过多种途径给药以激活宿主免疫系统; 2、病毒基因组在宿主细胞中保持游离体形式,不整合宿主基因组; 3、HSV 基因组中表达 TK 基因可以将无细胞毒性的药物,比如 Ganciclovir,可以被转变成有细胞毒性的代谢物以杀死被病毒感染的细胞,同时不造成副作用。 实际上,无论是使用 HSV-BAC、扩增子载体、复制缺陷型 HSV 还是减毒 HSV,在应用于抗击多种病原体的疫苗时均具有良好的表现。 减毒 HSV 特别适用于开发抗 HSV 疫苗,这是因为它们为宿主的免疫系统提供了接触多种类型的病毒抗原的机会,从而可以激活细胞免疫和体液免疫。 此外,与非活性疫苗或者仅表达病毒特定亚基的疫苗载体相比,减毒活疫苗可以提供更长期的有效保护。 此外,HSV 疫苗的开发是有一定紧迫性的,这是因为全世界人口中有很大一部分有感染过 HSV-1 或 HSV-2,但是目前尚未有 FDA 批准的疫苗可用于治疗这两种病毒。VC2 是一种在开发时对病毒糖蛋白 gk 和膜蛋白 UL20 进行了部分删除的减毒活 HSV-1 病毒,当前已经在 HSV-1 和 HSV-2 感染的动物模型中测试并表现出良好的应用潜力。 包含删除突变的复制缺陷型 HSV(删除了病毒复制所必需的以及表达特异性外来抗原的基因)在作为疫苗注射各种病毒或细菌感染的动物模型中,表现出持久诱导激活免疫反应的特点。 此外,在使用小鼠模型的一些临床前研究中,扩增子载体作为治疗性疫苗已广泛用于治疗癌症、微生物感染以及神经疾病。当前,还需要在其他动物模型中评估 HSV 疫苗的免疫原性,包括那些已经存在HSV免疫的动物模型。 HSV 作为基因递送载体 HSV 扩增子载体是基于 HSV-1 设计的,但是只包含一个或多个目的基因以及最小病毒基因组序列。HSV 扩增子载体由于其天然的神经嗜性、极大的装载能力(可达150 kb)、低毒性以及在病毒基因组序列在靶细胞内以游离体存在的特点,特别适合作为针对神经元的进行基因递送。当前 HSV 扩增子载体广泛用于以下领域的研究:一、神经退行性疾病,例如阿尔茨海默症和帕金森疾病;二、神经精神异常,包括抑郁和上瘾;三、治疗方法中需要将治疗性基因导入神经系统的疾病,例如缺血性脑卒中。 此外,由于扩增子载体能够感染多种分裂细胞系,并且与传统质粒转染相比,HSV 扩增子载体更容易感染细胞,因此扩增子载体非常适合体外药理学研究。 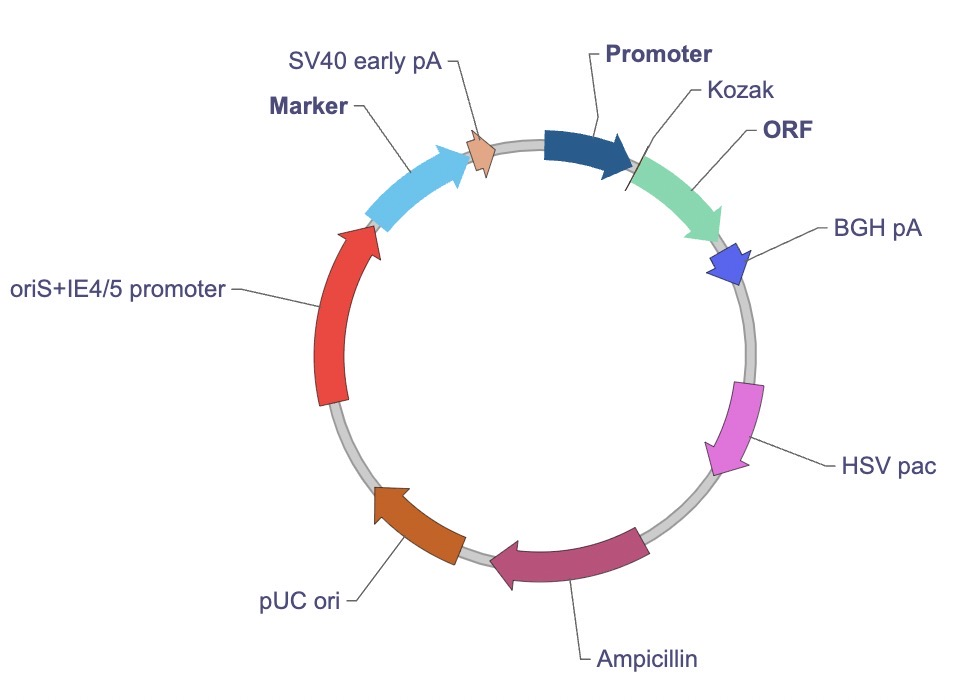
云舟生物 HSV-1 扩增子载体
通过删除病毒复制所必需的基因以显著降低细胞毒性,复制缺陷型的 HSV 也是一种基因递送载体被应用于基因治疗。这些 HSV 由于多个基因的缺失,其装载能力也到了提升,使得它们能够携带多个独立的基因表达盒,而这是对用于复合基因治疗的载体的典型要求。 因此,复制缺陷型 HSV 已广泛用于多种基因治疗研究,包括慢性疼痛、帕金森疾病、脊髓损伤以及溶酶体储存障碍等。NP2是一种表达人前脑啡肽(Preproenkephalin,PENK)的复制缺陷型 HSV,在治疗疼痛的一期临床试验中显示出良好的结果。
想要了解 HSV 病毒基因治疗应用的更多详情 可到此查看云舟生物 HSV 病毒载体制备服务↓ https://www.vectorbuilder.cn/service/herpes-simplex-virus-hsv-vectors.html 参考文献
|
