大家都在搜
| 传代培养中的细胞传代培养 (subculture),当原代培养成功以后,随着培养时间的延长和细胞不断分裂,一则细胞之间相互接触而发生接触性抑制,生长速度减慢甚至停止; 另一方面也会因营养物不足和代谢物积累而不利于生长或发生中毒。当培养的细胞增殖达到一定密度后,将会出现密度抑制现象,表现为细胞的生长和分裂速度逐渐减慢,甚至停止。此时如果不及时进行分装再培养,即传代培养,细胞将逐渐走向衰老、死亡。将培养的细胞从一个容器以 1∶2 或其他比率转移到其他容器中扩大培养,称为传代培养。贴附型生长细胞采用酶消化传代法,而悬浮型生长细胞则采用直接传代法或离心传代法。 实验步骤: 一、贴附型生长细胞的传代贴附型生长的细胞采用酶消化的方法进行传代。 具体步骤如下: 1. 细胞的清洗 取已长成或接近长成致密单层的 HeLa 或 T47D 细胞(或原代培养细胞)一瓶,倒去培养液,加入 2~3 mL Hanks 清洗液,轻轻振荡漂洗细胞后倾去清洗液,以去除残留的培养液和衰老脱落的细胞及其碎片。 2. 消化 加入适量(盖满细胞面即可)0.25% 胰蛋白酶溶液,室温下(或 37℃)消化 2~3 分钟后,倒置显微镜下观察细胞面,待培养细胞变成圆形时即可快速倒去消化液(如消化程度不够时可延长时间);再加 Hanks 清洗液轻轻清洗一遍后倾出或直接进行下一步操作。如在酶消化过程中,见细胞大片脱落,表明消化过度,此时为避免细胞大量丢失,不应倒去消化液,而要加入等量的培养液吹打,收集细胞,800r/min 离心 5 分钟后弃去上清液,再进入下一步。 3. 接种 在培养瓶中加入 3 mL 培养液(含 10% 血清)以终止消化。用吸管反复吹打瓶壁上的细胞层,直到全部细胞被冲下,轻轻吹打混匀,制成单细胞悬液。按 1∶2 或 1∶3 分配,接种到 2~3 个培养瓶内,再向各瓶补加培养液到 5 mL,也可以取细胞悬液计数,分别按需要的细胞浓度接种到一定数量其他的培养瓶中,再补足培养液进行培养。原代培养的细胞首次传代时,细胞接种数量要多一些,以使细胞尽快适应新环境,利于细胞生存和增殖,随消化分离后的组织块也可一并传入新的培养瓶(图 5-2)。 4. 观察 细胞传代后,每天应对培养细胞进行观察,注意有无污染、培养液的颜色变化情况、细胞贴壁和生长情况等,若细胞贴壁存活则称为传代一次。 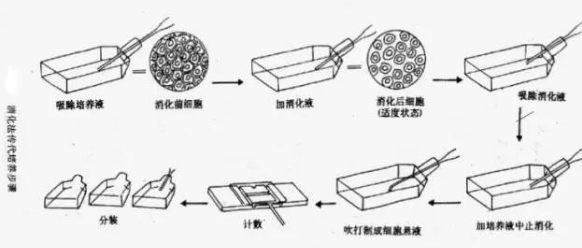
传代培养步骤
二、悬浮型生长细胞的传代因悬浮型生长细胞不贴壁,故传代时不必采用酶消化法,而可直接传代或离心收集细胞后传代。 1、直接传代 直接传代即让悬浮细胞慢慢沉淀在瓶底后,将上清液吸掉 1/2~2/3,然后用吸管吹打形成细胞悬液后再传代。 2、离心传代 (1)在超净台内用吸管将培养瓶中的细胞吹打均匀,尤其是将半贴壁的细胞吹打起来。 (2)将细胞悬液吸入离心管中,盖紧胶盖,与另一离心管配平后,置离心机中 800~1000r/min 离心 5 分钟。 (3)回到超净台操作,弃上清液,加入适量新培养液,用吸管吹打均匀,制成单细胞悬液。(4)按 1∶2 或 1∶3 分配传代培养,也可以计数后根据所需要的细胞浓度传至已准备好的新培养瓶或培养皿中,放入 CO2 培养箱中继续培养。 |