 荧光定量 PCR 实验结果不理想?重提了 RNA,再重头来一遍,结果还是一样? 很有可能您忽视了重要步骤,也可能是您还没有选对逆转录的试剂...看着很简单的逆转录,其实暗藏玄机。今天,莫纳丽莎为大家带来了逆转录实验的 tips,干货满满。快快加入我们,一起轻松实现高效的逆转录实验吧! 三代逆转录预混液 (MR05001) 
去基因组与逆转录一管化三代预混液 (MR05101) 
去基因组与逆转录两步进行的三代预混液(MR05201) 
|实验操作| ■ 1.试剂融化后稍离心,使用前放置冰(盒)上。 ■ 2.1 基因组 DNA 污染去除: 
#1 干冰(盒)上配制如下反应体系: 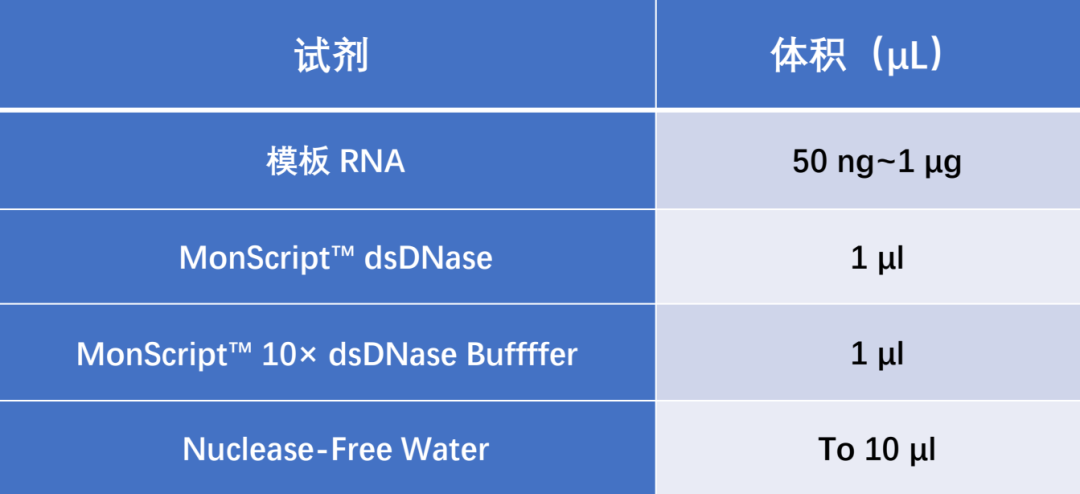
推荐使用试剂盒提取的高质量 RNA 作为模板。 #2 轻柔吸打混匀,瞬离; #4 可 55℃ 温育 5 min,以使 dsDNase 失活,冰(盒)上放置。 ■ 2.2 cDNA 第一条链合成: #1 干冰(盒)上配制如下反应体系: 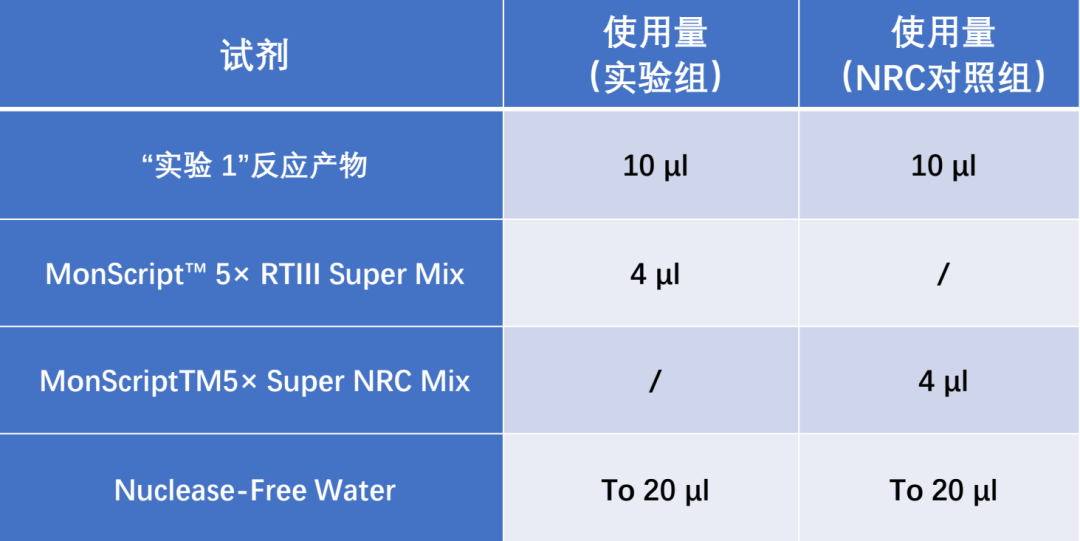
#2 轻柔吸打混匀,瞬离; |说明| ■ 使用该预混液,15min 可获得长达 12kb 的 cDNA,可以作为下游 qPCR 或者普通 PCR 扩增的模板,根据实验需要使用原液或者适当稀释后用于后续实验。 |注意事项| 逆转录相关的 RNA 操作需注意: ■ 要有专门划分出的 RNA 实验专区; |影响因素| 影响逆转录的关键因素: ■ 模板二级结构; |提高逆转录效率| 方法 1 
说明:更高逆转录反应温度-模板在 55℃ 充分打开。 MonScript™ 系列逆转录产品,为满足科研工作者对 cDNA 合成越来越高的需求,以 M-MLV 逆转录酶为基础,通过基因工程改造为更高反应温度 42℃-55℃,与市面上其他逆转录产品相比,拥有更高的逆转录反应温度,cDNA 产量更高,具有更完整的基因代表性。 方法 2 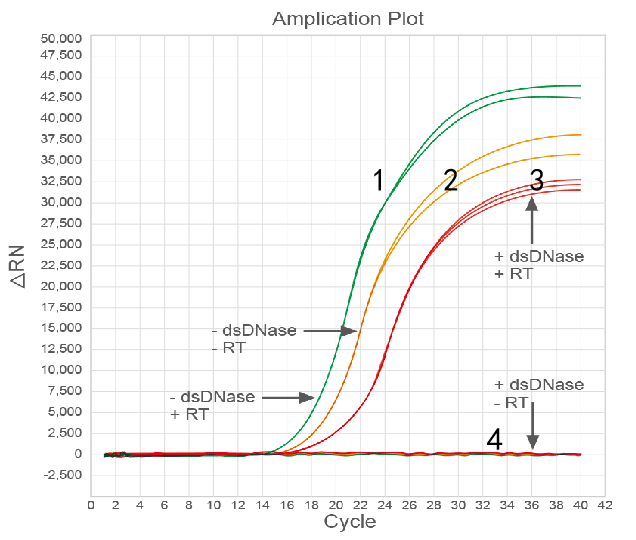
* 1. 不去基因组+逆转录 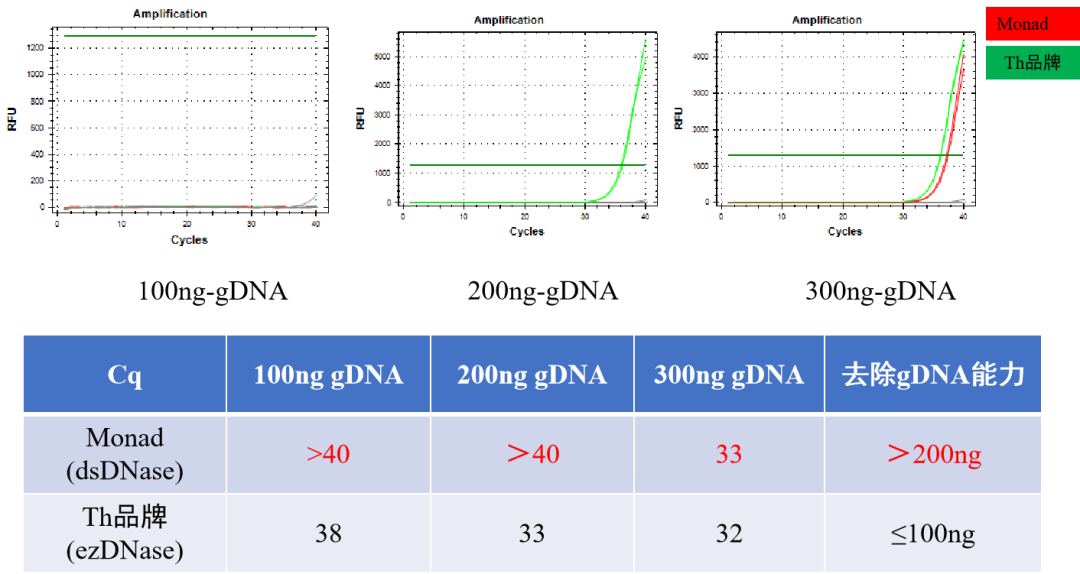
说明:彻底去除基因组污染,定量结果更准确。 莫纳预混液采用了高效的 dsDNase,该酶具有热敏感性,可在高温条件下快速不可逆地失活。与传统使用 DNase I 去除基因组 DNA 污染的方法相比,dsDNase 无需额外加入 EDTA 进行失活,不仅节省实验时间,而且降低了对逆转录反应的抑制。 方法 3 
说明:分别测试不同品牌的逆转录产品的酶动力学范围(绘制标准曲线)。 结果表明:Monad 逆转录产品整体表现稳定且酶动力学范围更广,即对于高浓度的 RNA 可以有效反转,对于低浓度的 RNA 也没有抑制作用。 方法 4   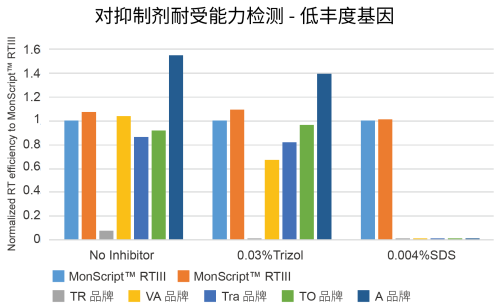
说明:提纯过程中的抑制剂存在对定量结果的影响。 莫纳逆转录产品在抑制剂存在的情况下,对植物样本高、中、低丰度基因扩增仍表现出较好的水平;与其他品牌相比,对抑制剂 SDS 有较好的耐受能力。 方法 5 
说明:全预混与半预混的产品形式,更少的加样步骤,更低的污染风险。 配制逆转录反应体系需要逆转录酶、dNTPs、DNase 等,以单组分形式会增加实验更多的操做和污染风险。预混液的形式,可以大大减少加样的操作,节省实验操作时间及降低污染风险,实现简单的操作体验。 |FAQ| 关于逆转录实验的常见问题与解答: Q1:用不同品牌反转录试剂盒反转录后,对 cDNA 进行浓度和纯度测定,发现所得到的 A260/A280 结果不同,不同厂家试剂盒反应的结果不同是什么原因? 以上就是今天关于逆转录实验的干货 Tips 啦!不知道有没有帮助到大家改进自己的实验呢? 你在逆转录实验中都遇到过哪些问题?又是如何解决的呢?欢迎莫粉儿们积极分享自己的经验,畅游科研世界,和莫纳一起探索无限!
1. Arhat/Tarzan 96 梯度 PCR 仪:温度准确、均一,专利技术防边缘蒸发,叠放省空间 |