细胞的死亡方式可谓是「花样百出」,但是究其根本,或死于「自杀」(程序性细胞死亡),或死于「他杀」(非程序性细胞死亡)。目前认为,程序性细胞死亡 (programmed cell death, PCD) 主要包括细胞凋亡和自噬。非程序性细胞死亡 (non-programmed cell death,NPCD),包括细胞坏死(necroptosis),副凋亡 (paraptosis)、细胞有丝分裂灾难 (mitotic catastrophe) 和细胞胀亡 (oncosis) 等 [1]。铁死亡是近年来发现的一种新型程序性细胞死亡方式,与中风,缺血再灌注,器官移植以及癌症等疾病息息相关。
图 1:铁死亡在多种系统性疾病中的作用[2]
铁死亡 2012年,Dixon等在大量研究的基础上提出了一种新的细胞死亡方式,并将这种铁依赖的死亡方式命名为铁死亡(ferroptosis)。研究表明小分子Erastin(CSN17148)可以诱导含有致癌基因RAS突变的肿瘤细胞死亡,但是没有典型的细胞凋亡特征。而且铁螯合剂能抑制Erastin诱导的肿瘤细胞死亡,表明铁离子在诱导该细胞死亡过程中发挥了重要作用 [1]。目前发现铁死亡与凋亡、坏死和自噬在形态学、生物化学和遗传学等方面均有差异。其典型的特征为线粒体变小,但双层膜的密度增加,同时表现为细胞质以及脂质活性氧自由基增多[1]。铁死亡的机制 铁死亡的影响因素有铁、脂质活性氧和谷胱甘肽过氧化物酶 4(glutathione peroxidase 4,GPX4)。诱导铁死亡发生的信号通路有所不同,其中上游通路是通过直接或间接影响这 3 种因素使其发生 [3]。大量学者研究发现,铁死亡是由脂质活性氧的过度积累导致的 [4],脂质活性氧的过量蓄积有赖于胞内铁离子的催化作用,当胞内铁含量增加时,脂质活性氧生成增加,若此时 GPX4 的合成减少,则会使脂质活性氧产生和清除的平衡被打破,进而导致细胞铁死亡。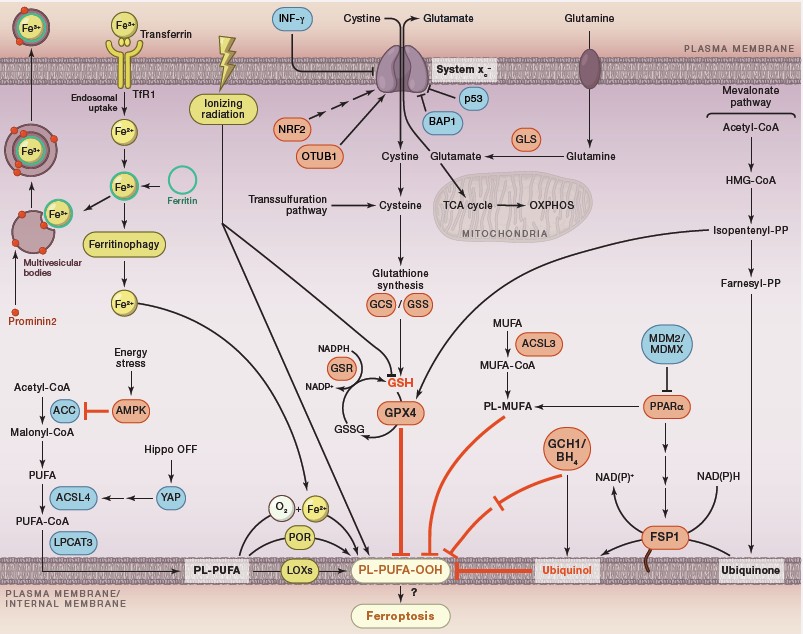
图 2:铁死亡的信号通路[5]
铁死亡诱导剂
铁离子的蓄积和脂质过氧化物生成增多是铁死亡的重要标志,铁死亡诱导剂均是通过破坏脂质活性氧产生和清除的平衡,使得脂质活性氧过量蓄积,从而引起细胞死亡。铁死亡诱导剂按作用靶点可分为 4 类(表 1):靶向胱氨酸/谷氨酸反向转运体 (System xc)、靶向 GPX4、靶向 GSH 以及靶向铁离子和 ROS 的诱导剂 [6]。代表化合物为:Erastin (CSN17148)、Sorafenib (CSN10381)、RSL3 (CSN17581)、Altretamine (CSN18706)、Artesunate (CSN13071)、Buthioninesulfoximine(CSN23750)、Sulfasalazine(CSN12011) 等。
表 1:铁死亡的诱导剂[7]

目前已有的铁死亡抑制剂(表 2)主要通过消除自由基、抑制产生脂质或脂质过氧化物的酶、减少游离铁等途径,维持脂质活性氧产生和清除的平衡,减少脂质活性氧蓄积从而发挥作用 [6]。如:Ferrostatins-1(CSN12654)、Deferoxamine (CSN13144)、alpha-tocopherol(CSN12210)、Trolox(CSN20793)、CoQ10(CSN12629)、idebenone(CSN11185)、deferiprone(CSN25406)、ciclopirox (CSN16738)、Butylated hydroxytoluene(CSN27512)、tetrahydrobiopterin(CSN23846)、zileuton(CSN12237) 和 Baicalein (CSN17375)等。
表 2:铁死亡的抑制剂[5]

目前已发现各种类型的铁死亡诱导剂和抑制剂,然而对其中大多数化合物的作用靶点和潜在应用仍有待深入了解。进一步阐明这些化合物(尤其是多作用靶点化合物)的作用机制、各机制间的关联和作用特点,同时探讨联合用药的可能性以及开发特异性更高的诱导剂或抑制剂,都将对铁死亡的临床应用产生深远影响 [6]。 CSNpharm 作为一家全球知名的小分子化合物供应商,拥有多种铁死亡相关的抑制剂和诱导剂,可用于相关疾病的探索。此外,还有 Ferroptosis Compound Library (CSN-L1031A),包含 260 多个活性化合物, 覆盖 GPx、Nrf2、HIF 等靶点, 可用于高通量以及高内涵筛选,是铁死亡机制研究的有利工具! 友情提示:CSNpharm 产品仅用于科学研究!
1. 关鹏等. 铁死亡: 一种新的细胞死亡方式 [J]. 生物化学与生物物理进展, 2013, 040(002):137-140. 2. Li J et al. Ferroptosis:past, present and future[J]. Cell Death & Disease, 2020, 11(2):88. 3. 刘宏伟, 邵莹莹, 陈倩, 等. 铁死亡调控机制及其在肝细胞癌中的研究进展 [J]. 中南药学, 2020, v.18. 4. Angeli J et al. Ferroptosis Inhibition: Mechanisms and Opportunities.[J]. Trends in Pharmacological Sciences, 2017, 38(5):489-498. 5. Hadian K,Stockwell BR. SnapShot: Ferroptosis. Cell. 2020 May 28;181(5):1188-1188.e1. 6. 孙晟杰, 涂画, 唐励静, 等. 铁死亡诱导剂和抑制剂的研究进展 [J]. 中国药理学与毒理学杂志 2020 年 34 卷 8 期, 623-633 页, ISTIC PKU CSCD CA, 2020. 7. Bebber CM, MüllerF, Prieto Clemente L, Weber J, von Karstedt S. Ferroptosis in Cancer CellBiology. Cancers (Basel). 2020 Jan 9;12(1):164. |