| 上一篇软文《必看!2020年科研中的18个高频问题》小编罗列了过表达转录本选择、基因下调注意事项、荧光素酶实验等常见问题。剩余的九个问题主要涉及细胞感染、动物实验两个方面,且看小编为你盘点。 细胞感染
慢病毒对细胞的感染效率受多个因素影响,如细胞自身生长的状态、细胞数量、细胞被慢病毒感染的难易程度等。因此保证细胞正常增殖,轮廓清晰,合适的细胞密度,选择最优的感染条件可以更好的保证感染效率。
对于一些较难转染的细胞,如原代细胞、干细胞、不分化的细胞等,可以通过添加病毒感染增强液来显著提高转染效率。
吉凯基因自主研发了HitransG A和HitransG P 两款感染增强液,可显著提升难感染细胞的感染效率。
这两款增强液的原理和适用范围详见下表: 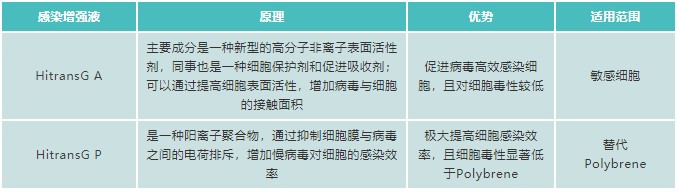
悬浮细胞除了难感染,还难培养。所以长期培养多种悬浮细胞的吉凯研发小伙伴为大家整理了细胞培养过程中的小技巧:
1.悬浮细胞换液时,对于状态好及细胞数较多的细胞,一般采取低速离心法沉淀并进行换液。对细胞状态差或是细胞数量少时,可将旧培养基轻轻吸取一半弃去再补加新鲜培养基,以减少对细胞的机械损伤。
2. 若是悬浮细胞数少及状态差时,可将细胞从原来的培养皿移至更小的培养板中进行培养,待状态好及细胞数增多时再移至大一点的孔板或皿中培养。
3. 对需要加细胞因子的细胞培养如:NK92细胞,不可将IL2加至配好的培养基中,应直接将IL2加至含培养液的培养皿中,轻轻晃匀,并记下培养液体积,以便后续再按比例补加细胞因子。
吉凯基因针对悬浮细胞,选取慢病毒、逆转录病毒做测试,并搭配自研的助感染试剂HiTransB-1、HiTransB-2,获得了一系列常用悬浮细胞的MOI供大家参考(由于不同实验室细胞代数、状态等因素,MOI 值存在一定差异,以下数据仅供参考):
HiTransB-2:在 HiTransB-1 基础上添加了一种阳离子聚合物,通过抑制细胞膜与病毒之间的电荷排斥,显著增加病毒对细胞的感染效率 。
//3. 加入慢病毒后,细胞死亡很厉害,该如何处理? 如果不幸遇到了细胞死亡的情况,调整并降低感染的MOI值,并且在感染后4小时、8 小时、12 小时对细胞进行观察;若发现细胞状态变差时,则需要立刻对细胞进行换液操作,使用新鲜的完全培养液替换病毒感染培养液。 动物注射 目前的动物实验多以腺相关病毒AAV为主,针对此类操作,我们的科研顾问王自山博士写了大量的软文并进行相关直播讲座,下面看看常见问题的节选: //4. 如何选择注射方法及剂量? 使用AAV时,在这里常犯的错误主要有两个:
1. 注射方法选择不合适,理论上尾静脉注射后AAV会进入血液循环而到达全身各处,因此不少人不管感染什么组织都选择尾静脉注射(操作简单嘛),然而实际上很多组织虽然通过尾静脉注射的方法可以感染,但是很难达到很好的感染效果,比如骨关节、鼻腔、瘤体组织、肺等;
2. 注射剂量选择不合适,许多人注射AAV时喜欢直接将文献中的注射方法和剂量拿过来用,这种方法看似稳妥实则埋雷无数,因为不同实验室操作手法、注射体积、动物背景等的差异,往往导致AAV注射剂量存在差异。比如同样是尾静脉注射AAV感染成年小鼠肝脏,相同的剂量用100μl体系注射的效果就明显不如200μl体系 。
针对以上常犯错误,我们总结了感染不同组织器官时推荐的注射方法以及注射剂量范围(如表3所示),建议大家以此为参考,在正式实验之前设置至少三组浓度梯度进行预实验,确定最适合的AAV注射剂量。
表3.小鼠不同组织器官AAV 注射方法及剂量 
腺相关病毒感染细胞是通过其衣壳蛋白与细胞表面的受体蛋白相结合进而经胞饮作用进入细胞体内,不同的血清型具有不同的衣壳蛋白空间结构,其识别的细胞表面受体也不同,因此不同血清型对细胞或组织的亲和力不同。所以一旦选择的血清型对目标细胞或组织亲和力较差,很难实现较好的感染效果。
为了帮助大家跨过这个雷区,吉凯基因技术团队通过分析大量使用AAV的高分文章案例并亲自对比验证,总结出了研究不同组织器官时血清型选择推荐表(表4),根据感染目标组织,血清型选择一目了然。
表4. 常见组织器官推荐血清型 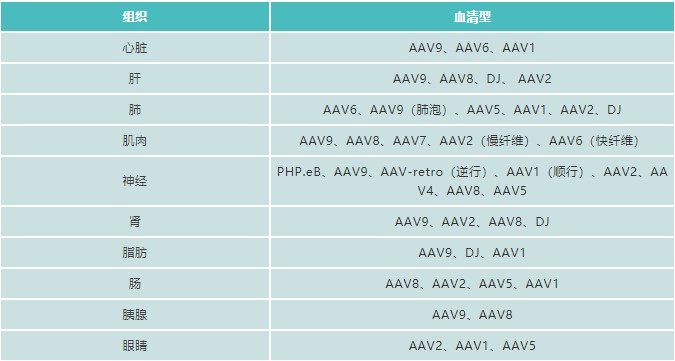
对于动物实验用何种病毒,首先要了解各类型病毒的特征: 
目前的动物实验多以腺相关病毒操作,其优势是:免疫原性低、滴度高(也就意味着能感染的细胞多)、非分裂细胞稳定表达等。当然,也有对应劣势:包装容量小、表达时间慢。腺病毒的特点是表达快,但不能长期表达,对于短时间的实验研究可以选择;慢病毒的特点是整合后稳定表达,但是其滴度较低,所以一般需要原位注射,注射动物的成本相对较高。实际操作可结合以上病毒特征选择对应的病毒工具。
//7. AAV的保存与分装 正确的保存AAV确保其质量是取得良好实验结果最基本的前提,看似简单的事情也曾让不少人付出惨痛代价。常见的如病毒放在4℃冰箱后忘记收到-80℃冰箱,或不管用量多少都整管取出导致反复冻融,再有分装时未在无菌条件下操作导致病毒污染,还有分装体积过小致使病毒损失严重等等。
因此,在使用AAV时应注意以下几点:
1. 收到病毒后立即置于-80℃保存,勿放于4℃,如需分装,则分装后的病毒也要放在-80℃;
2. 初次使用时可根据每次病毒用量进行合理的分装,不过分装最小体积不宜小于10 μl(吉凯基因AAV产品均已分装为50μl/管,除用量极少的情况下,一般无需再次分装);
3. 病毒分装或一次不能用完时,一定要确保无菌操作,保证病毒的纯净状态;
4. 病毒当天未用完但明天会接着用,可直接4℃保存过夜,因为-80℃保存会增加冻融次数严重影响AAV滴度;
5. AAV需要稀释后使用时,按需稀释,稀释后的病毒需一次性用完,不要再冻存于-80℃。
//8.为什么很多动物实验用特异性启动子表达外源基因? 阅读文献,我们经常看到如下载体结构pAAV9-CaMKIIα-eNpHR3.0-mCherry,pAAV-HCRApoE/hAAT-Pcsk9(D377Y),其中CaMKIIα和HCRApoE/hAAT就是特异性启动子。由于常规AAV血清型具有广泛的组织亲噬性,为了将基因表达限定于目的细胞,则需要利用特异性启动子表达外源基因。 组织特异性启动子目前已被广泛应用于神经、肌肉、骨骼、心血管、眼科、肝脏、肾脏、脂肪、胰腺等多个研究领域,吉凯基因通过挖掘文献,搜罗了一大批特异性启动子,助力动物实验: 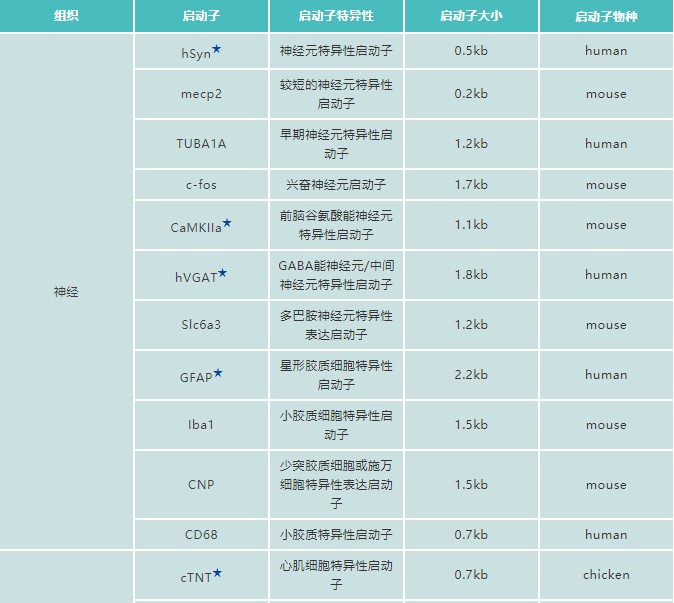
腺相关病毒(AAV)已经成为基因传递载体,成为许多人类疾病潜在基因治疗的载体。迄今为止,AAV在176项I、II和III期临床试验中的安全性在及其至少八种人类疾病中的功效现已得到明确记录。但常规血清型由于存在广泛的组织亲噬性,其用于基因治疗有潜在的脱靶性。
此外,具有特异性感染某一细胞能力的AAV,对常规科研也大有裨益,不仅能减少注射病毒的量,达到减少成本的目的,也能获得较优的实验数据。
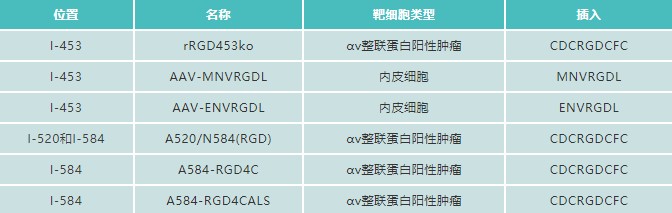
要达到上述目的,就得对AAV的外壳进行改造,使其专一性地感染特定细胞。常规手段有针对外壳进行突变(如针对耳的Anc80L65),或者插入靶向肽(如针对骨的DSS肽)而实现:

扫码添加微信获取原文和更多科研资料,免费直播讲座 |