Olink Proteomics品牌商
1 年
手机商铺
- NaN
- 0
- 1
- 2
- 1
推荐产品
公司新闻/正文
Olink助力首医团队建立肺癌免疫治疗效果与毒性预测模型
361 人阅读发布时间:2025-10-30 11:18
研究背景
免疫治疗革命性地改变了晚期非小细胞肺癌(NSCLC)等疾病的治疗格局。然而,其临床应用仍面临三大核心挑战:首先,仅部分患者能从治疗中持久获益;其次,原发性和获得性耐药现象普遍存在;再者,部分患者会出现严重免疫相关不良事件。目前临床常用的疗效预测标志物,如肿瘤组织PD-L1表达水平和肿瘤突变负荷(TMB)的预测效能有限,且依赖有创组织活检的检测方式存在取样偏差、时空异质性等固有局限。这些瓶颈共同催生了一个亟待解决的临床需求:开发基于外周血的非侵入性液体活检生物标志物,以实现安全、动态且精准的疗效预测与毒性预警。

首都医科大学团队在《Molecular Biomedicine》(IF=10.1)发表的重磅研究,通过血浆蛋白质组学分析,成功建立了可预测PD-1/PD-L1抑制剂疗效和毒性的新型生物标志物模型,为"个体化免疫治疗"提供了重要工具。
试验设计
研究采用“发现队列+验证队列”的双队列设计。来自北京胸科医院的34例晚期NSCLC患者(IIIB-IV期)被纳入发现队列,另外30名接受免疫检查点抑制剂(ICI)治疗的患者被纳入验证队列。其中,发现队列于ICI治疗前7天内采集基线样本,2个治疗周期后采集治疗后样本,共58份配对样本,验证队列仅采集基线期样本。采用Olink Immuno-Oncology Panel检测分析了92种免疫相关蛋白在ICI治疗前后的动态变化及筛选预测性生物标志物。
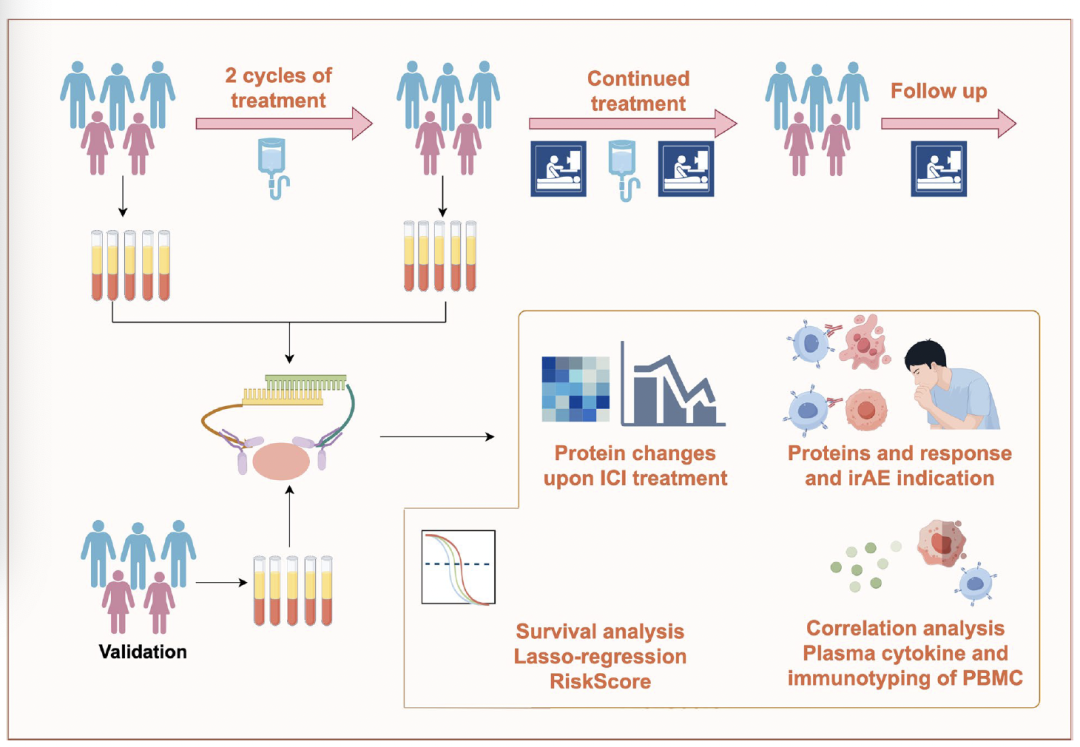
试验设计
亮点结果
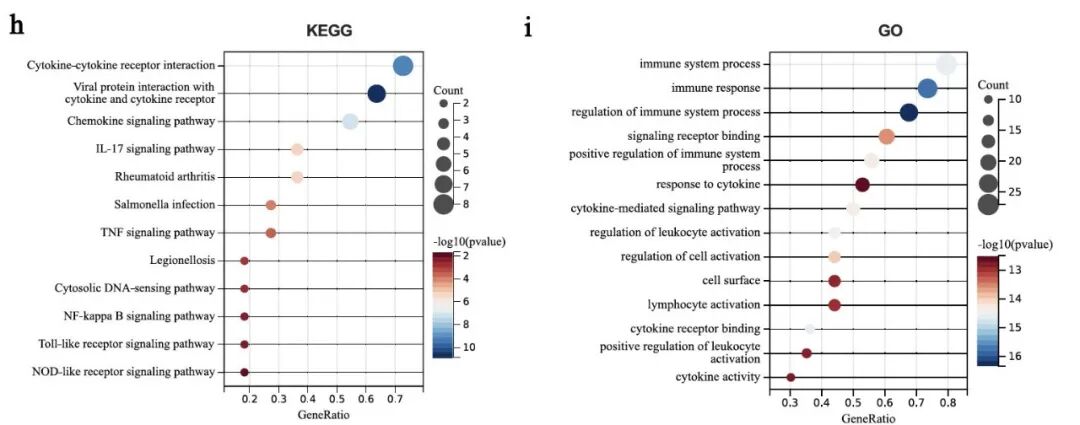
KEGG和GO分析
ICI治疗疗效与毒性预测
研究团队通过进一步研究NSCLC患者ICI治疗前后蛋白水平的动态变化,揭示了与治疗响应和毒性相关的关键分子特征。
相较于非PR患者,治疗前PR组患者血浆中4种蛋白显著上调(IL18、TNF、TNFRSF、GZMH),5种蛋白显著下调(LAMP3、IL2、ANGPT1、TNFSF14、CXCL10)。值得注意的是,免疫检查点抑制剂(ICI)治疗后KLRD1和PD-L2水平的升高与更优的ICI疗效呈正相关。
治疗前高表达的6种蛋白(CD28、LAMP3、CXCL9、ANGPT1、PTN、MMP12)与PD风险显著相关;而治疗后血浆中CD40L、MCP4和PGF水平的升高,以及HO-1水平的降低,则提示疗效不佳。
发生irAEs(免疫相关不良反应)的患者具有独特的蛋白表达特征:治疗前血浆IL-4和IL-13水平较高,但CXCL13和TNFRSF9水平较低;治疗后IL-18和GZMA的升高也与irAEs的发生相关。
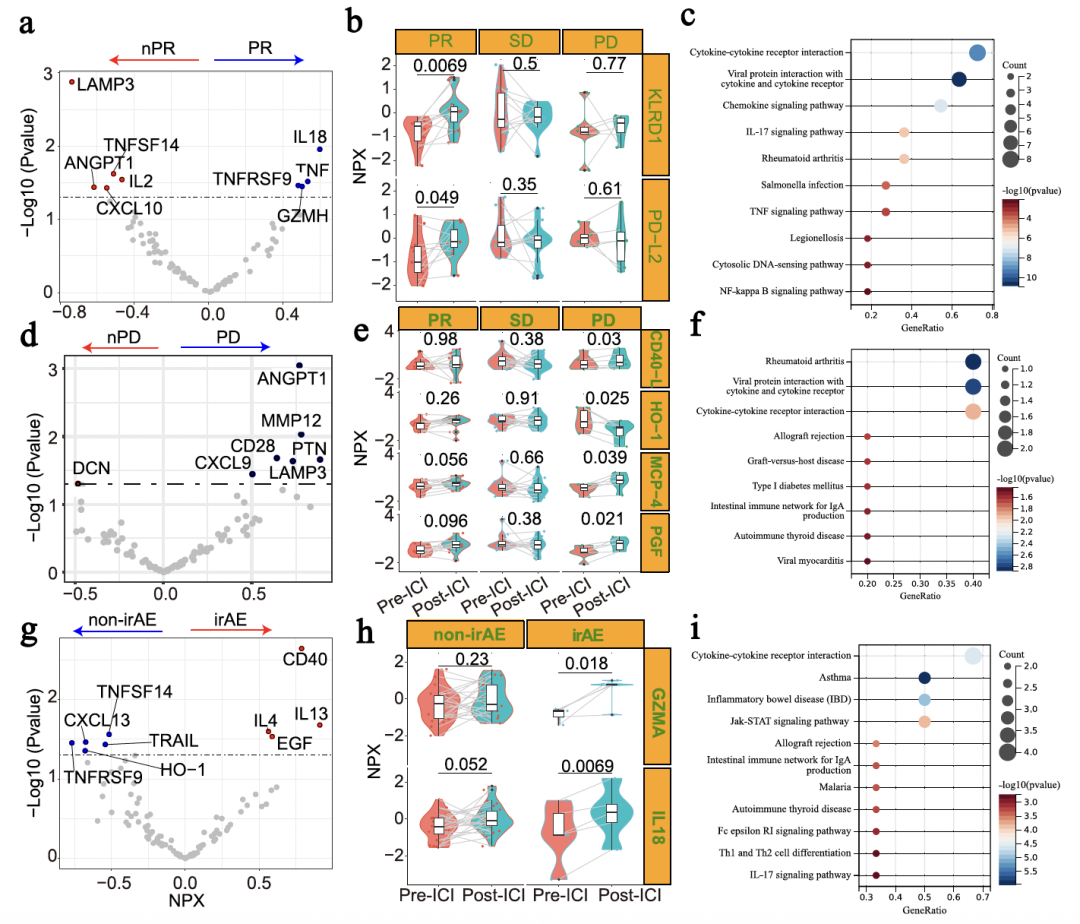
验证队列的30份基线期血浆样本检测显示,9种与PR相关的蛋白中,有5种蛋白(ANGPT1, TNF, CXCL10, TNFSF14和TNFRSF9)得到了验证,可以作为预测ICI治疗疗效的候选生物标志物。治疗前血浆CXCL13、CD40、TRAIL、TNFSF14和TNFRSF9也被证实可作为NSCLC患者irAEs的生物标志物。
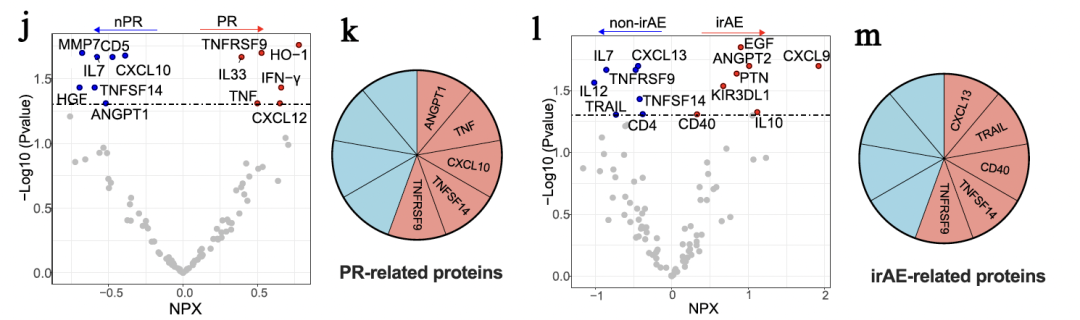
免疫检查点抑制剂治疗反应及毒性的血浆蛋白质组学研究
基于血浆蛋白的ICI治疗生存风险评分的建立与评估
基于单变量Cox回归分析,研究人员筛选出9种与不良总生存期(OS)显著相关的血浆蛋白(GZMA、CD28、TNFSF14、CXCL10、ADA、CD83、HO-1、ARG1、MIC-A/B),以及2种与良好OS相关的蛋白(EGF、CCL23)。
进一步通过LASSO-Cox回归分析,从上述候选标志物中优化筛选出8种核心蛋白(ARG1、CCL23、TNFSF14、CXCL10、CD28、TNFRSF9、GZMA、ADA),据此构建了名为"I-SCORE"的预后风险模型。该模型能有效区分患者为高风险组和低风险组——在发现队列与验证队列中,高风险组的OS均显著短于低风险组。
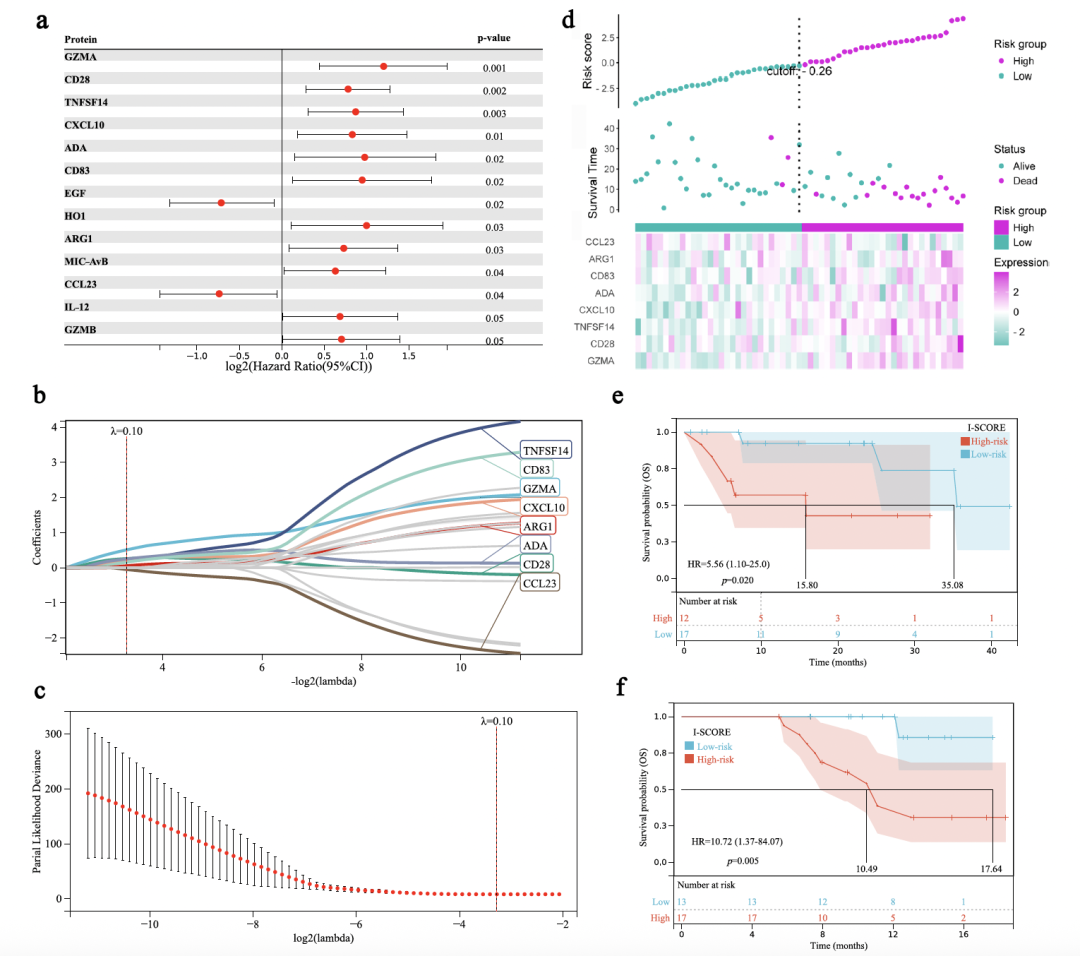
ROC曲线显示,I-SCORE模型对6,12,18个月OS的预测AUCs分别能达到0.97,0.94和0.95,显著优于单个蛋白;而对于PFS和ICIs治疗反应预测效果则和单个蛋白相当。
I-SCORE与NSCLC患者的促炎反应及免疫抑制相关
将I-SCORE与炎症因子、免疫细胞表型关联进一步分析显示,高风险组的患者表现出明显的促炎症和免疫抑制特征,其体内促炎性细胞因子(如IL-6、IL-7和IL-10)水平较高,而免疫刺激因子(如IL-33和EGF)水平较低,表明I-SCORE高风险患者因处于“促炎+免疫抑制”状态,无法有效响应ICIs治疗。这一发现进一步揭示了I-SCORE风险评分的生物学意义。
写在最后
本研究采用前瞻性、双队列(发现队列+验证队列)设计,基于Olink PEA高特异性蛋白检测技术,精准捕捉了非小细胞肺癌患者接受免疫检查点抑制剂治疗前后外周血蛋白的动态变化,成功筛选出与疗效和毒性密切相关的关键蛋白标志物。
该研究不仅发现了可预测ICI疗效和毒性的非侵入性生物标志物,更创新性地构建了I-SCORE生存风险评分模型,能精准区分高/低风险患者,显著提升治疗决策的科学性。这一突破性成果为临床提供了一种安全、便捷、高效的液体活检工具,助力实现个体化免疫治疗。
期待未来能再更大规模人群中进一步验证该研究的临床价值,并基于这些标志物探索增强免疫疗效的新型联合治疗策略,推动肺癌精准医疗再上新台阶!
1. Gao Y, Qi F, Zhou W, Jiang P, Hu M, Wang Y, Song C, Han Y, Li D, Qin N, Zhang H, Luo H, Zhang T, Li H. Liquid biopsy using plasma proteomics in predicting efficacy and tolerance of PD-1/PD-L1 blockades in NSCLC: a prospective exploratory study. Mol Biomed. 2025 Jul 15;6(1):51. doi: 10.1186/s43556-025-00291-6. PMID: 40659985; PMCID: PMC12260144.