上海百英生物科技股份有限公司品牌商
6 年
手机商铺
- NaN
- 0.3999999999999999
- 0.3999999999999999
- 2.4
- 2.4
推荐产品
公司新闻/正文
尼帕病毒再敲警钟!高品质重组NiV蛋白为疫苗与中和抗体研发助力
276 人阅读发布时间:2026-03-25 10:18
近期,印度西孟加拉邦报告了尼帕病毒(Nipah Virus,NiV)感染病例,引起全球公共卫生领域的密切关注。作为一种被世界卫生组织列为重点优先研究病原体的高致死率病毒,尼帕病毒的病死率高达40%-75%,且目前尚无获批上市的疫苗或特异性抗病毒药物。
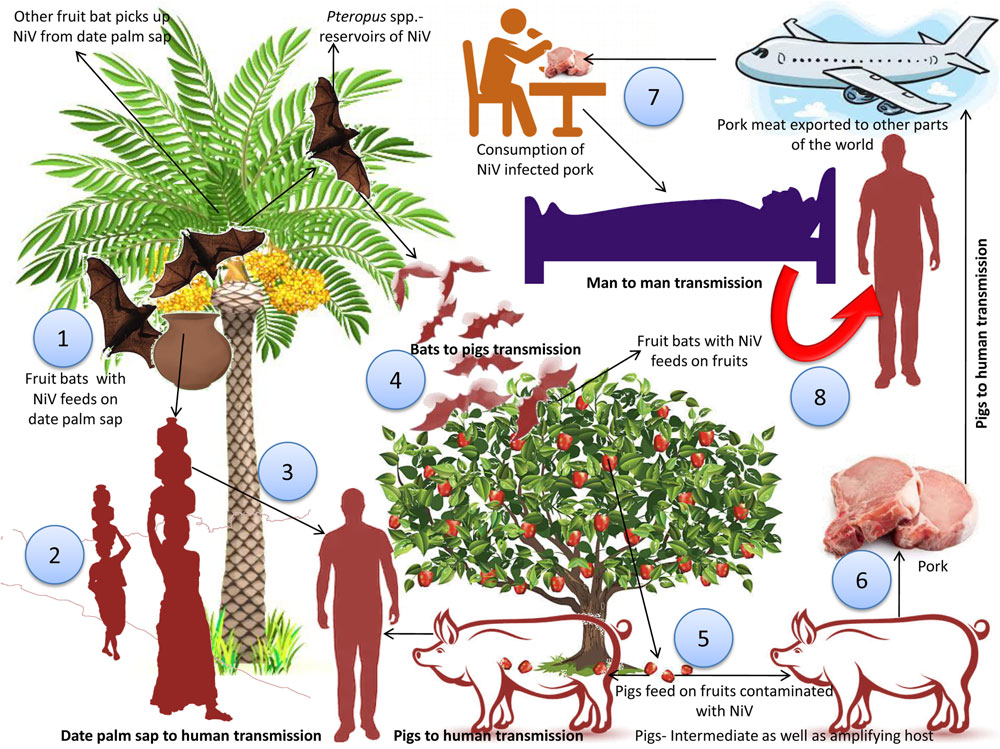
图1 尼帕病毒传播
(doi: 10.1080/01652176.2019.1580827.)
尼帕病毒属于副黏病毒科(Paramyxoviridae)亨尼帕病毒属(Henipavirus),与亨德拉病毒(Hendra virus,HeV)同属。它是一种具有囊膜的单股负链RNA病毒,病毒粒子呈多形性,通常为球形或丝状,直径约120-500纳米。
NiV基因组长度约为18.2 kb,是副黏病毒科中基因组较大的病毒之一。基因组由6个结构基因组成,按照3′-N-P-M-F-G-L-5′的顺序排列,分别编码6种结构蛋白:
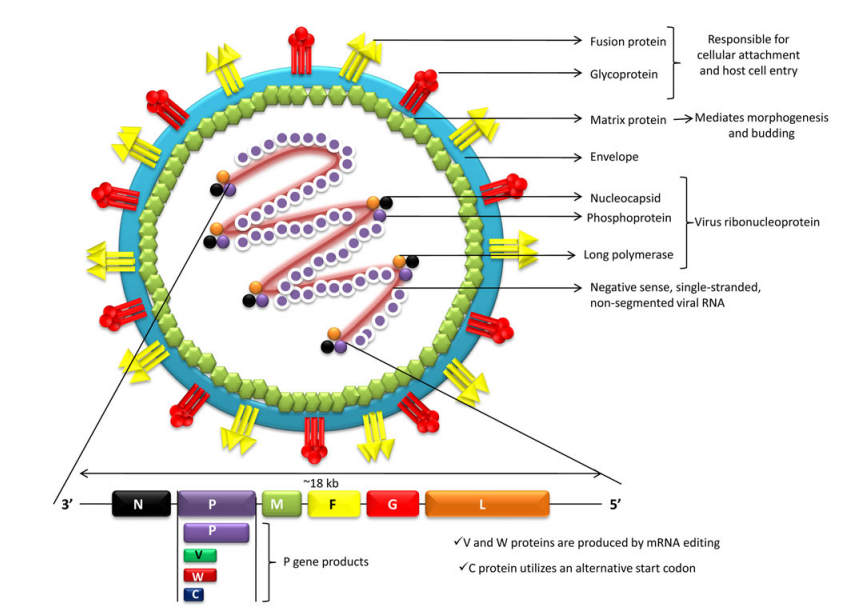
图2 Nipah Virus结构图
(doi: 10.1080/01652176.2019.1580827.)
多项研究证实,尼帕病毒的F蛋白(融合蛋白) 和G蛋白(糖蛋白) 是诱导中和免疫反应的关键靶点。传统研究多关注G蛋白的受体结合功能,而F蛋白(融合蛋白) 则是病毒与宿主细胞膜融合过程中不可或缺的“引擎” 。F蛋白在病毒表面以两种构象存在:融合前构象(Pre-fusion) 和融合后构象(Post-fusion)。其中,Pre-fusion蛋白是激发机体产生保护性中和抗体的关键靶点。
近日,复旦大学团队研发的脂肽融合抑制剂VQ-P1-EK3-C16,正是靶向F蛋白的HR1区域,阻断6-HB形成,从而抑制病毒膜融合过程。该脂肽抑制剂活性比已进入临床的抗体强562倍。这一成果凸显了稳定的融合前构象F蛋白在抗病毒药物筛选中的关键价值——精准的构象是高效药物发现的基石。

融合前构象高度不稳定,极易发生构象改变。百英生物自主研发的Recombinant (NiV) Pre-Fusion Glycoprotein/His Strep Protein产品正是针对这一核心需求而设计,并具备以下显著特点:
-
精准的融合前构象:通过序列优化稳定了预融合构象,确保蛋白抗原表位天然暴露。这是筛选能够阻断膜融合过程的广谱保护性中和抗体的核心工具 。
-
完善的标签系统(His & Strep):双标签设计不仅便于通过多种方法(镍柱、Strep-Tactin)进行温和高效的纯化与检测,同时保留了蛋白的天然构象和生物活性,适用于多种实验平台。
-
高质量的表达系统:采用哺乳动物细胞(如HEK293)真核表达系统,确保复杂的翻译后修饰(如糖基化)正确无误,这对抗体的特异性识别至关重要。
-
高纯度与批间稳定性:我们执行严格的质量控制标准,SDS-PAGE纯度>95%,批次间一致性高,让您的实验数据更可靠。