推荐产品
技术资料/正文
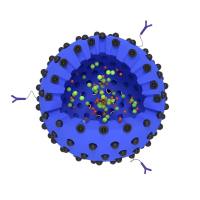
抗EGFR抗体修饰脂质体 靶向EGFR的免疫脂质体 用于增强EGFR阳性肿瘤治疗
492 人阅读发布时间:2025-09-25 09:23
什么是EGFR及抗EGFR抗体?
表皮生长因子受体(Epidermal Growth Factor Receptor,EGFR):一类跨膜受体酪氨酸激酶,在细胞增殖、分化和存活过程中发挥关键作用。在多种恶性肿瘤中(如非小细胞肺癌、结直肠癌、头颈鳞癌),EGFR常发生异常高表达或突变,驱动肿瘤发生与发展。
抗EGFR抗体:一类专门针对EGFR胞外结构域的单克隆抗体,通过与受体结合阻断配体(如EGF、TGF-α)结合位点,抑制受体活化及下游信号通路,从而抑制肿瘤细胞的生长、增殖和转移。
抗EGFR抗体的特点
高特异性:能够精确识别并结合EGFR,避免对非靶点分子的干扰。
多重作用机制:不仅阻断信号通路,还可介导抗体依赖性细胞毒作用(ADCC)和补体依赖性细胞毒作用(CDC)。
临床验证:已有多种抗EGFR抗体药物获批并应用于肿瘤治疗,疗效明确。
联合应用潜力:常与放疗、化疗、免疫治疗等形成协同效应。
目前应用和研究较多的抗EGFR单克隆抗体主要包括:
西妥昔单抗(Cetuximab):嵌合型单克隆抗体,已广泛用于结直肠癌和头颈鳞癌。
帕尼单抗(Panitumumab):全人源化单克隆抗体,免疫原性更低,主要用于晚期结直肠癌。
尼妥珠单抗(Nimotuzumab):人源化抗体,毒副作用较轻,已在头颈癌和胶质瘤中应用。
Necitumumab:第二代全人源单克隆抗体,用于晚期肺鳞癌。
这些抗体的成功应用奠定了EGFR靶向治疗的临床基础,但单药治疗依旧存在疗效受限、耐药性及全身副作用等挑战。
抗EGFR抗体修饰脂质体的优势与作用
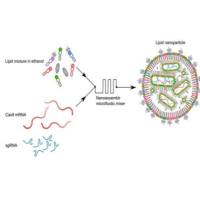
为克服传统抗EGFR抗体和化疗药物的局限性,研究者提出了抗EGFR抗体修饰脂质体。这一策略将纳米药物递送系统与分子靶向结合,形成多层次、精准化的治疗工具。
优势与作用包括:
靶向递送:通过抗EGFR抗体的“导航”功能,使脂质体能够主动识别并聚集于肿瘤细胞表面,显著提高药物在肿瘤区域的浓度。
增强内吞作用:EGFR介导的内吞可促进脂质体进入细胞,使载药高效释放,提高杀伤效果。
降低系统毒性:靶向分布减少药物在正常组织的积累,显著改善患者耐受性。
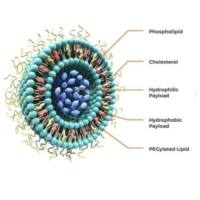
多样化载荷:脂质体可负载化疗药物、siRNA、mRNA乃至免疫调节分子,拓展了治疗策略。
协同治疗潜力:可与放疗、免疫检查点抑制剂联合,构建多模态治疗体系。
抗EGFR抗体修饰脂质体整合了抗体的靶向特异性与纳米载体的高效递送能力,为肿瘤精准治疗提供了强有力的新工具。它不仅有望突破传统EGFR抑制剂耐药和毒副作用的瓶颈,还可能成为未来个体化治疗的重要平台。
在精准医学和纳米药物不断发展的背景下,抗EGFR抗体修饰脂质体无疑代表着肿瘤治疗领域的新方向,展现出从科研走向临床应用的巨大潜力。